Clear Sky Science · fr
Nanocapsules chitosane‑sulfate de dextrane pour améliorer l’efficacité de la tigécycline contre Salmonella enterica non typhique
Pourquoi cela importe pour la sécurité alimentaire
La plupart des gens connaissent Salmonella comme une cause fréquente d’intoxication alimentaire, souvent liée à la volaille insuffisamment cuite. Moins nombreux sont ceux qui réalisent que certaines souches sont devenues si résistantes aux antibiotiques que même des médicaments puissants « de dernier recours » peuvent échouer. Cette étude explore une approche basée sur la nanotechnologie pour sauver l’un de ces médicaments, la tigécycline, en l’encapsulant dans de minuscules capsules à base de sucres qui l’aident à pénétrer dans les cellules infectées et à neutraliser les mécanismes clés de résistance chez Salmonella.
La menace croissante des Salmonella résistants
Les sérovars non typhiques de Salmonella (NTS) sont une cause majeure de diarrhée et d’infections sanguines dans le monde, en particulier dans les pays à revenu faible ou intermédiaire. Les chercheurs ont examiné 12 souches de Salmonella enterica issues de viande de poulet et de canard en Égypte. Ces souches étaient résistantes à de nombreux antibiotiques couramment utilisés, y compris les pénicillines, les céphalosporines, les tétracyclines et d’autres, et présentaient des scores élevés de résistance multiple aux antibiotiques. Même la tigécycline, un médicament à large spectre réservé aux cas difficiles, était peu efficace : les bactéries toléraient des concentrations très élevées. Une raison majeure était la suractivité des « pompes d’efflux » — des machineries moléculaires situées dans la membrane bactérienne qui expulsent en permanence les antibiotiques hors de la cellule.
Concevoir une capsule médicamenteuse plus intelligente
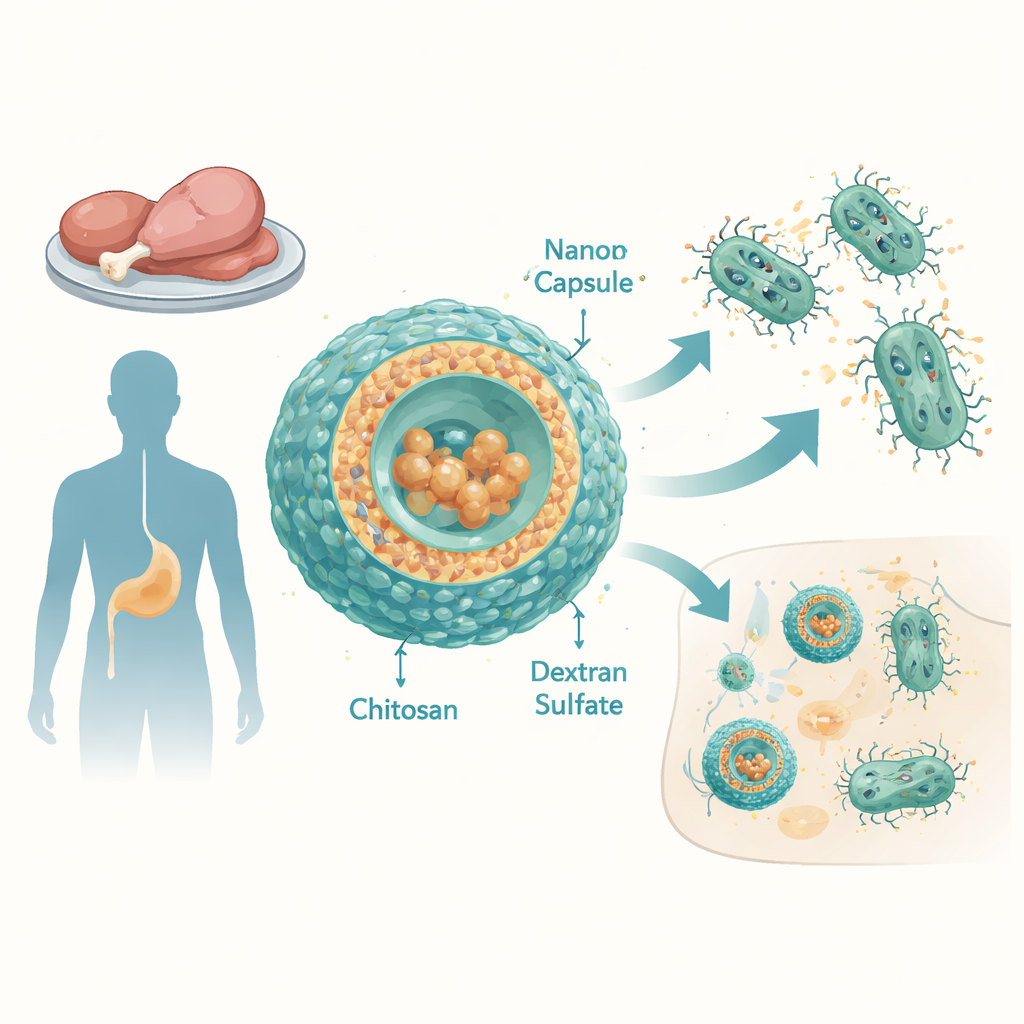
Pour surmonter cela, l’équipe a conçu des capsules à l’échelle nanométrique fabriquées à partir de deux polymères d’origine naturelle : le chitosane, obtenu à partir de la chitine (le matériau des coquilles de crustacés), et le sulfate de dextrane, une molécule de sucre ramifiée. En ajustant soigneusement les proportions de ces composants, ils ont produit des particules stables d’environ 100–150 nanomètres de diamètre, avec une charge de surface positive qui favorise leur interaction avec les membranes bactériennes et cellulaires de l’hôte. La tigécycline a été chargée dans ces particules avec une efficacité remarquable — pratiquement la totalité du médicament s’est retrouvée à l’intérieur des capsules. Dans des tests en laboratoire reproduisant les conditions du sang, les capsules ont libéré la majeure partie de leur tigécycline en quelques heures, suggérant qu’elles pourraient délivrer une forte impulsion d’antibiotique sur les sites d’infection.
Désactiver les défenses bactériennes
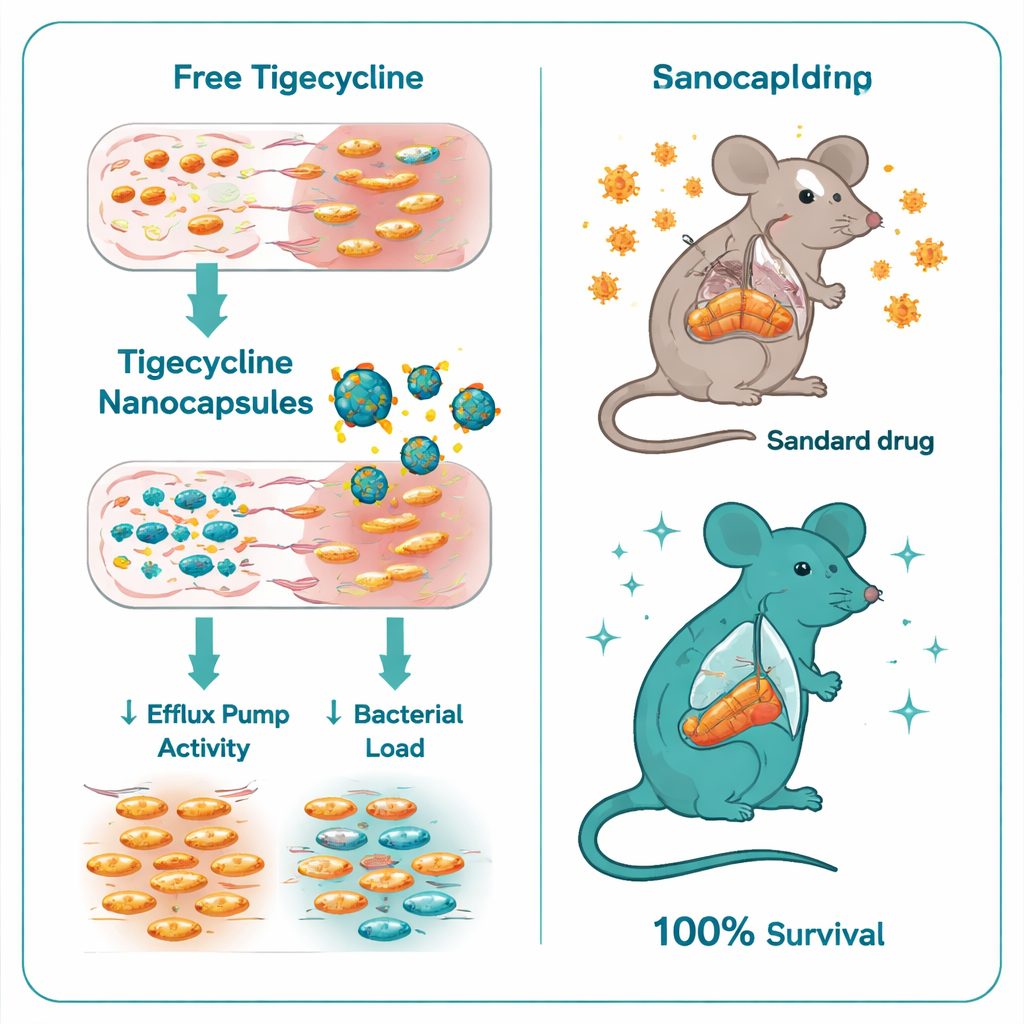
Lorsque les chercheurs ont comparé la tigécycline seule à la tigécycline encapsulée dans les nanocapsules chitosane–sulfate de dextrane, la différence a été saisissante. La concentration minimale de médicament nécessaire pour arrêter la croissance bactérienne est passée de 32–128 microgrammes par millilitre pour la tigécycline libre à seulement 0,5–1 microgramme par millilitre avec les nanocapsules — une amélioration d’un facteur six à sept. Des expériences de « time‑kill » ont montré que la forme encapsulée tuait Salmonella beaucoup plus rapidement et complètement. Au niveau génétique, les nanocapsules ont aussi réprimé des régulateurs clés de la résistance : l’expression des gènes ramA et acrB, qui contribuent à contrôler et former des pompes d’efflux majeures, a diminué de plusieurs fois chez les bactéries traitées. Autrement dit, les capsules n’ont pas seulement délivré plus de médicament ; elles ont aidé à couper l’une des principales voies d’évasion des bactéries.
Protection des souris infectées contre une maladie mortelle
L’équipe a ensuite testé la nouvelle formulation dans un modèle murin d’infection sévère par Salmonella Typhimurium. Les souris infectées non traitées sont toutes mortes en moins de huit jours. Les souris recevant la tigécycline standard ont mieux résisté mais ont présenté une mortalité encore élevée, seulement 40 % ayant survécu. En net contraste, toutes les souris traitées avec les nanocapsules chargées de tigécycline ont survécu. Ces animaux avaient beaucoup moins de bactéries dans leur foie et leurs intestins, des analyses sanguines plus proches d’une fonction hépatique et rénale normale, et des lésions tissulaires bien plus légères à l’examen microscopique. Même les capsules chitosane–sulfate de dextrane « vides », sans antibiotique, ont offert une certaine protection, probablement parce que le chitosane possède lui‑même des effets antimicrobiens et anti‑inflammatoires modestes, mais la combinaison avec la tigécycline était clairement supérieure.
Ce que cela pourrait signifier pour les traitements futurs
Pour les non‑spécialistes, le message central est que l’encapsulation d’un antibiotique existant dans une nanocapsule intelligente et biocompatible peut restaurer son efficacité contre des Salmonella hautement résistants. En aidant le médicament à atteindre des bactéries cachées à l’intérieur des cellules et en diminuant les pompes qui expulsent normalement le médicament, le système chitosane–sulfate de dextrane a transformé un antibiotique de dernier recours en difficulté en un traitement très efficace chez la souris, avec 100 % de survie. Bien que des travaux supplémentaires soient nécessaires avant d’envisager une utilisation chez l’homme ou chez les animaux d’élevage, cette approche offre une voie prometteuse pour prolonger la durée d’utilisation des antibiotiques importants et améliorer la sécurité de notre approvisionnement alimentaire sans devoir inventer de nouveaux médicaments entièrement nouveaux.
Citation: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Mots-clés: Salmonella, résistance aux antibiotiques, nanoparticules, libération de médicaments, tigécycline