Clear Sky Science · fr
La protéomique et la métabolomique intégrées révèlent que des lactones sesquiterpéniques végétales inhibent l’activité des cellules TNBC en épuisant la synthèse d’ATP et en reprogrammant le métabolisme primaire
Composés végétaux qui affament un cancer du sein agressif
Le cancer du sein triple‑négatif est l’une des formes les plus difficiles à traiter, car il manque les « poignées » hormonales habituelles auxquelles de nombreux médicaments se fixent. Cette étude examine deux molécules extraites d’une plante médicinale qui semblent couper les centrales internes de ces cellules cancéreuses, interrompant leur apport énergétique tout en épargnant les cellules mammaires normales. Comprendre ce mécanisme pourrait ouvrir la voie à des traitements plus ciblés et plus doux pour des patientes qui disposent aujourd’hui de peu d’options.
Pourquoi cibler la source d’énergie du cancer est essentiel
Toute cellule dépend de petites structures appelées mitochondries pour produire l’ATP, le carburant de base de la cellule. Les cellules cancéreuses, en particulier les plus agressives, dépendent souvent de façon accrue de leurs mitochondries pour soutenir une croissance rapide, la dissémination et la survie en conditions de stress. Les chercheurs se sont concentrés sur des cellules de cancer du sein triple‑négatif, qui représentent environ 15–20 % des cancers du sein et rechutent et métastasent plus souvent que d’autres types. Ils ont étudié une molécule naturelle, la déoxyléléphantopine (DET), et sa cousine optimisée DETD‑35, toutes deux des lactones sesquiterpéniques issues de la plante médicinale Elephantopus. Des travaux antérieurs montraient que ces composés déclenchent un stress oxydatif et des formes inhabituelles de mort cellulaire dans les cellules cancéreuses, mais la manière dont ils perturbent les centrales énergétiques des cellules restait mal comprise.
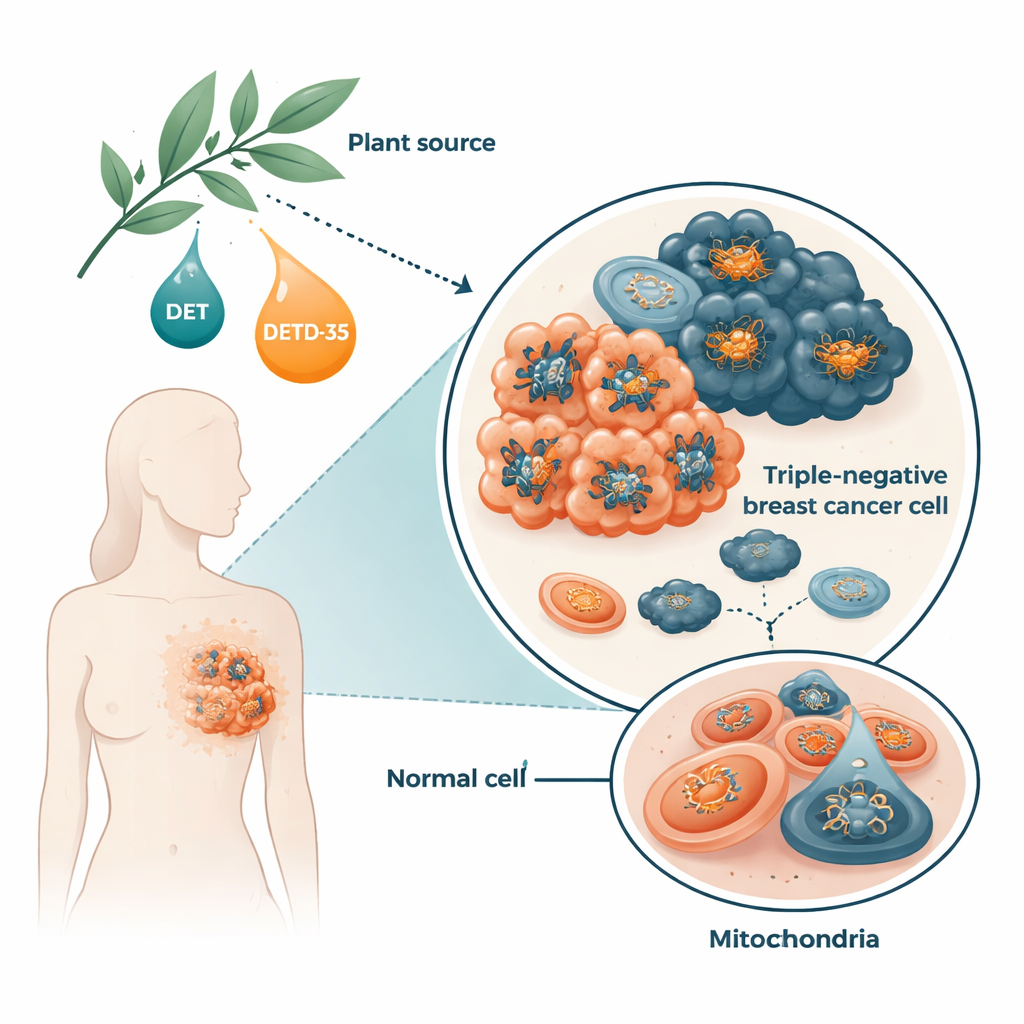
Comment les molécules végétales perturbent les mitochondries des cellules cancéreuses
En utilisant des cellules humaines de cancer du sein triple‑négatif cultivées en laboratoire, l’équipe a constaté que DET et DETD‑35 augmentaient rapidement la production d’espèces réactives de l’oxygène, un type de « fumée » chimiquement réactive générée lors de la production d’énergie. En réponse, les cellules ont renforcé certaines enzymes protectrices, mais pas suffisamment pour rétablir l’équilibre. Les composés ont également forcé l’ouverture d’un canal dans la membrane mitochondriale connu sous le nom de pore de perméabilité de transition, une modification liée au gonflement, à la perte du potentiel de membrane et aux premières étapes de la mort cellulaire. En seulement quelques heures, les niveaux d’ATP à l’intérieur des cellules cancéreuses ont chuté fortement. Lorsque les chercheurs ont préalablement ajouté un antioxydant, ces effets délétères ont été largement inversés, montrant que le stress oxydatif jouait un rôle central dans le processus.
Cartographier les dommages aux protéines et au métabolisme
Pour comprendre la situation dans son ensemble, les scientifiques ont combiné deux approches « omiques » puissantes. Ils ont répertorié des milliers de protéines mitochondriales et mesuré de nombreux petits métabolites dans des cellules traitées versus non traitées. Cette vue intégrée a révélé que DET et DETD‑35 perturbaient des protéines impliquées dans la phosphorylation oxydative, la principale voie utilisée par les mitochondries pour produire de l’ATP, et activaient des signaux liés à la mort cellulaire. Parallèlement, des voies métaboliques centrales traitant les acides aminés, les lipides et les éléments constitutifs de l’ADN ont été reconfigurées. Certains lipides qui contribuent à la structure de la membrane mitochondriale interne, ainsi que des molécules liées aux défenses antioxydantes et à la dégradation du sucre, ont évolué de manière cohérente avec un état de cellules stressées et privées d’énergie. De manière cruciale, ces changements généralisés n’ont pas été observés dans des cellules mammaires normales exposées aux mêmes doses, suggérant un certain degré de sélectivité pour les cellules tumorales.
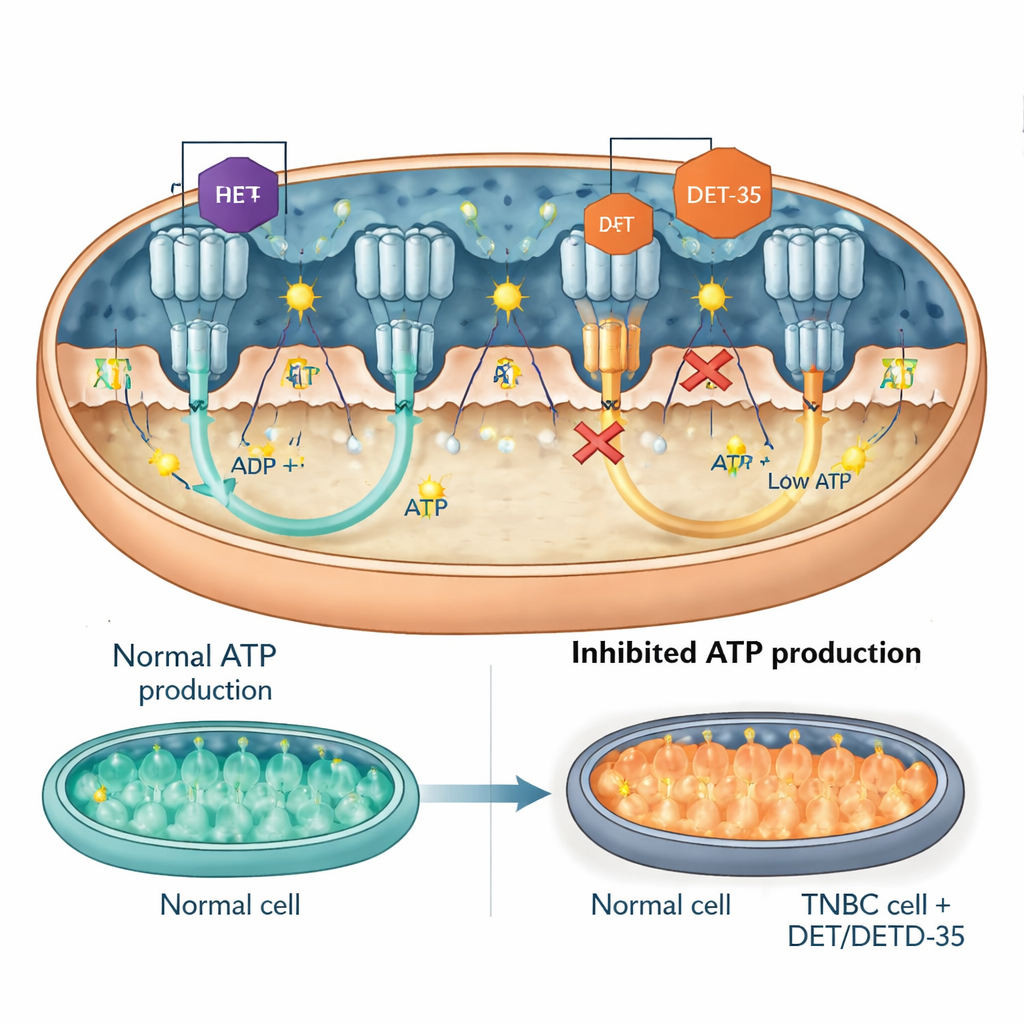
Une protéine de signalisation clé et la turbine ATP elle‑même
L’équipe s’est ensuite concentrée sur des acteurs spécifiques au sein de ces réseaux perturbés. L’un d’eux était PRKCA, une protéine de signalisation qui peut migrer vers les mitochondries et influencer à la fois la production d’énergie et les réponses au stress. DET et DETD‑35 augmentaient les niveaux de PRKCA dans les cellules cancéreuses. Lorsque les chercheurs ont utilisé des outils génétiques pour réduire l’expression de PRKCA, les drogues sont devenues moins toxiques : les cellules cancéreuses avaient davantage de chances de survivre, produisaient plus d’ATP et montraient moins de signes de dysfonction mitochondriale et d’apoptose. Un autre élément clé était l’ATP synthase, la « turbine » moléculaire qui tourne pour créer de l’ATP. Les mesures ont montré que DET et DETD‑35 réduisaient directement l’activité de l’ATP synthase dans les mitochondries des cellules cancéreuses. Des modèles de docking informatique ont suggéré que les deux composés se logent à des interfaces critiques de l’enzyme, les mêmes régions générales où se fixent des inhibiteurs connus de l’ATP synthase, entravant physiquement son mouvement et réduisant la production d’ATP. Chez des souris porteuses de tumeurs humaines triple‑négatives, le traitement par l’un ou l’autre composé abaissait les niveaux de composants de l’ATP synthase dans le tissu tumoral, soutenant les résultats obtenus en culture cellulaire.
Ce que cela pourrait signifier pour les traitements futurs du cancer
Globalement, l’étude dessine un tableau cohérent : ces composés d’origine végétale poussent les cellules de cancer du sein triple‑négatif dans une crise énergétique en les surchargeant de stress oxydatif, en ouvrant les pores mitochondriaux et en bloquant directement la machinerie de production d’ATP. À mesure que l’ATP diminue et que le métabolisme est bouleversé, les cellules cancéreuses perdent leur capacité à croître et à survivre, tandis que les cellules mammaires normales restent en grande partie indemnes dans les mêmes conditions. Pour un lecteur non spécialiste, la conclusion est que les scientifiques pourraient exploiter la forte dépendance du cancer à ses centrales internes, en utilisant des molécules conçues — certaines inspirées par des plantes — pour décharger les batteries des cellules tumorales sans couper l’alimentation des tissus sains. Il faudra encore beaucoup de travail avant que de tels agents puissent atteindre la clinique, mais cette vision intégrée des protéines, des métabolites et du flux énergétique offre une feuille de route prometteuse.
Citation: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Mots-clés: cancer du sein triple-négatif, mitochondries, ATP synthase, produits naturels, métabolisme du cancer