Clear Sky Science · fr
Cadre piloté par l’IA pour la détection précise de la maladie d’Alzheimer dans l’EEG
Pourquoi les ondes cérébrales comptent pour la perte de mémoire
La maladie d’Alzheimer mine progressivement la mémoire et l’autonomie ; toutefois, lorsque les symptômes deviennent évidents, une grande partie des dégâts est déjà faite. Les médecins ont un besoin urgent de méthodes pour repérer la maladie plus tôt, en utilisant des outils sûrs, abordables et pratiques pour les bilans de routine. Cette étude examine si de simples enregistrements d’ondes cérébrales — électroencéphalogrammes, ou EEG — combinés à l’intelligence artificielle moderne peuvent révéler des signes cachés d’Alzheimer bien avant qu’ils ne soient visibles sur les images cérébrales ou dans la vie quotidienne.
Écouter le cerveau sans chirurgie
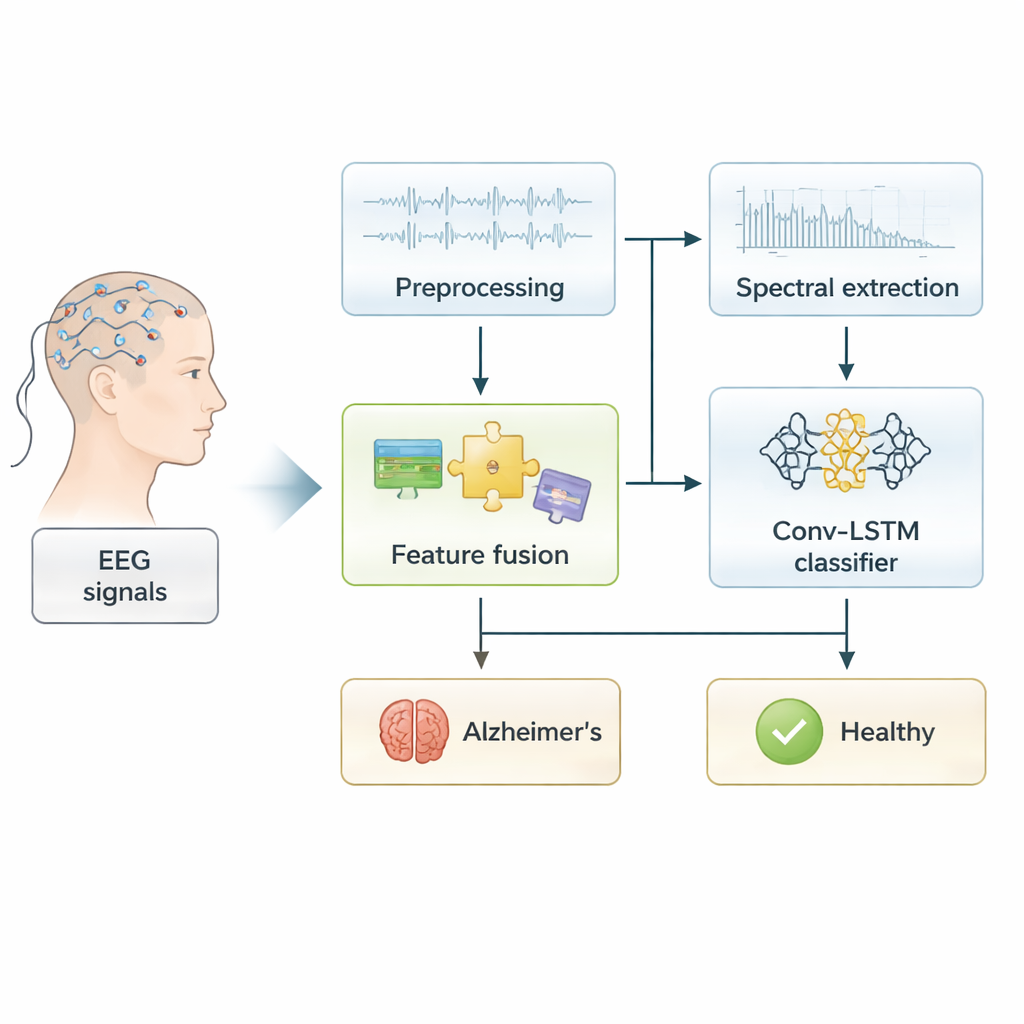
L’EEG est un examen indolore où de petits électrodes placés sur le cuir chevelu captent l’activité électrique du cerveau. Il est bien moins coûteux et plus portable que l’IRM ou la tomographie par émission de positons (TEP) et peut être répété fréquemment. Cependant, les signaux EEG bruts sont désordonnés. Ils contiennent beaucoup de bruit dû aux clignements, aux mouvements musculaires et à l’environnement, et les motifs liés à Alzheimer peuvent être subtils et répartis sur de nombreuses régions cérébrales et fréquences. Traditionnellement, les chercheurs se concentraient soit sur des résumés mathématiques conçus à la main de ces signaux, soit utilisaient des réseaux d’apprentissage profond qui apprennent des motifs directement à partir des données brutes. Chaque approche a des forces mais aussi des angles morts importants.
Combiner deux façons d’observer l’activité cérébrale
Les auteurs proposent une stratégie hybride qui réunit le meilleur des deux approches. D’abord, ils nettoient les enregistrements EEG en filtrant le bruit indésirable et en corrigeant les dérives lentes du signal. Ensuite, ils extraient des caractéristiques « spectrales » qui décrivent comment la puissance électrique du cerveau se répartit entre différentes bandes de fréquence — des ondes lentes associées à la somnolence, par exemple, versus des rythmes plus rapides liés à l’attention. Ces mesures sont connues depuis longtemps pour évoluer dans la démence. Parallèlement, un réseau de neurones convolutionnel (CNN) spécialement conçu examine les données EEG de manière plus holistique, apprenant automatiquement des motifs spatiaux complexes qui peuvent échapper aux experts humains.
Apprendre à l’IA à lire les changements dans le temps
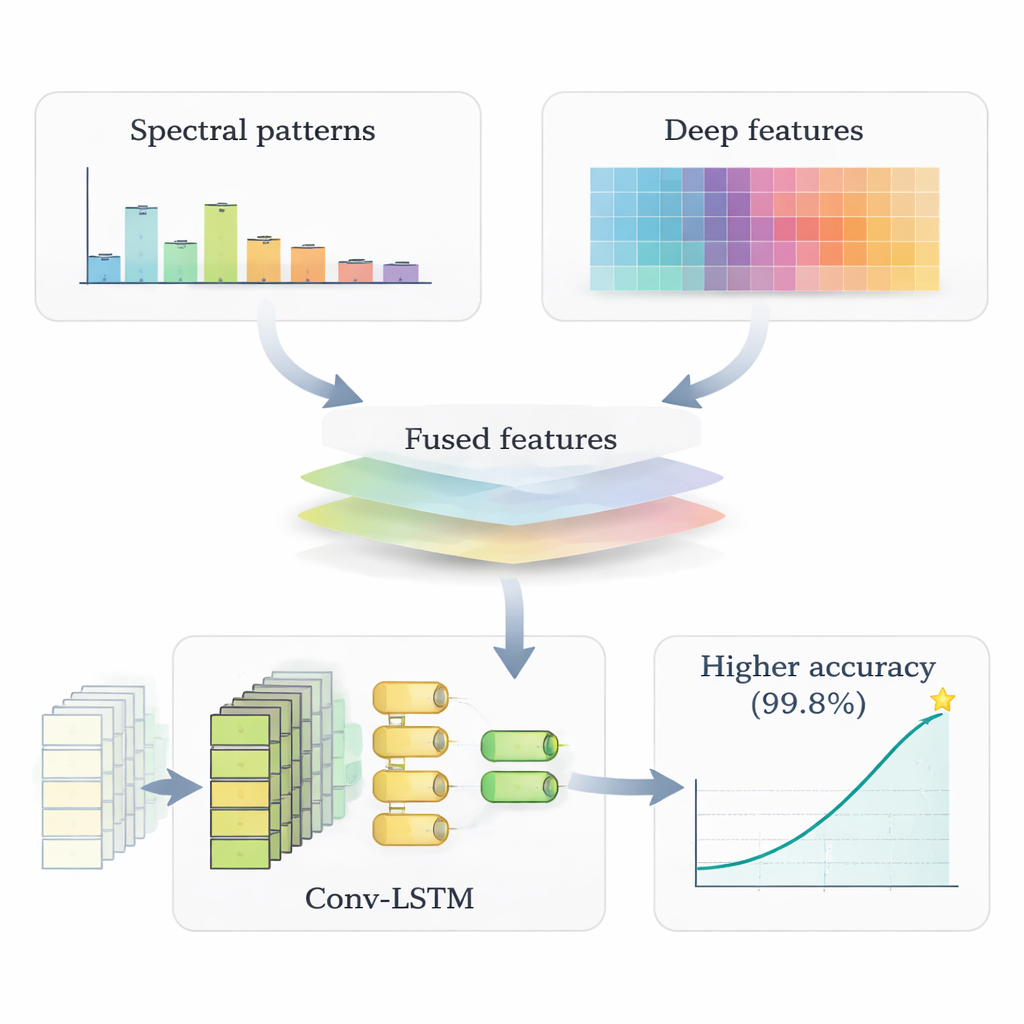
Plutôt que de traiter ces deux ensembles de caractéristiques séparément, le système les fusionne en une description unique et riche de l’activité cérébrale de chaque personne. Cette représentation combinée est ensuite alimentée dans un réseau plus avancé appelé modèle Convolutional Long Short-Term Memory (Conv-LSTM). La partie « convolutionnelle » capte la manière dont l’activité est organisée sur le cuir chevelu, tandis que la partie « LSTM » est conçue pour suivre l’évolution des motifs dans le temps, un peu comme suivre des phrases dans le langage parlé. En pratique, le modèle apprend à la fois où et quand apparaissent les changements liés à Alzheimer dans l’EEG, en utilisant environ 0,9 million de paramètres entraînables — suffisamment compact pour s’exécuter sur du matériel standard.
Quelle est l’efficacité du système ?
Les chercheurs ont testé leur cadre sur des données EEG en état de repos provenant de personnes âgées avec et sans maladie d’Alzheimer. Ils ont séparé les enregistrements en jeux d’entraînement, de validation et de test final, et évalué les performances à l’aide de mesures standard d’exactitude et de fiabilité. Le modèle Conv-LSTM basé sur la fusion a correctement distingué les cas d’Alzheimer des cas non-Alzheimer dans 99,8 % des instances — nettement mieux que plusieurs systèmes de comparaison, incluant des CNN seuls, des réseaux LSTM seuls et des approches classiques d’apprentissage automatique. Les modèles dépourvus soit des caractéristiques spectrales, soit des caractéristiques apprises en profondeur étaient systématiquement moins précis, soulignant la valeur de la combinaison de points de vue complémentaires sur les mêmes signaux cérébraux.
Ce que cela peut signifier pour les patients et les cliniques
Pour un non-spécialiste, la conclusion est simple : en laissant l’intelligence artificielle écouter plus attentivement les ondes cérébrales, cette méthode transforme un test familier et à faible risque en un puissant système d’alerte précoce pour la maladie d’Alzheimer. Les résultats suggèrent qu’un outil EEG automatisé et relativement léger pourrait aider les cliniciens à dépister les patients en contextes de soins courants, en signalant ceux qui nécessitent un suivi plus approfondi ou des examens d’imagerie avancés. Bien que des études plus larges et plus diverses soient encore nécessaires avant que de tels systèmes puissent orienter des décisions thérapeutiques, cette recherche préfigure un avenir où des enregistrements routiniers des ondes cérébrales, interprétés par des algorithmes intelligents, contribuent à détecter la démence plus tôt et plus précisément, donnant potentiellement aux patients et à leurs familles plus de temps pour planifier et bénéficier des thérapies émergentes.
Citation: Hemalatha, B., Venkatachalam, K., Siuly, S. et al. AI-driven framework for accurate detection of Alzheimer’s disease in EEG. Sci Rep 16, 5509 (2026). https://doi.org/10.1038/s41598-026-35184-3
Mots-clés: Maladie d’Alzheimer, ondes cérébrales EEG, apprentissage profond, diagnostic précoce, IA médicale