Clear Sky Science · fr
Des bactéries alimentaires et du microbiote intestinal produisent du méthylglyoxal et ce métabolite conduit à la formation d’alcaloïdes 1‑acétyl‑β‑carboline bioactifs
Pourquoi le laboratoire chimique de votre intestin compte
À l’intérieur de nos intestins et dans de nombreux aliments fermentés, des trillions de bactéries transforment en permanence les sucres que nous consommons en une multitude de sous‑produits chimiques. Cette étude examine en détail l’une de ces voies : comment certaines bactéries communes transforment les sucres en un composé très réactif appelé méthylglyoxal, puis en une famille de molécules bioactives appelées 1‑acétyl‑β‑carbolines. Parce que ces substances sont liées à la fois à des processus pathologiques et à de potentielles nouvelles thérapies, comprendre quand et comment les bactéries les produisent pourrait modifier notre manière de penser l’alimentation, le microbiome et la santé.
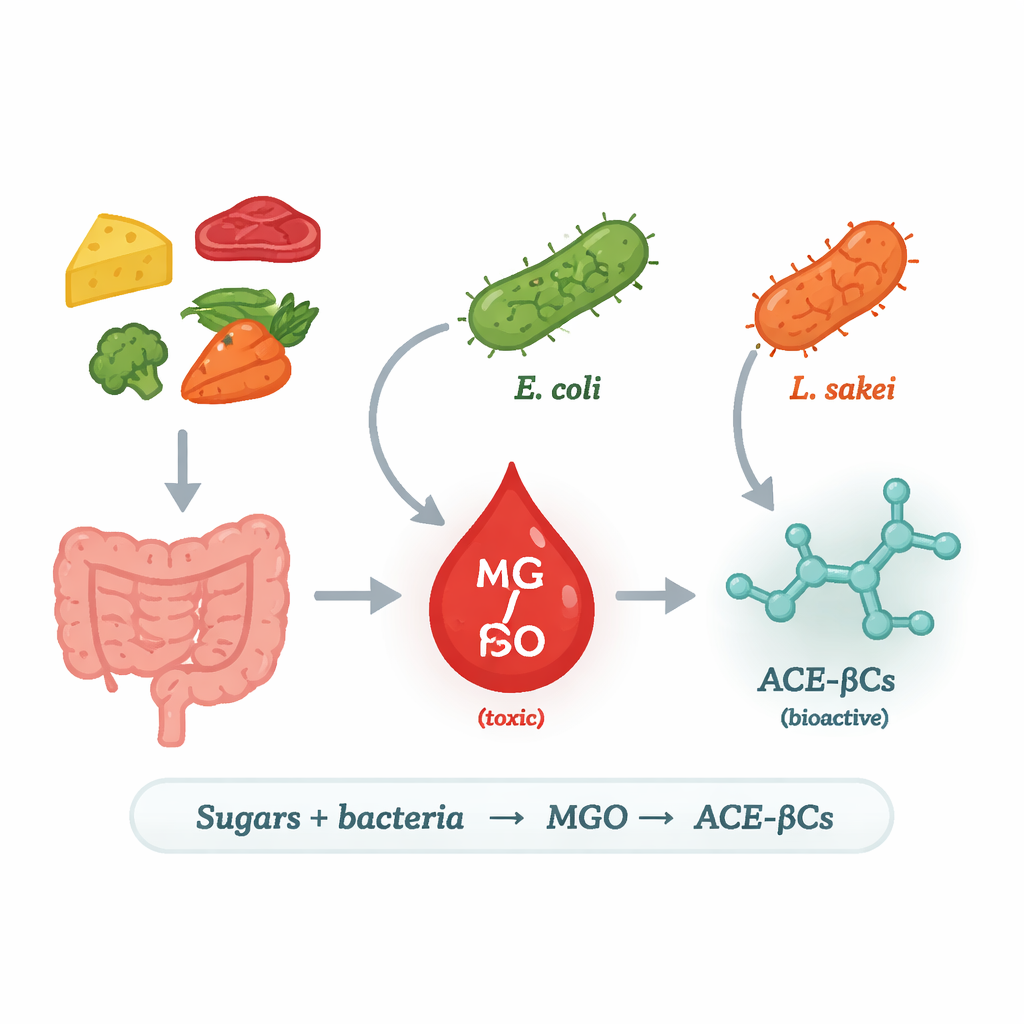
Des sucres quotidiens à une molécule risquée
Les chercheurs se sont concentrés sur le méthylglyoxal (MGO), un sous‑produit très réactif et toxique de la dégradation des sucres. Chez l’humain, un excès de MGO est associé au diabète, aux maladies cardiaques et à la neurodégénérescence parce qu’il peut endommager les protéines et l’ADN. Nos cellules contrôlent normalement le MGO grâce à des systèmes de détoxification, mais elles ne sont pas la seule source : les bactéries peuvent aussi produire du MGO. Chez certains microbes, une enzyme appelée méthylglyoxal synthase (MgsA) convertit un intermédiaire du métabolisme des sucres directement en MGO, créant un « raccourci » dans la métabolisation de l’énergie. L’équipe a cherché quelles bactéries alimentaires et intestinales utilisent cette voie, dans quelles conditions, et que devient le MGO qu’elles libèrent.
Qui sont les producteurs bactériens ?
Pour répondre à cette question, les scientifiques ont fait croître plusieurs souches de bactéries lactiques souvent présentes dans les aliments, ainsi qu’une souche de laboratoire d’Escherichia coli, dans un milieu contrôlé contenant soit du glucose soit du galactose. Ils ont ensuite suivi le MGO et deux alcaloïdes apparentés dans le liquide de culture au fil du temps à l’aide de chromatographie et de spectrométrie de masse de haute précision. Seuls E. coli et l’espèce associée aux produits carnés Lactilactobacillus sakei ont produit des quantités notables de MGO et des alcaloïdes ; les autres bactéries lactiques testées ne l’ont pas fait. Une recherche génomique a révélé la différence clé : E. coli et L. sakei possèdent le gène codant pour MgsA, alors que la plupart de leurs parentes lactiques ne l’ont pas. Lorsque les chercheurs ont inséré le gène mgsA de L. sakei dans une souche non‑productrice, la bactérie modifiée a commencé à produire à la fois du MGO et les alcaloïdes, établissant fermement le lien entre MgsA et cette voie.
Comment un MGO toxique devient des alcaloïdes bioactifs
La question suivante était de savoir ce qu’il advient du MGO une fois produit. L’équipe s’est intéressée aux alcaloïdes 1‑acétyl‑β‑carbolines (ACE‑βC), de petites molécules auxquelles on prête des activités antimicrobiennes, anti‑inflammatoires et anticancéreuses. Ils ont montré que lorsque des bactéries productrices de MGO étaient cultivées en présence de l’acide aminé L‑tryptophane, les niveaux de deux ACE‑βC — 1‑acétyl‑β‑carboline et sa forme 3‑carboxylique — augmentaient fortement. L’ajout de MGO supplémentaire au milieu favorisait également leur formation. Cela indique que le MGO diffuse hors des cellules et réagit spontanément avec le L‑tryptophane dans le liquide environnant, sans enzymes supplémentaires, pour générer ces composés bioactifs. Autrement dit, la même chimie qui rend le MGO dangereux le transforme aussi en molécules plus complexes susceptibles d’avoir des effets utiles.
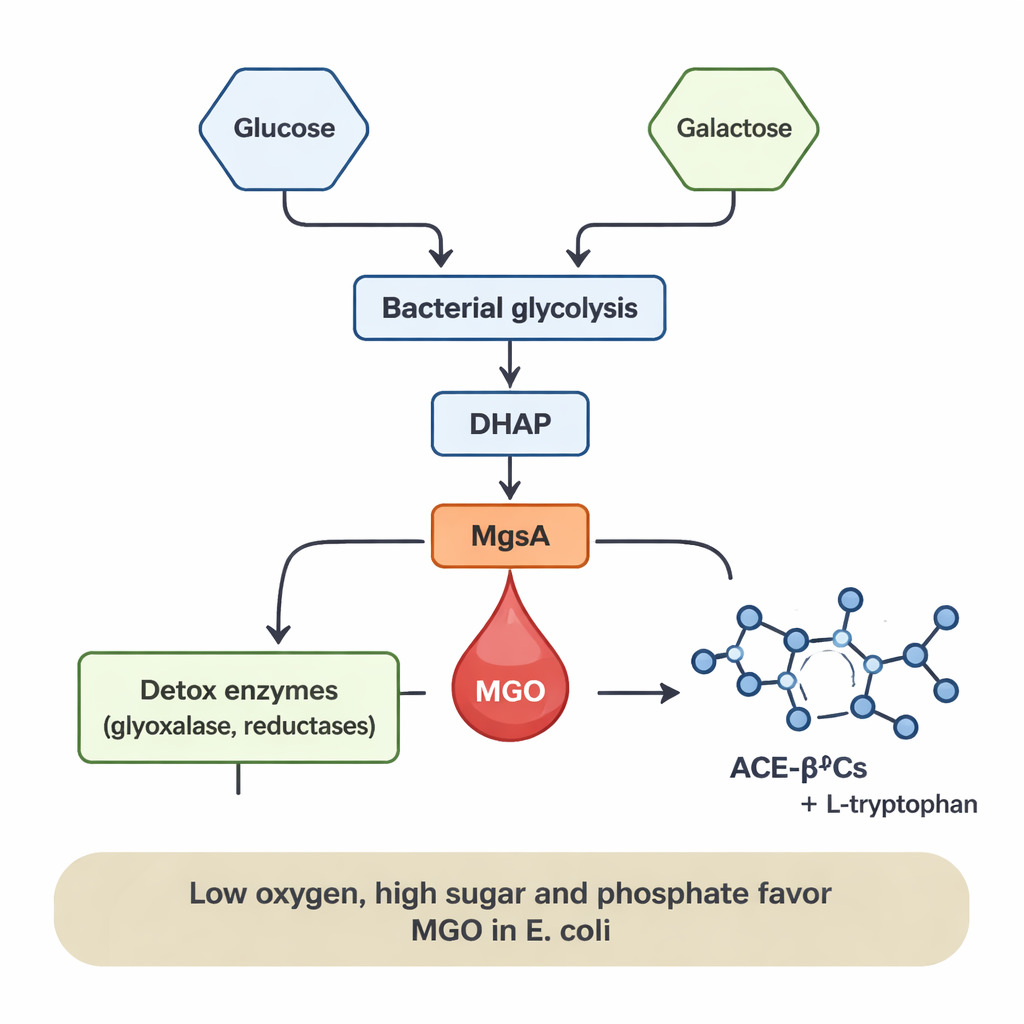
Ce qui augmente ou diminue la production
La production de MGO n’était pas fixe ; elle dépendait fortement du régime et de l’environnement des bactéries. Chez E. coli, le MGO n’apparaissait qu’en présence de glucose, et ses niveaux augmentaient avec la concentration en glucose. L’ajout de phosphate, un nutriment minéral courant, a encore multiplié la formation de MGO, vraisemblablement parce qu’il favorise l’accumulation d’intermédiaires phosphorylés du sucre qui alimentent le raccourci MgsA. Des conditions de faible oxygène (anaérobies) — similaires à celles de l’intestin humain — favorisaient aussi la libération de MGO, alors que des conditions riches en oxygène et bien aérés la réduisaient fortement bien que les bactéries continuent de bien croître. En revanche, L. sakei produisait principalement du MGO lorsqu’elle croissait sur du galactose, et la production augmentait avec des niveaux de galactose plus élevés. Ces schémas suggèrent que chaque fois que le flux de sucre dans le métabolisme bactérien est élevé et que l’oxygène est limité, le MGO peut agir comme une « soupape de sécurité », soulageant la pression d’accumulation des intermédiaires du sucre.
Quelles implications pour l’alimentation et la santé
Les résultats suggèrent que toutes les bactéries du microbiote ou des aliments ne se valent pas quant à leur capacité à fabriquer du MGO et des ACE‑βC. Les espèces qui portent l’enzyme MgsA, comme certaines souches de L. sakei et E. coli, peuvent être des contributeurs significatifs, notamment dans des environnements riches en sucres et pauvres en oxygène comme l’intestin ou certaines fermentations. Le MGO qu’elles excrètent pourrait s’ajouter à la charge chimique globale sur les tissus de l’hôte, mais sa conversion en alcaloïdes ACE‑βC peut aussi en partie « piéger » ce composé réactif tout en générant des molécules ayant leurs propres effets biologiques. Bien que cette étude ait été réalisée en cultures de laboratoire, elle met en lumière une voie plausible par laquelle l’alimentation, la composition du microbiote et le métabolisme bactérien façonnent ensemble l’équilibre entre substances nocives et potentiellement bénéfiques dans nos organismes, et elle souligne les ACE‑βC comme marqueurs possibles de la production bactérienne de MGO dans les aliments et l’intestin.
Citation: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Mots-clés: microbiote intestinal, méthylglyoxal, métabolisme bactérien, fermentation alimentaire, alcaloïdes β‑carboline