Clear Sky Science · fr
Dérivation d’un biomarqueur d’activité cérébrale intrinsèque pour la prédiction la plus précoce du déclin cognitif
Pourquoi les changements précoces du cerveau sont importants
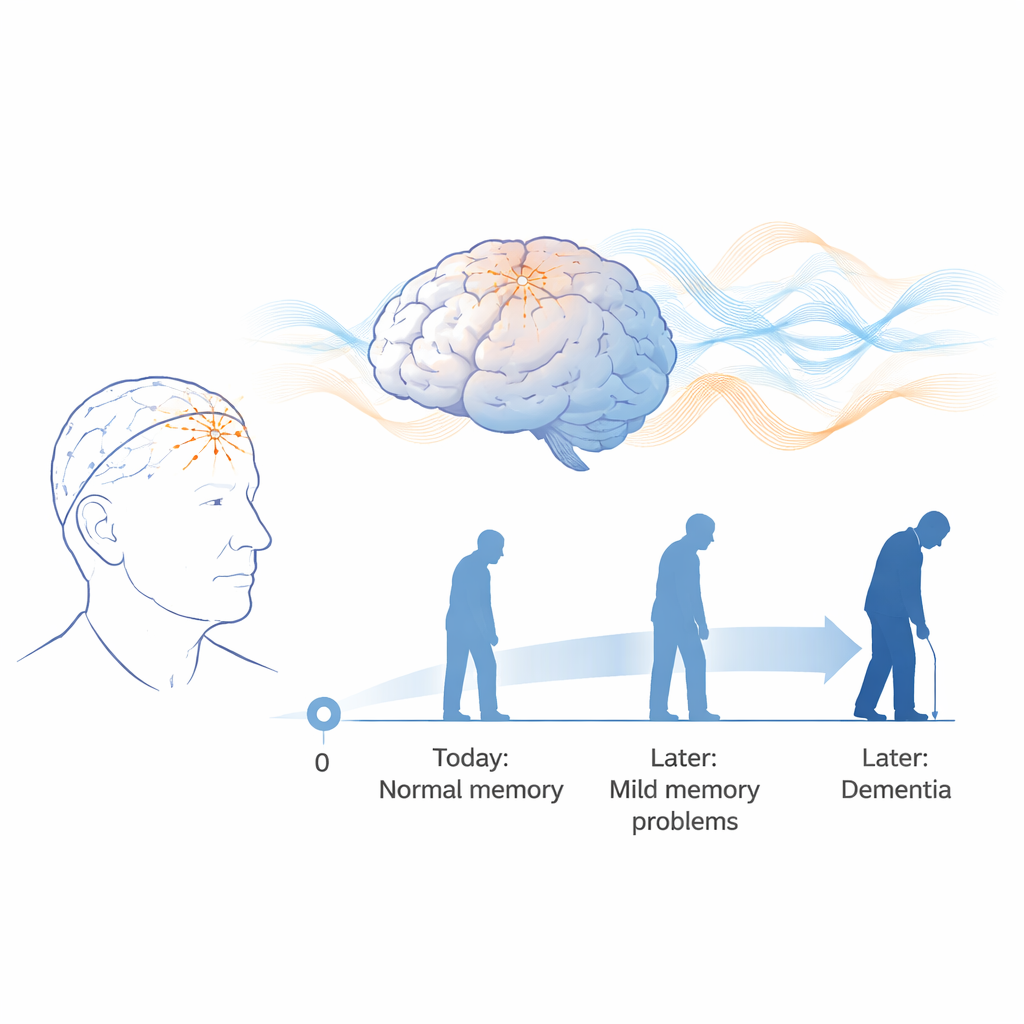
Beaucoup de personnes âgées remarquent de légères pertes de mémoire bien avant qu’un médecin ne puisse poser un diagnostic de démence. À ce stade, les scanners cérébraux et les analyses sanguines standard sont souvent normaux, et pourtant le processus pathologique sous-jacent peut déjà être en cours. Cette étude explore si un test simple et non invasif des ondes cérébrales — l’électroencéphalogramme, ou EEG — peut révéler des modifications très précoces du fonctionnement cérébral et prévoir de manière fiable qui est le plus susceptible de subir un déclin cognitif sévère des années plus tard.
Écouter les signaux discrets du cerveau
Les chercheurs se sont concentrés sur des personnes avec un « déclin cognitif subjectif » (DCS) : des adultes âgés qui sentent leur mémoire décliner mais obtiennent encore des performances normales aux tests standards. Quatre-vingt-huit volontaires de 52 à 85 ans ont bénéficié d’un EEG de repos de 20 minutes enregistré les yeux fermés, puis ont été suivis pendant 5 à 7 ans. Au cours du suivi, les médecins ont évalué l’état cognitif de chaque personne à l’aide d’échelles établies. À la fin de cette période, certains participants sont restés stables, tandis que d’autres ont évolué vers un trouble cognitif léger ou une démence. Ces résultats ont permis à l’équipe de se demander si des motifs subtils dans l’EEG initial auraient pu prédire qui se détériorerait par la suite.
Transformer les ondes cérébrales en empreinte prédictive
Plutôt que d’examiner l’EEG à l’œil nu, l’équipe a utilisé l’EEG quantitatif (qEEG), qui convertit les ondes brutes en milliers de caractéristiques numériques. Ces caractéristiques capturent l’intensité des différentes bandes de fréquence (comme les rythmes alpha et thêta), la synchronisation entre régions cérébrales distantes (connectivité et décalage de phase), et la complexité ou le désordre apparent du schéma d’activité global. Parce que le vieillissement normal modifie aussi l’EEG, les chercheurs ont ajusté mathématiquement toutes les caractéristiques en fonction de l’âge, puis les ont standardisées de sorte que « zéro » représente la valeur attendue pour une personne en bonne santé du même âge. Pour éviter le surapprentissage, ils ont réduit de façon systématique plus de 6 000 mesures candidates à un ensemble compact, stable, non redondant et le meilleur pour séparer les personnes qui resteraient stables de celles qui déclineraient.
L’apprentissage automatique comme boule de cristal
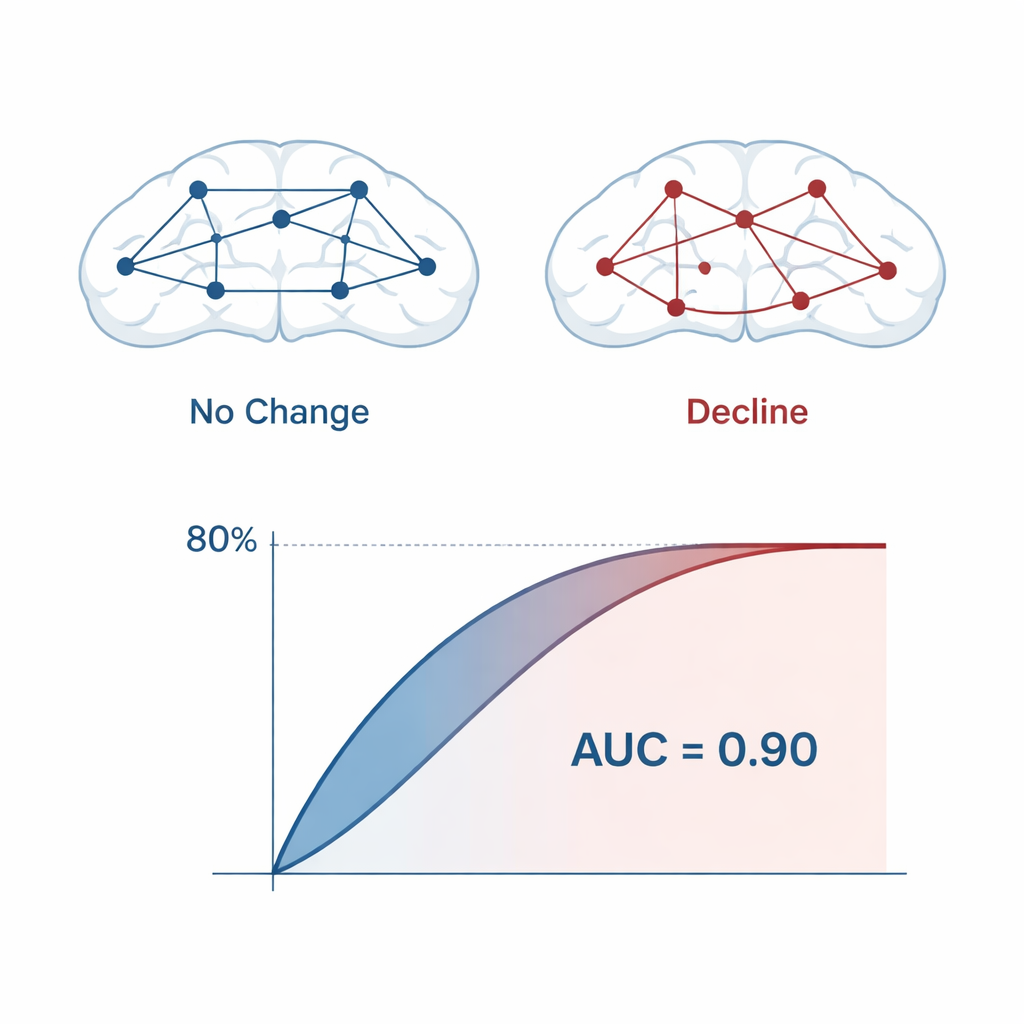
Avec cet ensemble réduit de caractéristiques, l’équipe a entraîné plusieurs modèles d’apprentissage automatique — régression logistique, machines à vecteurs de support et forêts aléatoires — pour estimer la probabilité de déclin futur de chaque participant. Des validations croisées répétées et une méthode bootstrap spécialisée ont été utilisées pour évaluer les performances de la manière la plus réaliste possible. Selon les modèles, la précision de prédiction était d’environ 80 %, avec une aire sous la courbe ROC (AUC) proche de 0,90, ce qui indique une forte capacité à distinguer les individus stables de ceux en déclin. Les modèles finaux verrouillés n’utilisaient que 14 caractéristiques qEEG, principalement issues des régions frontales enregistrées avec un petit jeu d’électrodes, rendant l’approche pratique pour un usage clinique courant.
Ce qui change dans le cerveau
Les caractéristiques les plus déterminantes pour une prédiction précise indiquaient une perturbation précoce de la communication entre les zones cérébrales. Les mesures de connectivité, en particulier le décalage de phase et l’asymétrie entre les régions frontales gauche et droite, étaient au centre du modèle. Des anomalies dans les bandes de fréquence alpha et thêta se distinguaient : une activité thêta augmentée ou décalée a été associée dans d’autres travaux à l’atrophie de l’hippocampe et à un amincissement cortical, tandis que des modifications de la puissance et de la fréquence alpha peuvent refléter les premières tentatives du cerveau pour compenser des lésions émergentes. Il est important de noter qu’aucune mesure EEG isolée ne racontait toute l’histoire. C’est la combinaison spécifique — « l’empreinte » du biomarqueur — qui signalait un risque accru des années avant l’apparition des symptômes francs.
Mettre l’outil à l’épreuve dans le monde réel
Pour vérifier si leur biomarqueur se généralise au-delà du groupe initial, les chercheurs l’ont testé sur deux cohortes indépendantes des États-Unis et d’Italie, chacune avec ses propres dispositifs d’enregistrement et caractéristiques des patients. Comme attendu sur des données vraiment nouvelles, la précision a légèrement diminué, jusqu’à environ 60–70 %, mais le modèle a quand même présenté des performances bien supérieures au hasard, suggérant que le signal qu’il capture est robuste. L’équipe a également montré que les cliniciens pouvaient ajuster le seuil de décision : l’abaissement du seuil augmente la sensibilité (détecter davantage de futurs déclinants au prix de plus de faux positifs), tandis que son relèvement augmente la spécificité (moins de faux positifs mais davantage de cas manqués). Cette flexibilité permet aux praticiens d’adapter l’outil aux priorités cliniques.
Ce que cela signifie pour les patients et les cliniciens
En termes simples, ce travail suggère qu’un enregistrement EEG court et indolore — utilisant seulement quelques électrodes au niveau du front — peut aider à identifier des personnes âgées qui paraissent normales aujourd’hui mais présentent un fort risque de déclin cognitif au cours des années suivantes. Bien que des études plus larges et des comparaisons avec d’autres biomarqueurs soient encore nécessaires, l’approche est peu coûteuse, non invasive et répétable, ce qui la rend attrayante pour un dépistage à grande échelle, notamment dans les contextes où l’imagerie avancée ou les analyses du liquide cérébrospinal sont impraticables. Si elle est validée plus avant, une telle biomarqueur fondé sur l’EEG pourrait aider les médecins à intervenir plus tôt, à surveiller la progression de la maladie et à sélectionner des participants pour des essais cliniques à l’étape où les traitements ont le plus de chances d’avoir un effet durable.
Citation: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Mots-clés: prédiction précoce de la démence, ondes cérébrales EEG, déclin cognitif subjectif, biomarqueur par apprentissage automatique, risque d’Alzheimer