Clear Sky Science · fr
Impact des méningiomes et des gliomes sur la dynamique cérébrale globale
Pourquoi les tumeurs cérébrales affectent plus qu’un seul point
Les tumeurs cérébrales sont souvent représentées comme des masses isolées qui compriment les tissus voisins. Mais nos pensées, nos mouvements et nos émotions dépendent de signaux qui se propagent à travers tout le cerveau. Cette étude pose une question apparemment simple aux implications larges : les tumeurs cérébrales courantes remodèlent-elles discrètement la façon dont l’ensemble du cerveau communique, même loin de la lésion visible — et, si oui, cela diffère-t-il entre deux types majeurs de tumeurs, les méningiomes et les gliomes ?
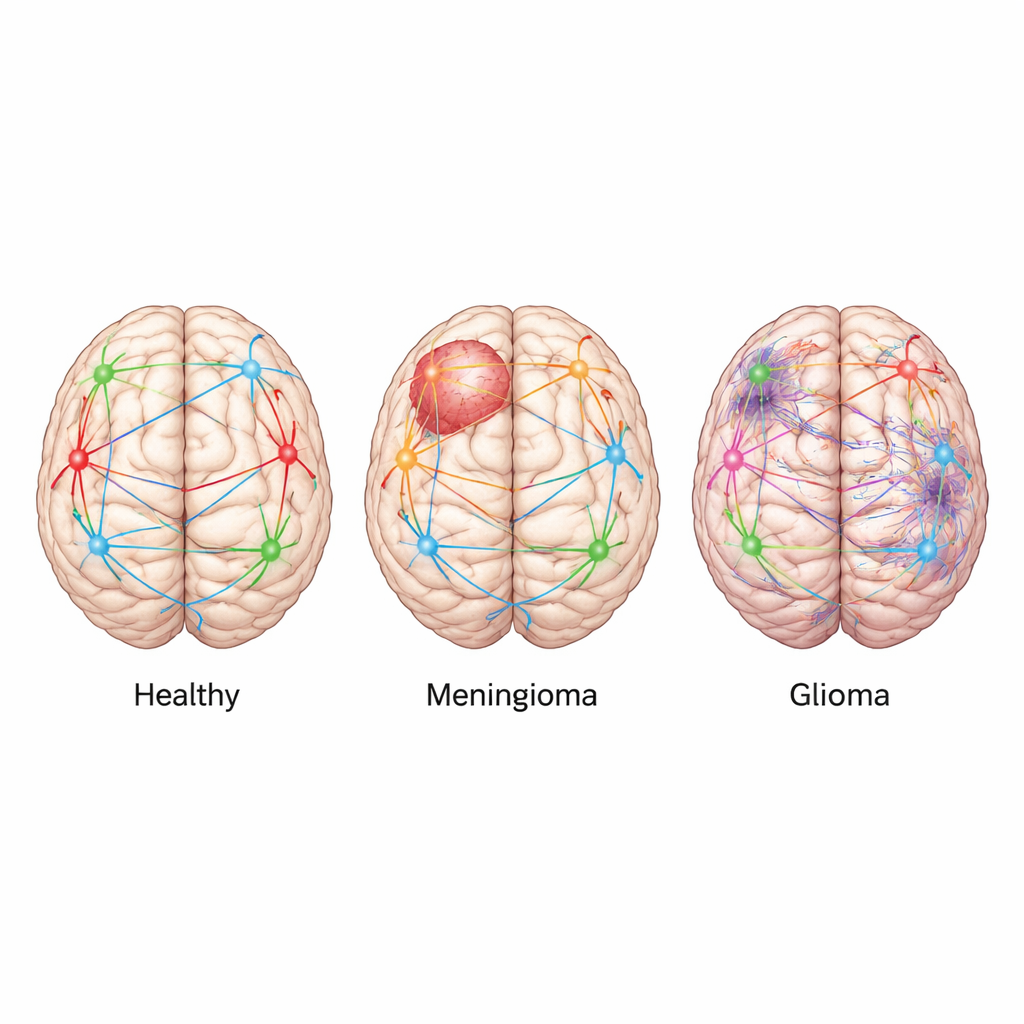
Deux tumeurs fréquentes au comportement très différent
Les méningiomes et les gliomes font partie des tumeurs cérébrales les plus fréquentes, mais leur comportement est très différent. Les méningiomes se développent généralement à partir des membranes protectrices du cerveau et ont tendance à pousser le tissu cérébral de l’extérieur, restant souvent bien délimités et à croissance lente. Les gliomes, en revanche, proviennent des cellules de soutien du cerveau et infiltrent le tissu environnant, s’immisçant dans les connexions cérébrales. Pour examiner comment ces modes de croissance distincts affectent la fonction cérébrale, les chercheurs ont utilisé des IRM de 34 adultes : 10 volontaires sains, 10 personnes atteintes de gliomes et 14 de méningiomes, tous scannés avant chirurgie en position de repos dans l’appareil.
Mesurer comment les signaux cérébraux se propagent et se modulent
Plutôt que de ne considérer que l’emplacement des tumeurs, l’équipe s’est concentrée sur la manière dont l’activité se déroule dans le temps à l’échelle de l’ensemble du cerveau. Ils ont utilisé l’IRM fonctionnelle au repos, qui suit les variations lentes du flux sanguin comme substitut de l’activité neuronale, et ont appliqué une approche computationnelle appelée Intrinsic Ignition Framework (cadre d’activation intrinsèque). En termes simples, ils ont posé deux questions : dans quelle mesure une bouffée locale d’activité dans une région peut-elle « enflammer » la communication à plus grande échelle dans le cerveau, et avec quelle flexibilité le cerveau alterne-t-il entre des états plus synchronisés et des états plus indépendants ? Ils ont appelé la première propriété « ignition intrinsèque » et la seconde « métastabilité », et ont calculé ces deux mesures pour chaque personne, ainsi que pour des régions et réseaux cérébraux spécifiques.
Les gliomes perturbent tout le réseau, les méningiomes surtout près de la tumeur
En comparant les groupes, un schéma net est apparu. Les personnes atteintes de gliomes présentaient une ignition et une métastabilité clairement réduites par rapport aux volontaires sains, ce qui signifie que leur cerveau était moins capable de diffuser des signaux locaux et moins flexible pour coordonner l’activité dans le temps. Ces perturbations apparaissaient même dans des régions qui semblaient indemnes sur les scans conventionnels, ce qui concorde avec le caractère infiltrant des gliomes, qui peuvent envoyer des filaments microscopiques loin de la masse principale. À l’inverse, les patients atteints de méningiomes affichaient des valeurs globales beaucoup plus proches de celles des témoins sains. Les modifications notables apparaissaient principalement dans les régions où la tumeur occupait plus d’environ un tiers de la surface, surtout pour l’ignition, ce qui suggère que la compression peut diminuer la capacité d’une région à impulser la communication tout en laissant une grande partie de l’architecture réseau intacte tant que la charge n’est pas trop importante.
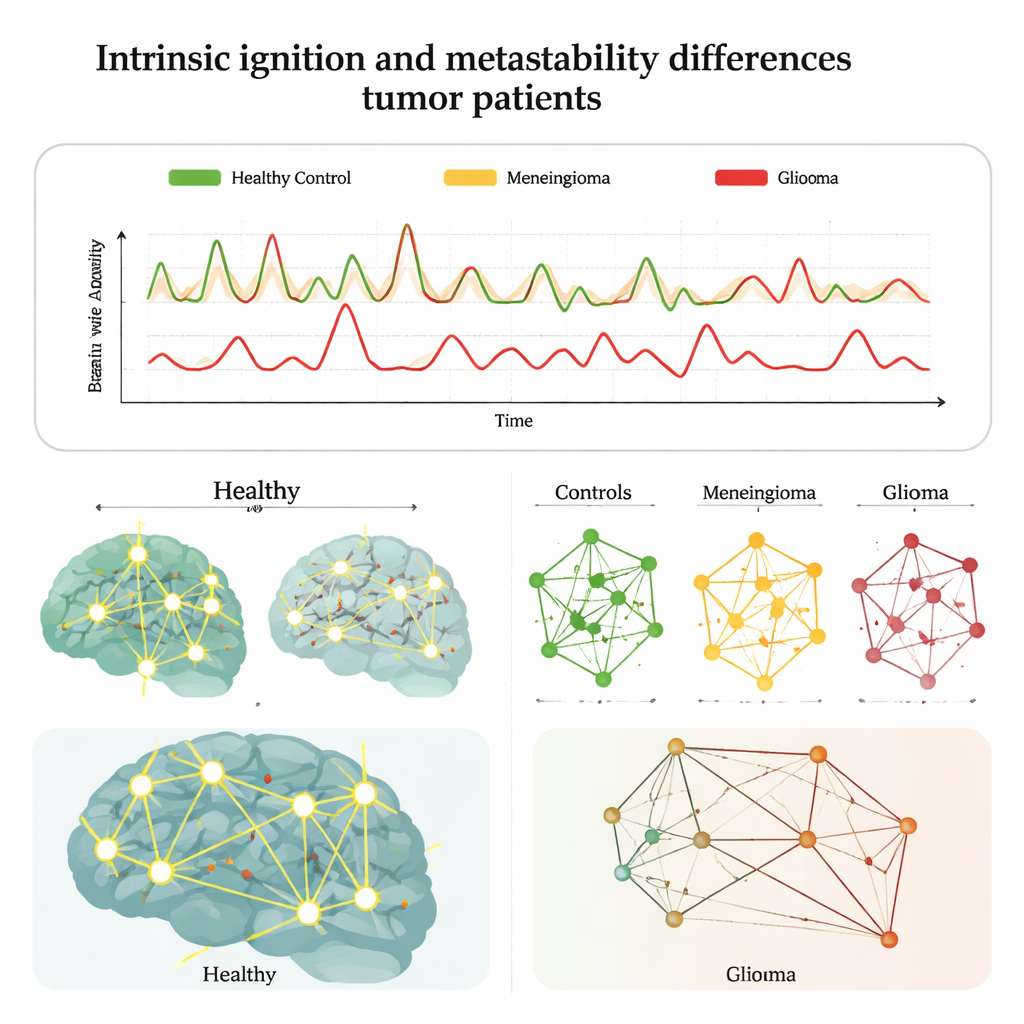
Changemens réseau cachés dans des systèmes cérébraux clés
Les chercheurs se sont ensuite concentrés sur des réseaux au repos bien connus, tels que ceux impliqués dans la vision, le mouvement, l’attention et la rêverie (le réseau du mode par défaut). Dans les cerveaux sains, la métastabilité était fortement coordonnée entre ces réseaux, et l’ignition et la métastabilité avaient tendance à augmenter et diminuer ensemble. Les patients atteints de méningiome montraient seulement un affaiblissement léger de ces relations. Les patients atteints de gliome, en revanche, présentaient des schémas nettement perturbés : les corrélations entre réseaux étaient fracturées, et le couplage habituel entre la force d’ignition des régions et la flexibilité de leur synchronisation était beaucoup plus faible. Fait important, lorsque l’équipe a relié ces mesures cérébrales aux performances à un test informatisé d’attention, les volontaires sains ayant une ignition plus élevée dans des réseaux clés répondaient plus rapidement. Les patients tumoraux, bien qu’ayant des scores de test globalement similaires, n’affichaient plus ce lien net cerveau‑comportement, ce qui suggère que leur cerveau s’appuyait sur des voies compensatrices moins efficaces.
Ce que cela signifie pour les patients et les soins futurs
Pris ensemble, les résultats soutiennent un message simple mais puissant pour le grand public : toutes les tumeurs cérébrales ne perturbent pas le cerveau de la même manière. Les méningiomes, en particulier les cas majoritairement bénins et à croissance lente étudiés ici, tendent à provoquer des problèmes mécaniques locaux qui ne se répercutent que progressivement sur la communication à plus large échelle. Les gliomes, en revanche, agissent plus comme une maladie des câblages du cerveau, dégradant silencieusement les schémas de communication entre des régions éloignées. L’étude montre aussi que des mesures sophistiquées de la façon dont les signaux s’enflamment et fluctuent à travers le cerveau peuvent révéler des atteintes réseau même lorsque les tests de routine semblent normaux. À l’avenir, ces « empreintes dynamiques » pourraient aider les cliniciens à suivre comment les tumeurs perturbent le flux d’information, adapter les traitements et surveiller la récupération au‑delà de ce que les seuls clichés anatomiques peuvent montrer.
Citation: Juncà, A., Escrichs, A., Martín, I. et al. Impact of meningioma and glioma on whole-brain dynamics. Sci Rep 16, 5032 (2026). https://doi.org/10.1038/s41598-026-35140-1
Mots-clés: tumeurs cérébrales, gliome, méningiome, réseaux cérébraux, IRM fonctionnelle