Clear Sky Science · fr
L’utilisation séquentielle d’articles jetables en FIV n’entraîne pas de toxicité cumulative, sauf lorsqu’un dispositif défectueux compromet toute la procédure
Pourquoi les outils de laboratoire du quotidien comptent pour la procréation
La plupart des gens associent la fécondation in vitro (FIV) aux hormones, à la ponction d’ovocytes et à la sélection des embryons. Peu réalisent que la réussite dépend aussi des dizaines d’objets plastiques — tubes, boîtes, pailles et cathéters — que touchent ovocytes, spermatozoïdes et embryons au cours du processus. Cette étude pose une question simple mais importante : lorsque tous ces outils jetables sont utilisés successivement dans un cycle de FIV normal, leurs faibles émissions chimiques s’accumulent-elles au point de nuire aux embryons, ou le danger provient-il principalement d’un petit nombre d’articles défectueux rarement détectés ?
La chimie cachée autour des embryons en FIV
La FIV moderne vise à reproduire au mieux le milieu corporel humain, en contrôlant la température, l’acidité et le taux d’oxygène pour que les embryons puissent se développer en sécurité. Pourtant chaque étape repose sur des consommables plastiques susceptibles de libérer de très faibles quantités de composés dans le milieu environnant. Ces substances peuvent provenir du plastique lui‑même, d’additifs améliorant la souplesse ou la transparence, ou de résidus laissés par la fabrication et la stérilisation. Des travaux antérieurs ont montré que certaines combinaisons d’outils utilisées ensemble peuvent réduire la qualité du sperme, ce qui soulève la crainte que les embryons — peut‑être encore plus fragiles — ne subissent aussi une accumulation de contaminants au cours d’une procédure complète de FIV.
Soumettre les dispositifs de FIV à un test de sécurité sur souris
Pour explorer cette question, les chercheurs ont reconstitué dix « parcours » typiques de FIV, depuis la collecte et la préparation du sperme jusqu’à la fécondation, la culture embryonnaire, la congélation, la décongélation et le transfert. Chaque parcours utilisait de 7 à 25 articles jetables différents, dans le même ordre et aux mêmes durées et températures qu’en clinique. Plutôt que d’exposer des embryons humains, ils ont fait circuler du milieu de culture à travers les dispositifs, puis ont utilisé ce milieu pour cultiver des embryons de souris dans un test de sécurité standard appelé Mouse Embryo Assay. Des ovocytes fécondés de souris frais ont été suivis pendant cinq jours, en vérifiant s’ils se divisaient normalement, s’ils atteignaient le stade blastocyste (une sphère creuse de cellules prête à s’implanter) et le nombre de cellules par blastocyste — une mesure sensible de la santé embryonnaire.
Quand un seul mauvais dispositif gâche toute la chaîne
La plupart des combinaisons de dispositifs se sont montrées inoffensives : les embryons cultivés dans des milieux exposés à huit des dix parcours se sont développés aussi bien que dans des milieux témoins propres. Toutefois, deux combinaisons se sont nettement distinguées. L’une incluait des pailles de congélation du sperme à haute sécurité, et l’autre portait sur le transfert embryonnaire avec un modèle de cathéter spécifique. Dans ces deux cas, moins d’embryons ont atteint le stade blastocyste avancé et ceux qui l’ont fait présentaient moins de cellules, signe de stress ou de dommages. Pour identifier le coupable, l’équipe a retesté chaque composant isolément et par lots répétés. Les mêmes types de paille et de cathéter ont systématiquement montré de la toxicité, surtout lorsqu’ils étaient utilisés dans des conditions routinières — humidification du bouchon de coton de la paille ou préchauffage du cathéter — étapes susceptibles d’augmenter la libération de composés volatils ou de substances ressemblant à des hormones provenant des matériaux.
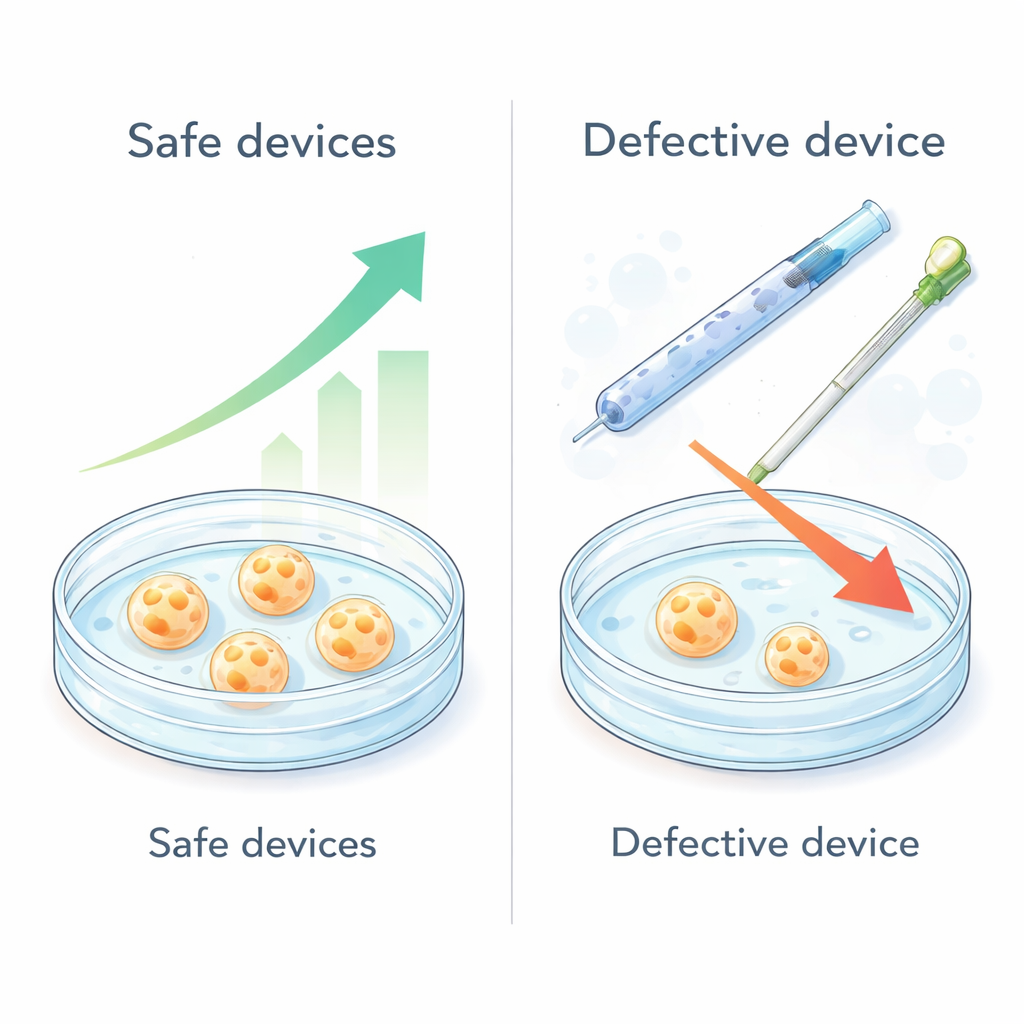
Pourquoi les labels de sécurité ne suffisent pas
Fait frappant : les pailles et cathéters problématiques avaient déjà passé les contrôles internes des fabricants et portaient les marquages réglementaires requis. Le décalage semble provenir de la manière dont le test standard sur souris est exécuté. Les entreprises peuvent utiliser des souches de souris, des conditions de culture ou des critères d’évaluation différents, certains étant moins sensibles aux toxicités subtiles. L’étude actuelle a utilisé une approche plus exigeante, incluant des comptages détaillés des cellules des blastocystes, et a mis en évidence des « faux négatifs » passés inaperçus. Les auteurs rappellent aussi que les plastiques peuvent libérer des mélanges complexes — composés organiques volatils et bisphénols notamment — qui peuvent être nocifs même à faibles concentrations, en particulier pour des embryons précoces dont le développement et la santé à long terme peuvent être influencés par de minimes modifications épigénétiques.
Ce que cela signifie pour les patients et les cliniques
Pour les personnes en parcours de FIV, la bonne nouvelle est que l’usage successif de nombreux dispositifs jetables n’entraîne pas automatiquement un environnement toxique. Le risque survient lorsqu’un seul article défectueux ou insuffisamment testé est introduit : il peut alors compromettre toute la procédure. Pour les cliniques et les autorités, le message est plus pressant : il ne faut pas s’en remettre uniquement aux certificats des fabricants. Chaque laboratoire devrait vérifier les nouveaux lots d’articles critiques avec des tests sensibles basés sur les embryons, et les autorités devraient promouvoir des protocoles d’essai harmonisés et plus stricts. En renforçant le contrôle qualité des outils « invisibles » de la FIV, on peut mieux protéger les embryons, réduire les échecs de cycle liés à une toxicité cachée et offrir aux patients une voie vers la parentalité plus sûre et plus fiable.
Citation: Delaroche, L., Besnard, L., Bazin, F. et al. The sequential use of IVF disposable devices doesn’t cause cumulative toxicity unless a defective device compromises the entire procedure. Sci Rep 16, 5491 (2026). https://doi.org/10.1038/s41598-026-35128-x
Mots-clés: Sécurité FIV, Embryotoxicité, Plastiques de laboratoire, Test sur embryons de souris, Dispositifs médicaux jetables