Clear Sky Science · fr
La phosphatase à double spécificité 6 interfère avec l’activité répressive de forkhead box O1 à l’égard de CYP4A11, qui médie l’accumulation lipidique dans le foie
Pourquoi la graisse dans le foie importe
Trop de graisse dans le foie, souvent appelée stéatose hépatique, devient de plus en plus fréquente avec les régimes modernes riches en sucre et en graisses. Si beaucoup de personnes connaissent le cholestérol ou la glycémie, peu savent que de petits commutateurs moléculaires à l’intérieur des cellules hépatiques contribuent à décider si les lipides sont brûlés ou stockés. Cette étude examine trois de ces commutateurs — des protéines nommées DUSP6, FOXO1 et CYP4A11 — et révèle comment leur lutte peut pousser les cellules hépatiques à accumuler un excès de graisse. Comprendre ce système de contrôle caché pourrait ouvrir la voie à de nouveaux traitements contre la stéatose hépatique et les troubles métaboliques associés.
Un contrôleur de trafic caché à l’intérieur des cellules hépatiques
Les chercheurs se sont concentrés sur une protéine appelée DUSP6, connue surtout pour éteindre une voie de signalisation cellulaire appelée voie ERK. Des travaux antérieurs ont montré que des souris dépourvues de DUSP6 résistaient étonnamment bien à la stéatose induite par l’alimentation, et leurs foies présentaient des niveaux plus faibles d’enzymes CYP4A, impliquées dans le traitement des lipides. Ici, l’équipe s’est intéressée à ce que fait DUSP6 dans des cellules d’origine humaine et comment elle pourrait affecter une version humaine de ces enzymes, CYP4A11. Ils ont utilisé deux lignées cellulaires de carcinome hépatique standard, HepG2 et HuH‑7, comme modèles de cellules hépatiques humaines et les ont exposées à un mélange d’acides gras (acide palmitique et oléique) pour reproduire un environnement malsain, riche en graisses. 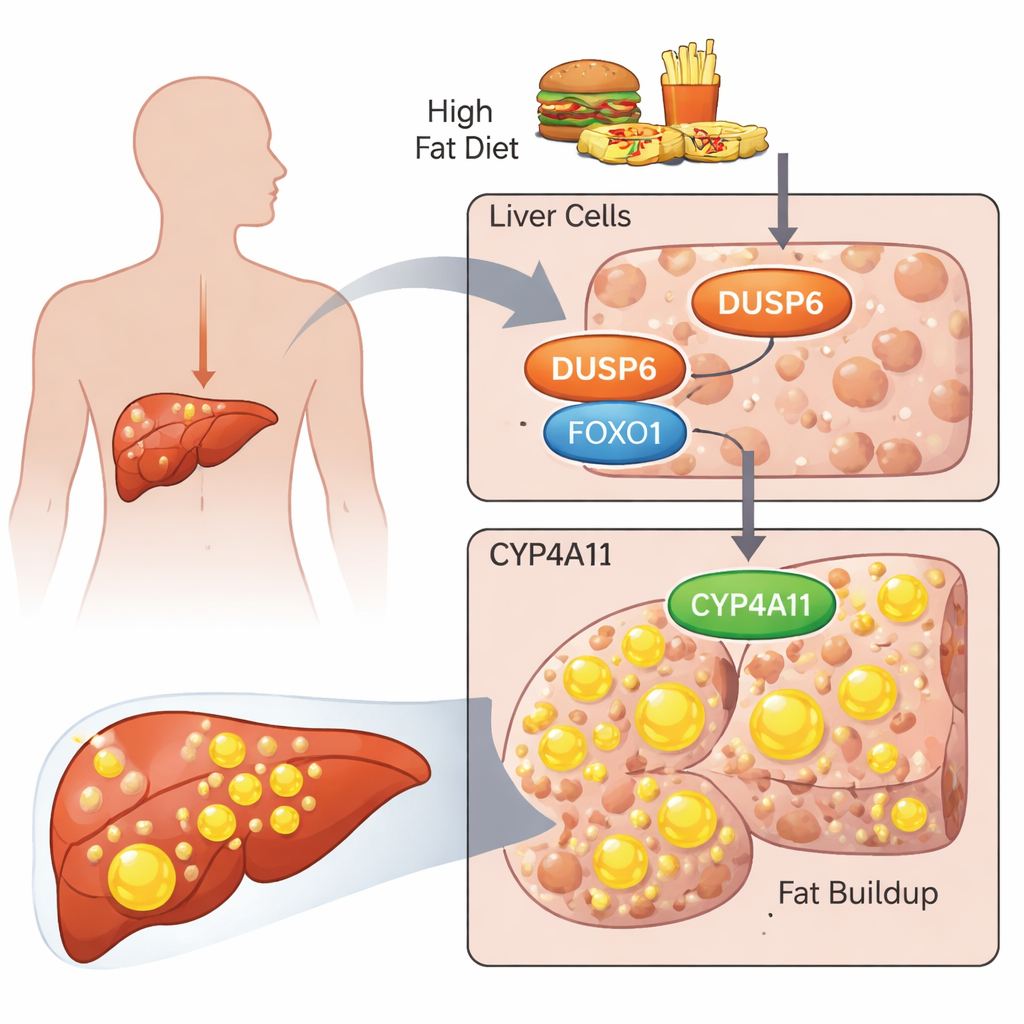
Des acides gras à une cellule remplie de lipides
Lorsque les cellules ont été mises au défi par ces acides gras, elles ont accumulé de manière visible des gouttelettes lipidiques, que les scientifiques ont colorées et quantifiées. En parallèle, les niveaux de DUSP6 et de CYP4A11 ont augmenté, ainsi que les formes activées de deux protéines de signalisation majeures, AKT et FOXO1. L’inhibition de DUSP6 par des ARN ciblés a inversé ce schéma : les cellules stockaient moins de lipides, les niveaux de CYP4A11 diminuaient, mais ERK, AKT et FOXO1 activés augmentaient. Bloquer uniquement la voie ERK aggravait en fait l’accumulation lipidique, alors que bloquer uniquement AKT la réduisait. Lorsque ERK et AKT étaient inhibés simultanément, l’accumulation de lipides chutait et les niveaux de CYP4A11 déclinaient. Ces expériences ont lié étroitement CYP4A11 à l’importance de l’accumulation lipidique et suggèrent que l’activité d’AKT est particulièrement déterminante pour favoriser le stockage des graisses.
Un frein sur les gènes favorisant les graisses
Un autre acteur clé, FOXO1, est un facteur de transcription — une protéine qui peut entrer dans le noyau cellulaire et activer ou réprimer des gènes. FOXO1 est connu pour agir comme un frein sur plusieurs membres de la même famille d’enzymes que CYP4A11. L’équipe a constaté que réduire les niveaux de FOXO1 poussait les cellules à accumuler davantage de lipides et augmentait CYP4A11, tandis que l’augmentation directe de CYP4A11 rendait les cellules encore plus grasses. En revanche, forcer la surproduction de FOXO1 réduisait à la fois CYP4A11 et l’accumulation lipidique. Un médicament bloquant l’activité de CYP4A11 (HET0016) a réduit le surplus de lipides induit par la baisse de FOXO1, soutenant l’idée que CYP4A11 n’est pas un simple spectateur mais un moteur de l’accumulation lipidique. Des tests chimiques ont montré que HET0016 réduisait le 20‑HETE, un produit fabriqué par CYP4A11 lié au stress oxydatif et à l’inflammation, reliant ainsi davantage cette voie aux lésions hépatiques.
Comment DUSP6 désamorce le frein
Pour comprendre comment FOXO1 contrôle CYP4A11, les scientifiques ont examiné la région d’ADN en amont du gène CYP4A11 et identifié des séquences où FOXO1 peut se lier. À l’aide d’un essai d’immunoprécipitation de la chromatine, ils ont montré que FOXO1 — en particulier sous sa forme non phosphorylée — se lie directement au promoteur de CYP4A11, cohérent avec un rôle répressif sur ce gène. Des expériences de co‑immunoprécipitation ont révélé que DUSP6 interagit physiquement avec FOXO1 mais pas avec sa forme phosphorylée. Des études de fractionnement et de microscopie ont montré que DUSP6 se situe dans le cytoplasme cellulaire et, lorsqu’elle est présente, retient davantage FOXO1 hors du noyau. Lorsque DUSP6 était réduit, plus de FOXO1 se déplaçait vers le noyau, où il pouvait se lier à l’ADN et réprimer CYP4A11. En pratique, DUSP6 agit comme une ancre, séquestrant FOXO1 dans le cytoplasme et l’empêchant d’exercer son rôle de frein sur CYP4A11. 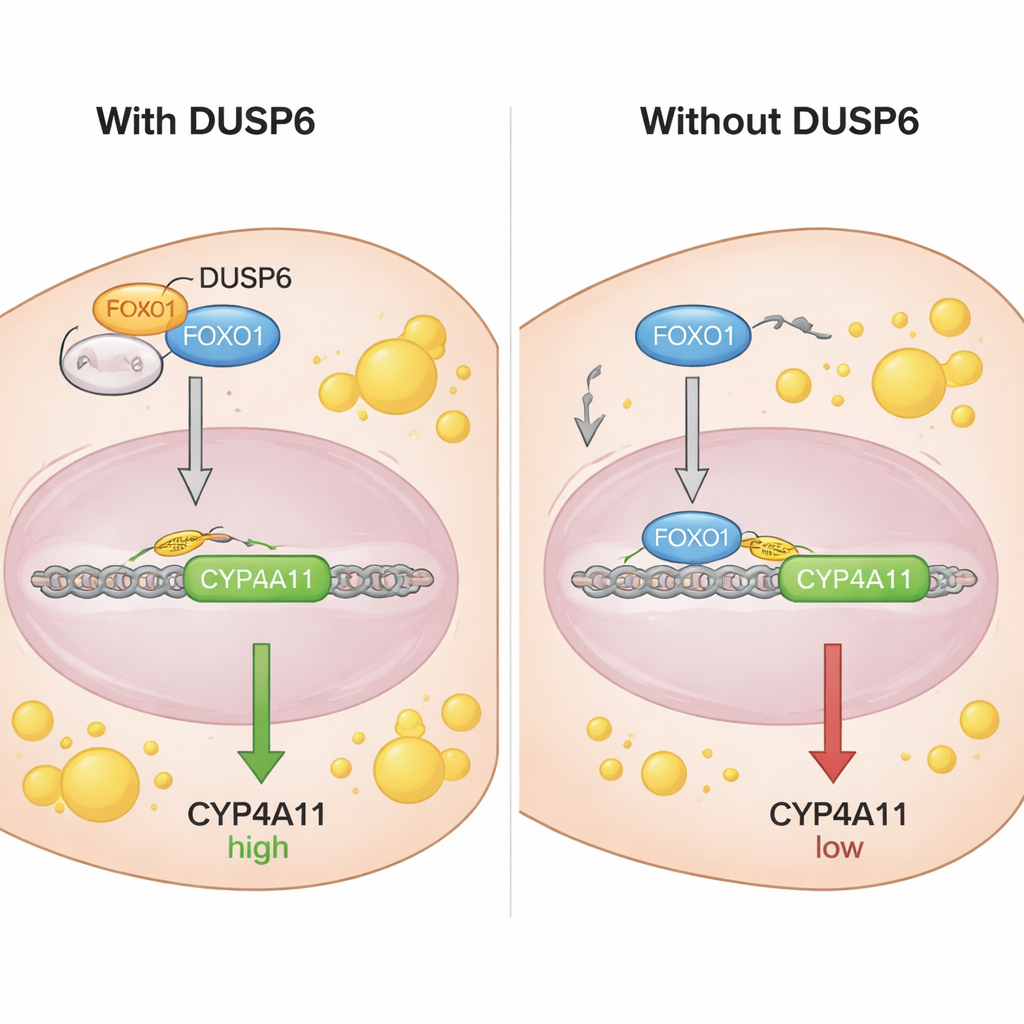
Ce que cela signifie pour la stéatose hépatique et au‑delà
En termes simples, ce travail cartographie une chaîne d’événements à l’intérieur des cellules hépatiques : DUSP6 retient FOXO1 dans le cytoplasme, ce qui affaiblit la capacité de FOXO1 à réprimer le gène CYP4A11. Avec FOXO1 neutralisé, CYP4A11 devient plus actif, contribuant à pousser la cellule vers un stockage lipidique accru et la production de molécules comme le 20‑HETE, susceptibles de favoriser le stress oxydatif et l’inflammation. Bien que ces observations proviennent de cellules dérivées de tumeurs hépatiques en culture et non de tissus hépatiques humains sains, elles mettent en lumière DUSP6 et CYP4A11 comme de nouvelles cibles potentielles pour traiter la stéatose hépatique liée à des dysfonctions métaboliques. Des thérapies visant à réduire l’activité de DUSP6 ou à atténuer les effets de CYP4A11 pourraient, en théorie, restaurer la fonction de freinage de FOXO1 et contribuer à limiter l’accumulation de graisse dans le foie.
Citation: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Mots-clés: stéatose hépatique, DUSP6, FOXO1, CYP4A11, métabolisme hépatique