Clear Sky Science · fr
Exploration de DrugBank par apprentissage automatique révèle de nouveaux candidats pour l’inhibition de BCL-2
Pourquoi découvrir des médicaments anticancéreux plus intelligents importe
Les cellules cancéreuses refusent souvent de mourir quand elles le devraient. De nombreux tumeurs survivent en surexprimant une famille de protéines « garde du corps » appelées BCL-2 qui bloquent le programme de suicide intrinsèque de la cellule. Des médicaments ciblant BCL-2 existent déjà, mais ils peuvent provoquer des effets indésirables et ne fonctionnent pas pour tous les patients. Cette étude examine comment l’apprentissage automatique moderne peut trier des milliers de médicaments existants pour identifier de nouveaux candidats plus sûrs susceptibles de neutraliser BCL-2 et d’aider les cellules cancéreuses à s’autodétruire.
Comment les cellules choisissent entre la vie et la mort
Les tissus sains éliminent en permanence les cellules endommagées ou inutiles via un processus contrôlé d’autodestruction appelé apoptose, ou mort cellulaire programmée. Un groupe de protéines nommé famille BCL-2 agit comme un interrupteur central pour cette décision. Certains membres poussent les cellules vers la survie, tandis que d’autres les poussent vers la mort. Dans de nombreux cancers, les membres promoteurs de la survie, y compris BCL-2 et son proche parent BCL-XL, sont produits en excès. Cette protection supplémentaire permet aux cellules cancéreuses d’ignorer les signaux de mort et de résister à la chimiothérapie. Pour cette raison, bloquer BCL-2 est devenu une stratégie attrayante en oncologie, mais les médicaments actuels ciblent souvent aussi des protéines apparentées, entraînant des effets secondaires tels que des chutes dangereuses du nombre de plaquettes.
Apprendre aux ordinateurs à reconnaître des molécules prometteuses
Plutôt que de rechercher de nouveaux composés à partir de zéro, les chercheurs se sont tournés vers des bases de données de molécules déjà étudiées ou utilisées comme médicaments. Ils ont commencé par une vaste ressource publique appelée ChEMBL, qui contient des mesures expérimentales de l’affinité de différentes substances pour BCL-2. Après un nettoyage minutieux de ces données — suppression des doublons, des mesures incertaines et des molécules trop grosses ou atypiques — ils ont obtenu 601 composés bien caractérisés. Chaque molécule a été traduite en une sorte d’empreinte numérique capturant ses caractéristiques structurales. Ces empreintes ont servi à entraîner et comparer sept modèles d’apprentissage automatique différents pour décider si une nouvelle molécule est susceptible d’être un fort bloqueur de BCL-2 ou essentiellement inactive. 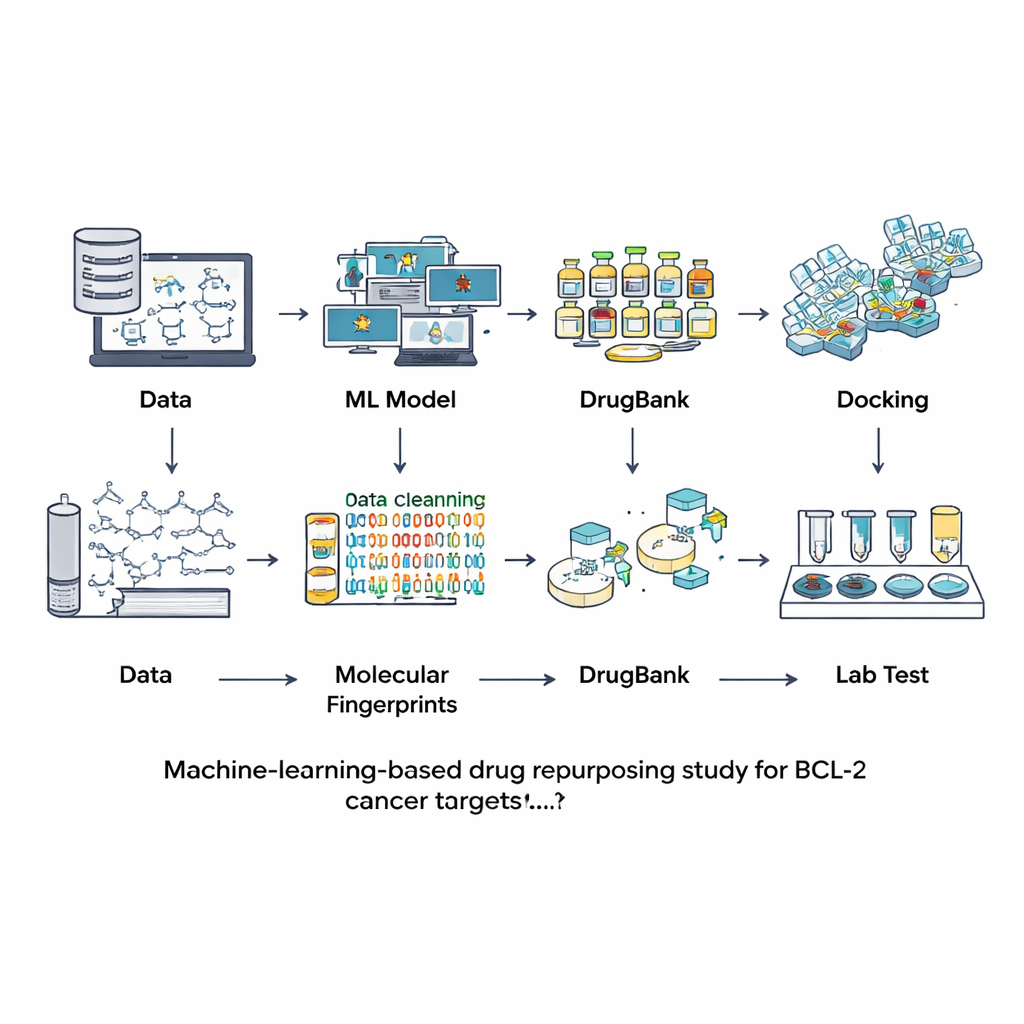
Choisir le meilleur modèle et scanner une bibliothèque de médicaments
L’équipe a évalué les modèles en utilisant un jeu de test distinct qui n’avait pas été vu pendant l’entraînement, en vérifiant non seulement la fréquence des prédictions correctes, mais aussi la capacité à distinguer les actifs des inactifs et l’équilibre des prédictions. Un modèle appelé LightGBM — une méthode moderne de boosting basée sur des arbres — a obtenu les meilleures performances sur la plupart des métriques, y compris la précision globale et la capacité à fournir des probabilités fiables. Avec ce modèle optimisé, les chercheurs se sont tournés vers DrugBank, une collection organisée de plus de 12 000 médicaments approuvés, expérimentaux et retirés. Après avoir calculé le même type d’empreintes, ils ont demandé à LightGBM quelles molécules semblaient être des inhibiteurs potentiels de BCL-2. Seulement neuf composés ont obtenu des scores élevés, soit à peu près le dixième de un pour cent de l’ensemble de la bibliothèque, montrant que le criblage virtuel était très sélectif. Quatre des neuf étaient déjà connus comme inhibiteurs de BCL-2, ce qui a rassuré l’équipe sur la validité de l’approche.
Des « hits » informatiques aux interactions moléculaires
Parmi les molécules restantes à score élevé, les chercheurs se sont concentrés sur trois qui n’avaient pas été précédemment liées à BCL-2 : Dersalazine, Opelconazole et Zongertinib. Pour vérifier si ces candidats pouvaient raisonnablement s’insérer dans la poche de liaison de BCL-2, ils ont utilisé le « docking » informatique, une technique qui prédit comment une petite molécule peut se loger dans la surface de la protéine. Les simulations suggéraient qu’Opelconazole et Zongertinib, en particulier, forment des réseaux de contacts favorables avec les mêmes acides aminés clés qui interagissent avec un médicament de référence bien étudié, ABT-737. Leurs forces de liaison prédites étaient proches de celles d’inhibiteurs établis, laissant entendre que le modèle d’apprentissage automatique avait effectivement découvert des molécules capables de neutraliser BCL-2. 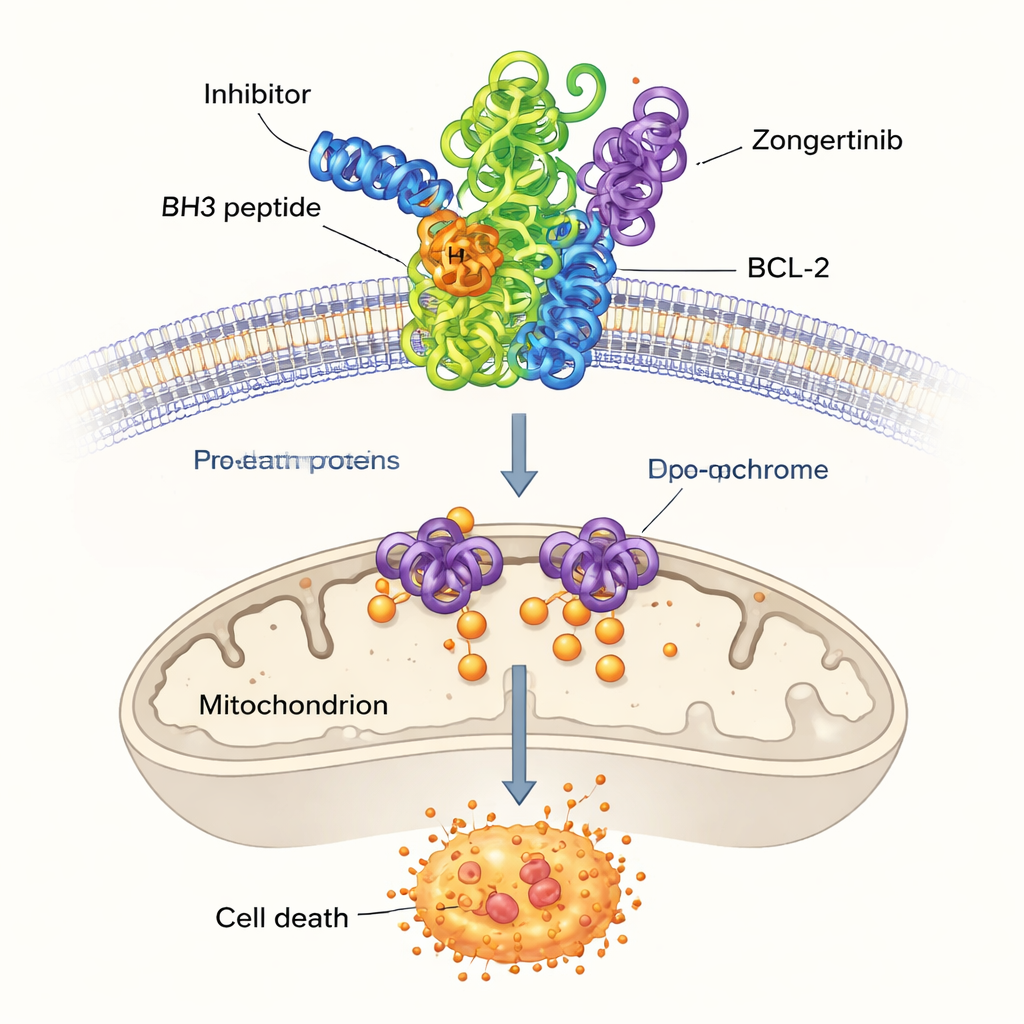
Mettre les prédictions à l’épreuve en laboratoire
Les indices computationnels ne sont utiles que s’ils se vérifient en conditions réelles. L’équipe a donc testé les trois candidats dans un essai biochimique qui mesure la capacité d’un composé à empêcher BCL-2 de se lier à l’un de ses partenaires naturels. À différentes concentrations, Dersalazine a montré peu d’effet. Opelconazole et Zongertinib, en revanche, ont tous deux réduit l’activité de BCL-2 à fortes doses, Opelconazole presque supprimant totalement le signal. Bien que ces concentrations soient supérieures à ce qui serait idéal pour un médicament prêt pour la clinique, elles démontrent que les candidats interagissent réellement avec BCL-2 et valident la chaîne de découverte globale.
Ce que cela signifie pour les thérapies anticancéreuses futures
Pour un non-spécialiste, le message clé est que les chercheurs ont réussi à entraîner un système informatique à reconnaître l’apparence d’une molécule bloquant BCL-2, puis l’ont utilisé pour exploiter une grande bibliothèque de médicaments et de composés apparentés. L’approche a redécouvert des médicaments connus ciblant BCL-2 et mis en avant de nouveaux candidats, dont deux ont montré une activité inhibitrice réelle dans des tests en laboratoire. Bien qu’il reste beaucoup à faire — améliorer la puissance, évaluer la sécurité et tester en cellules et chez l’animal — cette étude montre comment l’apprentissage automatique et une curation intelligente des données peuvent accélérer la recherche de meilleurs médicaments anticancéreux en recyclant et en réévaluant des composés déjà connus.
Citation: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Mots-clés: Inhibiteurs de BCL-2, apprentissage automatique, repositionnement de médicaments, apoptose, thérapie contre le cancer