Clear Sky Science · fr
Structure cristalline de la cystatine B d’Echinococcus multilocularis révèle une nouveauté chez les stefines classiques
Pourquoi l’arme secrète d’un parasite hépatique compte
L’échinococcose alvéolaire est un nom imposant pour une petite infection par un ténia qui se comporte beaucoup comme un cancer lent du foie. Elle est souvent mortelle ; les traitements actuels sont peu efficaces et peuvent entraîner des effets secondaires graves. Cette étude se concentre sur une molécule particulière produite par le parasite, une protéine appelée EmCystatin‑B, pour comprendre comment elle pourrait aider le ver à échapper aux défenses de l’hôte — et comment, à terme, elle pourrait devenir une cible pour de nouveaux traitements.
Un ténia dangereux qui croît comme une tumeur
La maladie est causée par le stade larvaire du ténia Echinococcus multilocularis. L’infection survient par ingestion accidentelle d’œufs du parasite, par exemple dans des aliments ou de l’eau contaminés. Une fois dans l’organisme, les larves s’implantent principalement dans le foie et se développent en nombreuses petites vésicules remplies de liquide qui infiltrent les tissus voisins, se propagent vers des organes proches comme la rate, et peuvent parfois atteindre des sites distants comme les poumons ou le cerveau. En l’absence de traitement efficace, plus de 9 patients sur 10 meurent dans les 10 à 15 ans. La chirurgie associée à des antiparasitaires au long cours reste pour l’instant la meilleure option, mais le diagnostic précoce est difficile et les médicaments ne permettent pas de guérir de manière fiable. D’où l’importance de comprendre, au niveau moléculaire, comment le parasite interagit avec le corps humain.
Une protéine parasitaire qui désarme des enzymes de découpe
De nombreux animaux, y compris les humains, produisent une famille de protéines appelées cystatines qui agissent comme des verrous de sécurité sur de puissantes enzymes digestives connues sous le nom de protéases à cystéine. Ces enzymes peuvent cliver d’autres protéines et sont importantes pour des processus tels que l’élimination des composants cellulaires usés et l’activation de réponses immunitaires. Les parasites ont évolué pour produire leurs propres protéines de type cystatine afin d’interférer avec les enzymes et le système immunitaire de l’hôte. Dans ce travail, les chercheurs ont identifié une protéine de type cystatine d’E. multilocularis et l’ont nommée EmCystatin‑B. Ils ont observé que le gène codant EmCystatin‑B est beaucoup plus actif dans les têtes larvaires matures du parasite (protoscolex) que dans le tissu kystique environnant, et que la protéine est présente dans le cytoplasme et le noyau des cellules du parasite, en particulier dans les cellules germinatives « souches » en division. Des tests en laboratoire ont montré qu’EmCystatin‑B peut bloquer fortement l’activité de la cathepsine B humaine, une protéase à cystéine importante pour l’immunité et le remodelage tissulaire.
Une forme familière avec un retournement inattendu
Pour voir précisément comment EmCystatin‑B est agencée, l’équipe a cristallisé la protéine purifiée et utilisé la cristallographie aux rayons X pour résoudre sa structure tridimensionnelle à résolution quasi‑atomique. Comme les autres membres de la famille des cystatines, chaque unité d’EmCystatin‑B présente une forme caractéristique : un segment hélicoïdal central soutenu par plusieurs brins aplatis en ruban, formant une calotte qui s’insère normalement dans le site actif d’une protéase. D’après sa séquence et l’absence d’un peptide signal évident pour la sécrétion, EmCystatin‑B appartient au sous‑groupe des « stefines », qui sont en général de petites protéines intracellulaires ne contenant pas de ponts disulfure stabilisants. De manière surprenante, la structure a révélé que bien que chaque unité d’EmCystatin‑B ait le repli attendu, la façon dont ces unités s’associent entre elles est inhabituelle et spécifique à l’espèce par rapport à l’équivalent humain, la cystatine B.
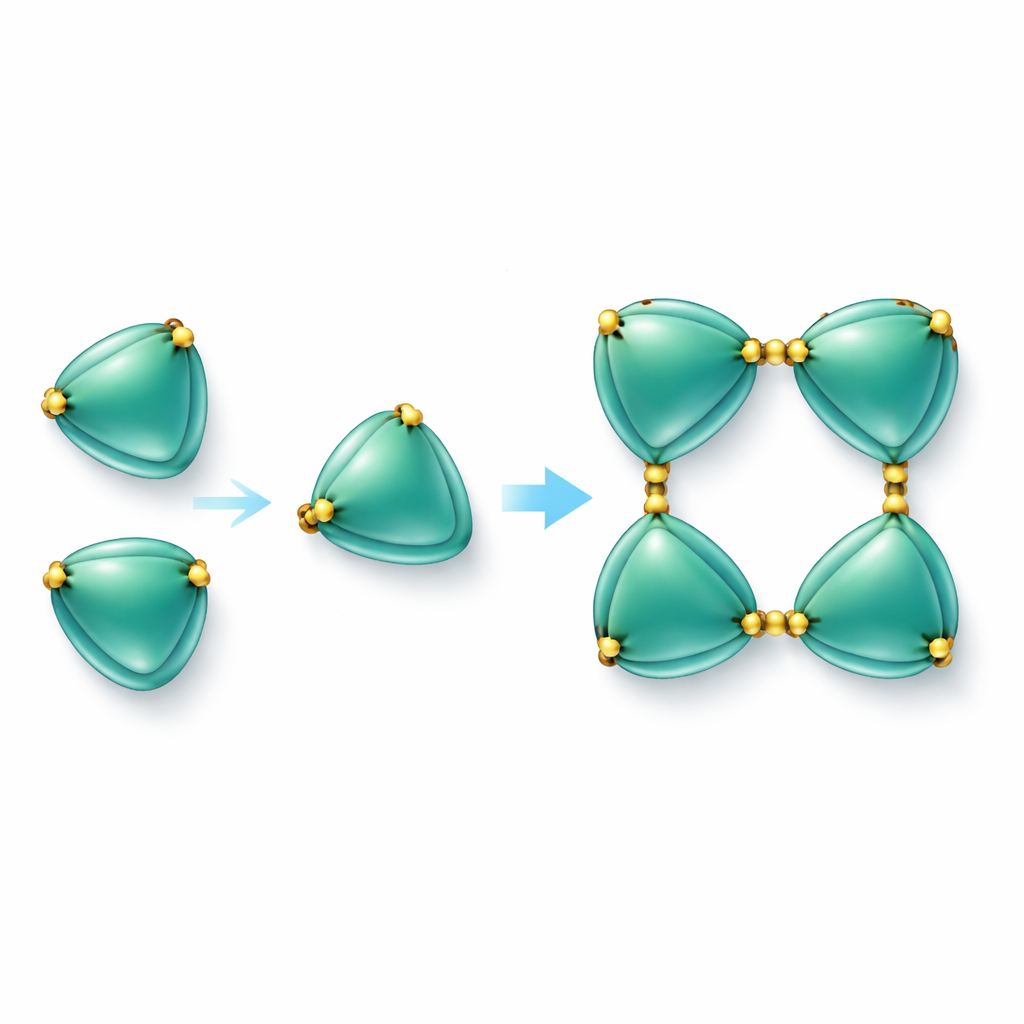
Assembler des chaînes protéiques par des liens soufrés
La découverte la plus marquante est que les molécules d’EmCystatin‑B ne circulent pas simplement comme des monomères isolés. Elles peuvent au contraire s’assembler de façon progressive pour former des dimères (paires) puis des tétramères (groupes de quatre). Deux mécanismes différents contribuent à la formation des dimères initiaux. Dans l’un, une partie d’une molécule bascule et complète la structure de sa voisine, un phénomène appelé échange de domaine. Dans l’autre, des paires de molécules sont liées par des ponts disulfure — des liaisons chimiques robustes entre acides aminés contenant du soufre (cystéines). Dans EmCystatin‑B, la cystéine en position 4 d’une molécule se lie à la cystéine en position 76 d’une molécule partenaire. Quatre de ces liaisons croisées stabilisent ensuite le tétramère. L’usage de multiples ponts disulfure inter‑moléculaires est entièrement nouveau pour les stefines classiques, qui en sont normalement dépourvues. Lorsque les chercheurs ont remplacé ces cystéines clés par un autre acide aminé, la protéine n’a plus pu s’assembler efficacement en complexes d’ordre supérieur et sa capacité à inhiber la cathepsine B a fortement diminué.
Ce que cela signifie pour la lutte contre l’infection
Pour un non‑spécialiste, le message est que le parasite a développé une version spécialement câblée d’une famille protéique courante, utilisant des « rivets » chimiques supplémentaires pour verrouiller plusieurs unités inhibitrices entre elles. Cette forme oligomérique semble importante pour désactiver une enzyme de l’hôte qui, sinon, contribuerait à contrôler l’infection. En révélant l’architecture précise d’EmCystatin‑B et ses assemblages uniques liés par des disulfures, l’étude élargit notre compréhension de la manière dont les protéines cystatines peuvent être modulées selon les espèces. À long terme, ces découvertes pourraient orienter la conception de médicaments visant soit à bloquer l’effet protecteur d’EmCystatin‑B pour affaiblir le parasite, soit à imiter ses propriétés anti‑inflammatoires pour traiter des maladies inflammatoires.
Citation: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Mots-clés: échinococcose alvéolaire, Echinococcus multilocularis, cystatine B, structure protéique, modulation immunitaire