Clear Sky Science · fr
Perturbation de l’assemblage de l’inflammasome NLRP3 via le remodelage induit par un ligand des interfaces du domaine pyrine
Pourquoi il est important d’apaiser l’inflammation incontrôlée
De nombreuses maladies chroniques — de l’arthrite et la goutte aux maladies cardiovasculaires et aux troubles neurodégénératifs — sont entretenues par un système d’alarme immunitaire intracellulaire hyperactif. Un élément clé de cette alarme, appelé inflammasome NLRP3, nous aide à combattre les infections mais peut aussi provoquer une inflammation délétère lorsqu’il se dérègle. Cette étude décrit une nouvelle petite molécule, nommée E9, qui cible une étape précoce de l’activation de NLRP3, offrant une nouvelle approche pour concevoir des médicaments qui atténuent l’inflammation nocive sans neutraliser complètement le système immunitaire.
Une alarme cellulaire aux conséquences sombres
Lorsque notre organisme détecte un danger, les cellules immunitaires assemblent l’inflammasome NLRP3, un grand complexe protéique qui fonctionne comme une alarme moléculaire. Une fois formée, cette structure active une enzyme appelée caspase‑1, qui à son tour active des messagers inflammatoires puissants, notamment les cytokines IL‑1β et IL‑18. Ces signaux sont essentiels pour lutter contre les infections et éliminer les tissus endommagés. Mais si l’inflammasome reste activé trop longtemps ou s’active au mauvais moment, il contribue à des phénomènes inflammatoires chroniques touchant les articulations, les vaisseaux sanguins, le cerveau et d’autres organes. C’est pourquoi des équipes de recherche du monde entier cherchent des moyens précis de contrôler NLRP3 sans supprimer l’immunité de façon générale.
Au‑delà des cibles médicamenteuses habituelles
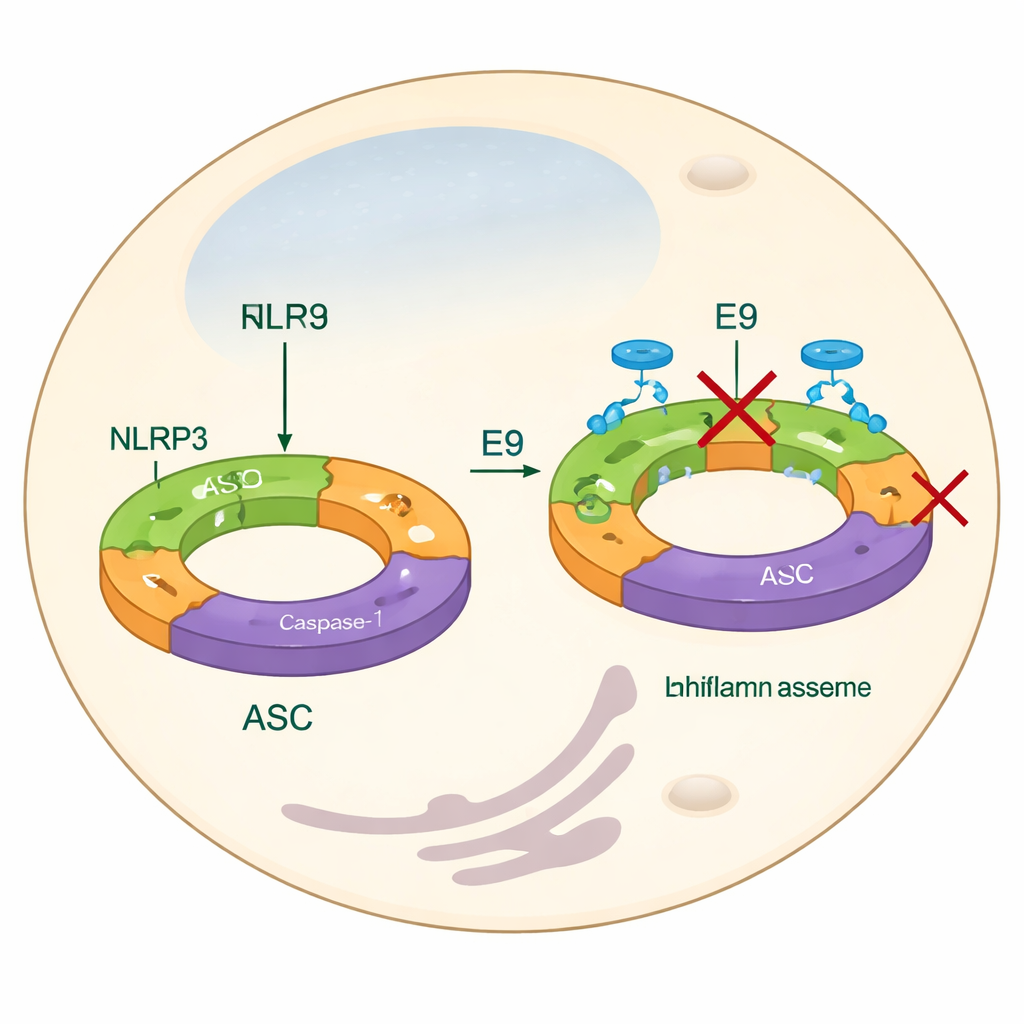
La plupart des stratégies actuelles pour maîtriser NLRP3 visent à bloquer ses produits finaux — comme l’IL‑1β — ou à interférer avec un domaine central analogue à un moteur qui utilise des molécules énergétiques telles que l’ATP. Bien que ces approches puissent être efficaces, elles peuvent manquer les étapes d’assemblage les plus précoces et n’expliquent pas complètement comment les protéines NLRP3 s’assemblent pour former une machine fonctionnelle. Dans ce travail, les auteurs se concentrent plutôt sur le domaine pyrine, une partie de NLRP3 qui aide les unités individuelles à s’assembler en longs filaments. Ces filaments recrutent ensuite une autre protéine adaptatrice, ASC, qui se regroupe en « points » lumineux à l’intérieur des cellules — une signature visuelle de l’activation de l’inflammasome. En recherchant des molécules capables d’empêcher les domaines pyrine de s’emboîter correctement, l’équipe vise à empêcher la formation de l’inflammasome dès le départ.
Trouver une molécule qui brise la chaîne
Les chercheurs ont testé une bibliothèque de 1500 petites molécules nouvellement synthétisées à l’aide d’un test ingénieux basé sur la lumière. Ils ont fusionné des fragments d’une luciférase à des domaines pyrine de NLRP3 ; lorsque deux domaines pyrine se rapprochaient, les fragments enzymatiques se réassemblaient et produisaient de la lumière. Les composés qui bloquaient le contact pyrine–pyrine entraînaient une diminution du signal lumineux. À partir de ce criblage, ils ont identifié quatre candidats prometteurs, dont un — E9 — se distinguait par son inhibition forte et constante. Des mesures complémentaires par thermophoresis microscopique ont montré que E9 se liait étroitement au domaine pyrine à des concentrations très faibles (submicromolaires), confirmant que son effet résultait d’une interaction spécifique et non d’un artefact aléatoire.
Observer l’effet à l’intérieur de cellules vivantes
Pour tester si E9 pouvait aussi agir dans un système vivant, l’équipe a utilisé des cellules ressemblant à des cellules immunitaires humaines, génétiquement modifiées pour produire une version fluorescente d’ASC. Lorsque ces cellules sont stimulées par des composants bactériens et un second déclencheur, NLRP3 s’active et les protéines ASC se regroupent en points lumineux qui peuvent être comptés au microscope. En présence d’E9, le nombre de ces points a fortement diminué, de manière comparable voire supérieure à certains bloqueurs connus de NLRP3. Cela montre que gêner les contacts entre domaines pyrine suffit à réduire l’assemblage de l’inflammasome et les étapes précoces de la mort cellulaire inflammatoire, du moins en conditions de laboratoire.
Comment E9 reconfigure l’échafaudage de l’inflammasome
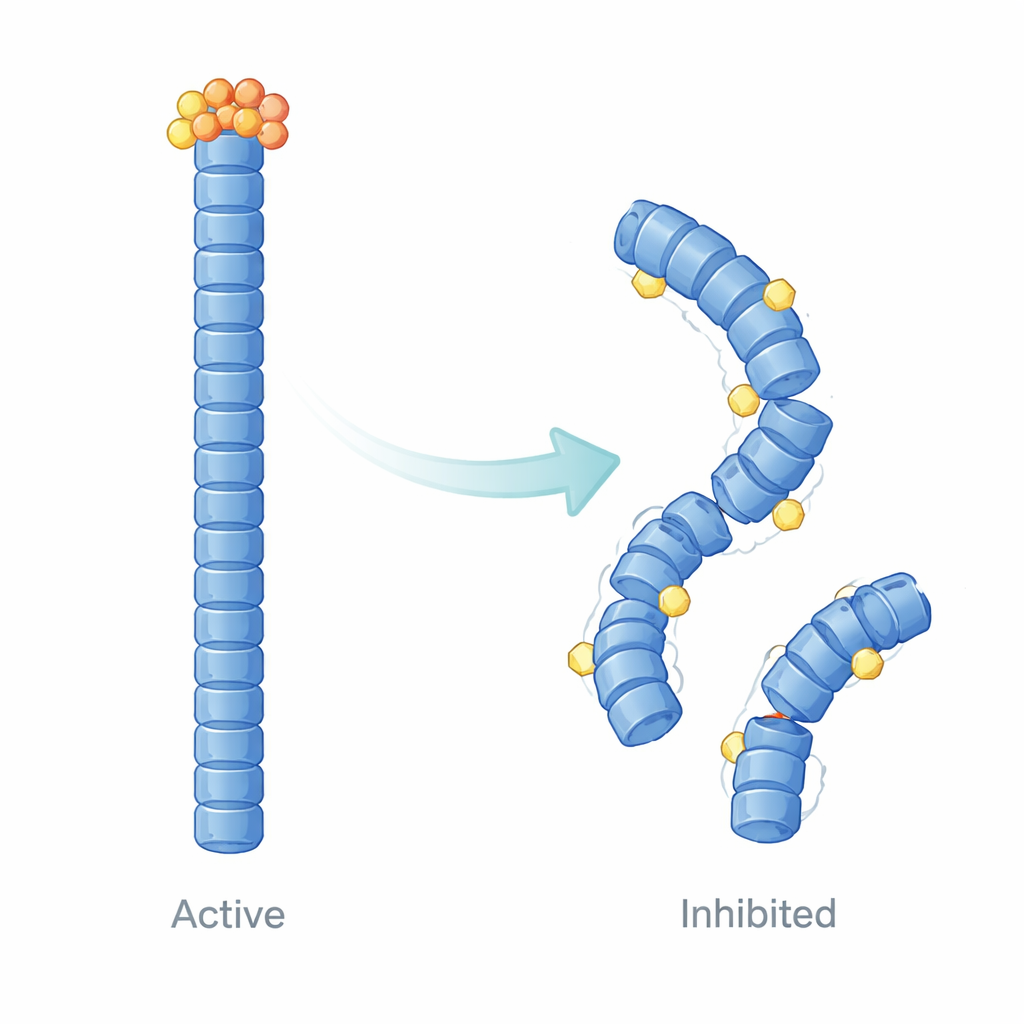
Au‑delà de la simple mesure de la liaison, les auteurs ont employé la modélisation structurale assistée par ordinateur et des simulations de dynamique moléculaire pour visualiser comment E9 modifie le comportement des filaments de NLRP3 au fil du temps. Leurs calculs suggèrent qu’E9 se loge à des surfaces de contact spécifiques où les domaines pyrine se touchent, desserrant et remodelant subtilement le filament. Plutôt que de former une structure coopérative uniformément stable, le filament devient inégal : les régions proches d’E9 deviennent plus flexibles et perdent leur alignement précis, tandis que d’autres parties se retrouvent dynamiquement isolées. Ces changements atténuent les mouvements à grande échelle et la communication serrée nécessaires au recrutement efficace d’ASC, offrant une explication physique à la réduction de la formation de points observée dans les cellules.
Ce que cela pourrait signifier pour les thérapies futures
Dans l’ensemble, les résultats positionnent E9 comme un prototype d’une nouvelle classe de médicaments ciblant l’inflammasome et agissant en perturbant les interfaces entre les éléments constitutifs de NLRP3 plutôt qu’en bloquant son utilisation d’énergie ou ses produits finaux. Bien que le travail actuel soit limité à des essais en éprouvette, des simulations informatiques et des cellules en culture — et que des études supplémentaires chez l’animal et chez l’homme soient nécessaires — il démontre que des petites molécules bien conçues peuvent remodeler l’échafaudage de l’inflammasome lui‑même. Pour les patients souffrant de maladies alimentées par une inflammation incontrôlée, de tels médicaments ciblant les interfaces pourraient un jour offrir un contrôle plus précis, réduisant l’activation immunitaire nuisible tout en préservant en grande partie les défenses essentielles.»
Citation: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Mots-clés: inflammasome NLRP3, domaine pyrine, inhibiteur de petite molécule, immunité innée, pyroptose