Clear Sky Science · fr
TTF2 comme biomarqueur potentiel et cible d’immunothérapie dans le diagnostic et le pronostic du gliome
Pourquoi cette étude sur le cancer du cerveau est importante
Les tumeurs cérébrales appelées gliomes font partie des cancers les plus mortels, la plupart des patients ne vivant que quelques années après le diagnostic. Les cliniciens ont un besoin urgent de meilleurs outils pour prédire le comportement de la maladie et pour trouver de nouvelles cibles thérapeutiques, en particulier pour les traitements immunitaires modernes. Cette étude se concentre sur une molécule peu connue, TTF2, et pose une question simple aux conséquences importantes : les niveaux de TTF2 dans les tumeurs cérébrales peuvent‑ils aider à diagnostiquer le gliome plus précisément, à prévoir la survie et même à orienter de futures immunothérapies ?
Un nouveau signal caché dans les gènes tumoraux
Le gliome n’est pas une maladie unique mais un groupe hétérogène de tumeurs cérébrales qui diffèrent par leur vitesse de croissance et leur réponse aux traitements. Les outils actuels, comme l’examen microscopique et quelques marqueurs génétiques, n’expliquent pas entièrement pourquoi certains patients vont bien tandis que d’autres déclinent rapidement. Les chercheurs se sont tournés vers de larges bases de données publiques sur les gènes du cancer, provenant des États‑Unis et de Chine, pour chercher des indices moléculaires supplémentaires. Ils ont focalisé leur attention sur TTF2, une protéine impliquée dans la répression de l’activité génique, liée à plusieurs autres cancers mais peu étudiée jusqu’ici dans le gliome.
TTF2 élevé, risque accru
En comparant des milliers d’échantillons, l’équipe a constaté que les niveaux de TTF2 sont beaucoup plus élevés dans les tissus de gliome que dans le tissu cérébral normal. Au sein des gliomes, les tumeurs présentant les niveaux les plus élevés de TTF2 avaient tendance à être plus avancées, à appartenir à des sous‑types plus agressifs et à survenir chez des patients plus âgés. Lors du suivi des issues cliniques, un schéma net est apparu : les personnes dont les tumeurs contenaient davantage de TTF2 avaient généralement une survie globale plus courte et une progression de la maladie plus fréquente. Même après avoir pris en compte des marqueurs puissants existants tels que le grade tumoral, le statut de mutation IDH et une altération chromosomique appelée codeletion 1p/19q, TTF2 restait un signe d’alerte indépendant. Le groupe a construit un diagramme de prédiction combinant TTF2 et ces facteurs standards, qui correspondait étroitement à la survie réelle à un, trois et cinq ans dans deux jeux de données patients séparés.
Indices provenant du voisinage tumoral
Pour comprendre pourquoi TTF2 pourrait être lié à de mauvais résultats, les chercheurs ont examiné quels autres gènes augmentent ou diminuent en parallèle et quels processus biologiques ces ensembles de gènes représentent. Les tumeurs à TTF2 élevé montraient une activité renforcée dans des voies liées au signalement immunitaire, à la production d’anticorps et à la communication intercellulaire, ainsi que dans des voies cancéreuses bien connues comme PI3K–AKT. À l’aide d’outils informatiques inférant la composition des cellules immunitaires à partir des profils géniques, ils ont ensuite analysé le microenvironnement tumoral. Les gliomes riches en TTF2 étaient également riches en certaines cellules immunitaires — lymphocytes T auxiliaires de type Th2, macrophages et neutrophiles — souvent associés à une réponse anti‑tumorale « assourdie » ou supprimée, et présentaient moins de cellules dendritiques plasmacytoïdes, qui peuvent contribuer à déclencher une immunité plus forte.
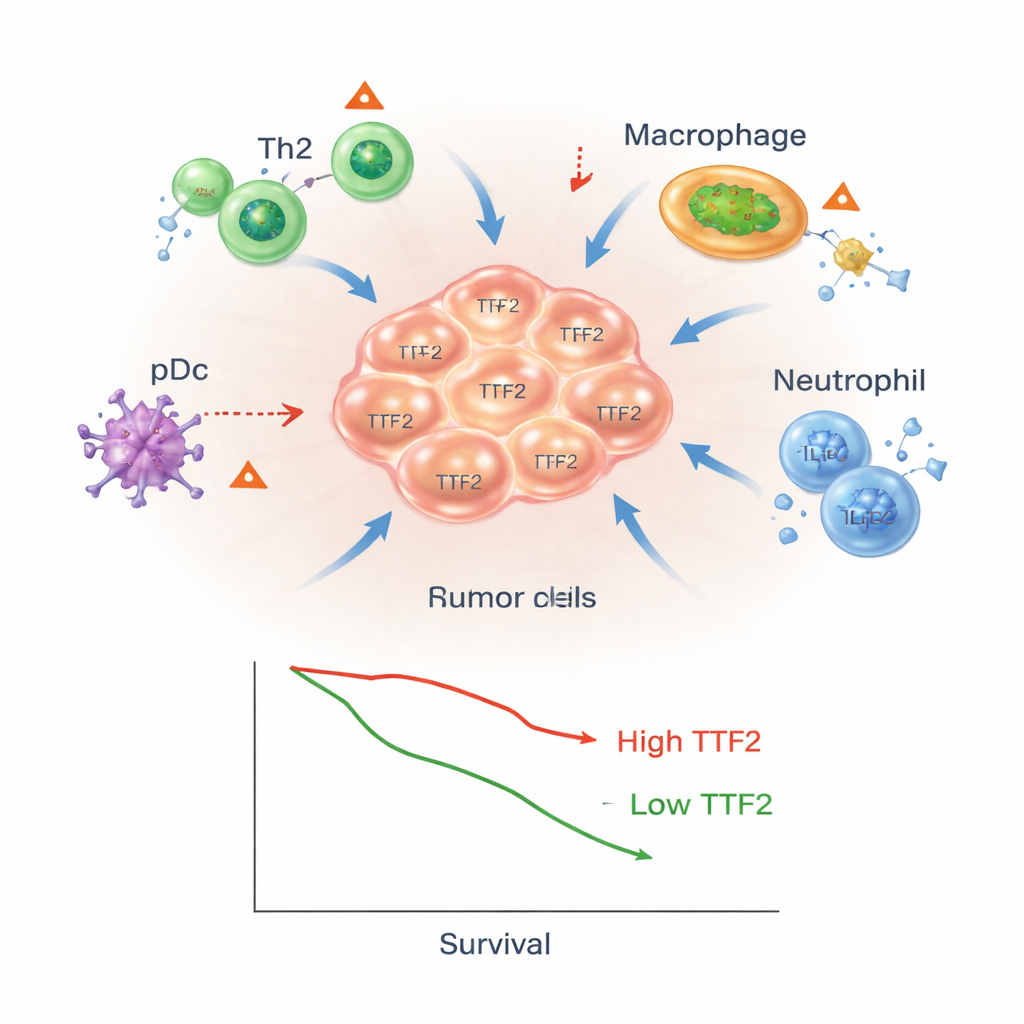
Comment TTF2 pourrait aider les tumeurs à se cacher
Ces résultats suggèrent que TTF2 ne se contente pas de marquer les tumeurs dangereuses ; il pourrait activement contribuer à créer un bouclier protecteur autour d’elles. Les auteurs proposent qu’en influençant la façon dont les gènes sont éteints, TTF2 pourrait modifier les niveaux de messagers immunitaires et de chimiokines clés — des molécules qui attirent ou repoussent les cellules immunitaires. Cela pourrait, à son tour, orienter les cellules T vers un état dominé par Th2, moins efficace pour tuer les cellules cancéreuses, et favoriser l’accumulation de macrophages et de neutrophiles soutenant la tumeur. Bien que ces idées proviennent d’analyses de données plutôt que de manipulations expérimentales directes de TTF2, elles offrent un modèle testable expliquant comment cette molécule pourrait promouvoir à la fois la croissance tumorale et l’échappement immunitaire.
Ce que cela signifie pour les patients
L’étude conclut que TTF2 est fortement surexprimé dans les gliomes et que des niveaux plus élevés sont de façon fiable associés à une survie réduite et à des caractéristiques de maladie plus agressives. Pour les patients, cela ouvre deux pistes encourageantes. D’abord, mesurer TTF2 dans les échantillons tumoraux pourrait aider les médecins à affiner le diagnostic et à personnaliser les estimations de risque au‑delà de ce que permettent aujourd’hui les tests standard. Ensuite, si des travaux expérimentaux futurs confirment que TTF2 aide les tumeurs à échapper au système immunitaire, des médicaments bloquant ou modulant TTF2 — ou ses voies en aval — pourraient entrer dans de nouvelles thérapies combinées rendant l’immunothérapie plus efficace pour les personnes atteintes de ce cancer cérébral dévastateur.
Citation: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
Mots-clés: gliome, TTF2, biomarqueur des tumeurs cérébrales, microenvironnement immunitaire tumoral, cible d’immunothérapie