Clear Sky Science · fr
Températures de transition vitreuse des liquides formant du verre purs et des mélanges binaires
Pourquoi le ralentissement des liquides compte dans la vie courante
De nombreux matériaux que nous utilisons — des écrans de smartphone et des emballages plastiques aux aliments lyophilisés et aux médicaments — ne sont pas des solides au sens strict mais des verres : des liquides dont le mouvement est devenu si lent qu’ils semblent figés. Comprendre quand un liquide fluide se transforme en verre, et comment cette « température de congélation » change lorsque l’on mélange des substances, est essentiel pour fabriquer des produits plus sûrs, plus stables et plus durables. Cet article propose une nouvelle méthode pour calculer directement cette température clé à partir de la façon dont les molécules d’un matériau se relaxent et se déplacent, et étend l’idée aux mélanges tels que les mélanges de sucres et les systèmes sucre–eau utilisés en alimentation et en pharmacie.
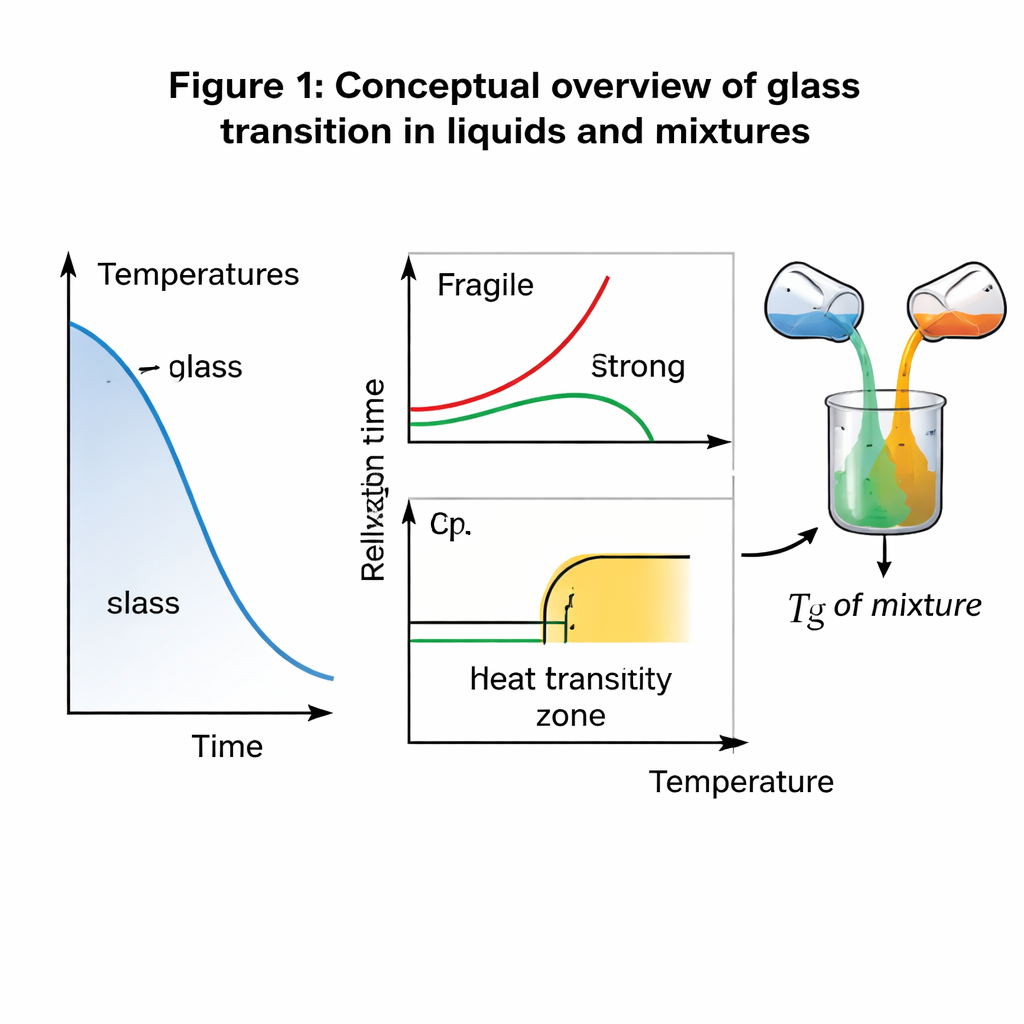
Des fondus nets aux « congelés » progressifs
Les cristaux comme la glace ou le sel de table fondent à une température nette et bien définie. Les verres se comportent différemment. Lorsqu’un liquide formant du verre refroidit, ses molécules ralentissent progressivement jusqu’à ce qu’à la température de transition vitreuse (Tg) elles ne puissent plus se réarranger assez rapidement pour suivre le changement de température. Le matériau sort de l’équilibre et se comporte comme un solide rigide mais désordonné. Classiquement, les scientifiques décrivent Tg de deux manières : thermodynamiquement, par un saut de capacité calorifique (la quantité de chaleur nécessaire pour chauffer le matériau), et dynamiquement, par le temps nécessaire aux réarrangements moléculaires. Une règle empirique courante situe Tg là où le temps de relaxation structurelle atteint environ 100–1000 secondes — mais il s’agit surtout d’une convention pratique plutôt que d’un principe fondé sur la physique.
Un lien plus net entre temps, température et vitesse de balayage
Les auteurs s’appuient sur une idée classique qui relie directement la vitesse à laquelle la température est modifiée dans une expérience (la vitesse de balayage) à la rapidité avec laquelle le temps de relaxation du matériau varie avec la température. Essentiellement, la transition vitreuse est définie comme le point où l’échelle de temps de la relaxation structurelle devient comparable à l’échelle de temps du balayage de température. En utilisant des modèles standards qui décrivent comment le temps de relaxation dépend de la température, ils transforment cette condition en équations mathématiques explicites pour Tg. Ces équations impliquent une fonction mathématique spéciale (la fonction Lambert W) qui est récemment devenue largement disponible dans les logiciels scientifiques, rendant pratique la résolution analytique de tels problèmes plutôt que le simple ajustement numérique.
Pourquoi l’échelle de temps « universelle » du verre est un mythe
Avec leurs nouvelles équations, les auteurs montrent que le temps de relaxation à la transition vitreuse, souvent supposé être une valeur « de laboratoire » fixe, dépend en réalité fortement à la fois de la vitesse de balayage et de l’énergie d’activation du matériau — la barrière énergétique effective qui contrôle le mouvement moléculaire. Pour une vitesse de balayage donnée, les matériaux ayant des énergies d’activation ou des Tg plus élevés peuvent présenter des temps de relaxation à la transition vitreuse qui diffèrent de plusieurs ordres de grandeur. Des simulations utilisant des modèles de transition vitreuse répandus confirment que, bien que différentes façons de définir Tg (par exemple là où la courbe de capacité calorifique fléchit le plus) ne soient pas identiques, elles donnent des températures très proches, tout en démontrant clairement qu’il n’existe pas un temps de relaxation unique et universel applicable à tous les formateurs de verre.
Comment les mélanges de formateurs de verre partagent leurs caractéristiques
Les matériaux réels sont rarement purs. Dans les mélanges de polymères, les produits alimentaires ou les médicaments amorphes, deux substances formant du verre ou plus sont mélangées, et les fabricants doivent connaître comment Tg du mélange dépend de la composition. Empiriquement, ceci est souvent décrit par l’équation de Gordon–Taylor, qui fait intervenir une constante d’ajustement dont la signification physique est restée peu claire et débattue. Les auteurs proposent une alternative dynamique : ils supposent que des paramètres cinétiques clés — comme les énergies d’activation effectives et des grandeurs apparentées — se mélangent de façon simple basée sur les fractions massiques de chaque composant. À partir de ces « règles de mélange dynamique idéales », ils dérivent une expression générale pour Tg du mélange et montrent que, dans un cas limite, la formule familière de Gordon–Taylor apparaît naturellement, la constante d’ajustement étant reliée aux énergies d’activation ou aux fragilités des composants (une mesure de la rapidité avec laquelle leur relaxation ralentit au refroidissement).
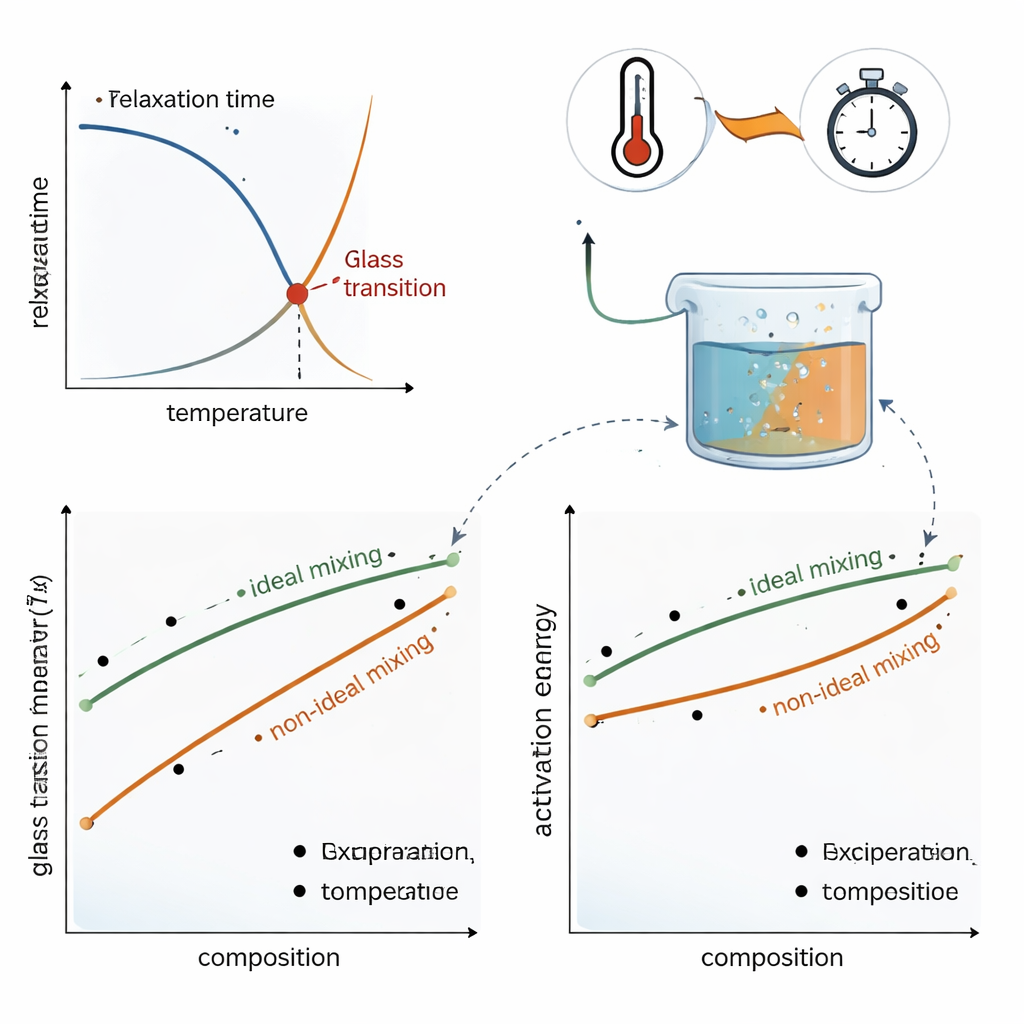
Mélanges réels : quand les règles idéales se brisent
Pour tester leur cadre, les auteurs examinent des données de deux systèmes d’importance pratique. Dans les mélanges des sucres saccharose et tréhalose — courants en conservation alimentaire et biologique — Tg mesurée et énergie d’activation varient seulement légèrement par rapport à ce que prédit un mélange dynamique idéal ; de modestes ajustements des règles de mélange captent les courbes observées. Dans les mélanges saccharose–eau, en revanche, le comportement est fortement non idéal : l’ajout d’une petite quantité d’eau diminue l’énergie d’activation et Tg bien plus qu’une simple moyenne ne le laisserait supposer. En autorisant des règles de mélange non linéaires, le nouveau modèle peut reproduire la dépendance pleinement incurvée de Tg et de l’énergie d’activation en fonction de la composition, reflétant la façon dont l’eau assouplit dramatiquement le réseau moléculaire du verre de sucre.
Message clé pour les matériaux et les produits du quotidien
En résumé, ce travail montre que la température à laquelle un liquide devient verre n’est pas gouvernée par une unique échelle de temps magique, mais par la rapidité avec laquelle les mouvements internes du liquide répondent à une vitesse de refroidissement ou de chauffage donnée. La même logique cinétique s’étend naturellement aux mélanges, où la relation largement utilisée de Gordon–Taylor apparaît comme un cas particulier de règles dynamiques plus générales. Pour les technologues concevant des écrans de téléphone plus résistants, des aliments plus durables ou des médicaments plus stables, ce cadre offre une manière plus fondée physiquement de prédire et d’ajuster les températures de transition vitreuse tant pour les matériaux purs que pour les mélanges complexes.
Citation: Kocherbitov, V., Argatov, I. Glass transition temperatures of pure glass-forming liquids and binary mixtures. Sci Rep 16, 1317 (2026). https://doi.org/10.1038/s41598-026-35024-4
Mots-clés: transition vitreuse, temps de relaxation, fragilité, mélanges formant du verre, équation de Gordon–Taylor