Clear Sky Science · fr
Base structurale du diosgénine en tant qu'agoniste inverse du récepteur orphelin apparenté à l'acide rétinoïque γ
Pourquoi un composé végétal et un commutateur immunitaire comptent
De nombreuses pathologies chroniques — des maladies auto-immunes comme la sclérose en plaques et le psoriasis jusqu’à l’obésité et le diabète de type 2 — sont alimentées par des signaux immunitaires excessifs et des signaux métaboliques désynchronisés. Les scientifiques cherchent depuis longtemps des médicaments plus sûrs capables de régler ces signaux avec précision. Cette étude examine comment le diosgénine, une molécule naturelle présente dans certaines plantes médicinales et ignames, se lie à une protéine régulatrice du système immunitaire appelée RORγ et la fait basculer vers un état moins actif. Comprendre cette interaction au niveau atomique pourrait ouvrir la voie à des thérapies plus douces et plus ciblées, dérivées d’un échafaudage naturel familier.
Un régulateur maître de l’immunité et du métabolisme
RORγ fait partie d’une grande famille de « récepteurs nucléaires » — des protéines intracellulaires qui activent ou désactivent des gènes en réponse à de petites molécules. Cette protéine particulière contrôle un groupe de cellules immunitaires appelées cellules Th17, qui produisent le signal inflammatoire IL-17A et sont associées à des maladies auto-immunes telles que la sclérose en plaques, le psoriasis, la polyarthrite rhumatoïde et la maladie de Crohn. RORγ influence aussi le développement des cellules adipeuses et la réponse de l’organisme à l’insuline, le reliant à l’obésité et au diabète. En raison de ce large spectre d’action, RORγ est devenu une cible attractive pour les médicaments, mais de nombreuses molécules synthétiques qui s’y lient ont rencontré des problèmes de sécurité, de sélectivité ou d’efficacité chez l’humain.
Un remède traditionnel fournit une piste prometteuse
Le diosgénine est une molécule de type stéroïde extraite de plantes, notamment des espèces de Dioscorea (igname sauvage) et de plusieurs plantes médicinales traditionnelles. Elle a été étudiée pour ses effets anti-inflammatoires, anticancéreux, antidiabétiques et cardiovasculaires dans des modèles cellulaires et animaux. Des travaux antérieurs suggéraient que le diosgénine pouvait influencer la voie RORα/γ et supprimer les réponses Th17 nocives, mais il n’était pas clair s’il agissait directement sur RORγ ni de quelle manière il modulait le comportement de la protéine. Pour répondre à ces questions, les auteurs ont criblé une bibliothèque de composés naturels avec un test de liaison sensible et ont identifié le diosgénine comme un ligand fort de la région de liaison du ligand de RORγ.
Comment le diosgénine fait rétrograder RORγ
Les chercheurs ont étudié la manière dont le diosgénine affecte la capacité de RORγ à recruter des protéines auxiliaires qui amplifient (coactivateurs) ou atténuent (corépresseurs) l’activité génique. De manière surprenante, le diosgénine favorisait la liaison de RORγ à ces deux types de partenaires, un profil différent de celui d’un antagoniste naturel connu, l’acide ursolique. Dans des essais cellulaires de type rapporteur qui suivent la commutation des gènes, le diosgénine a systématiquement réduit l’activité dirigée par RORγ de façon dépendante de la dose, avec une puissance dans la gamme sous-micromolaire. Ce comportement correspond au profil d’un « agoniste inverse » : un composé qui non seulement bloque l’activité de base mais pousse activement le récepteur vers un état éteint, même lorsqu’il serait autrement activé.
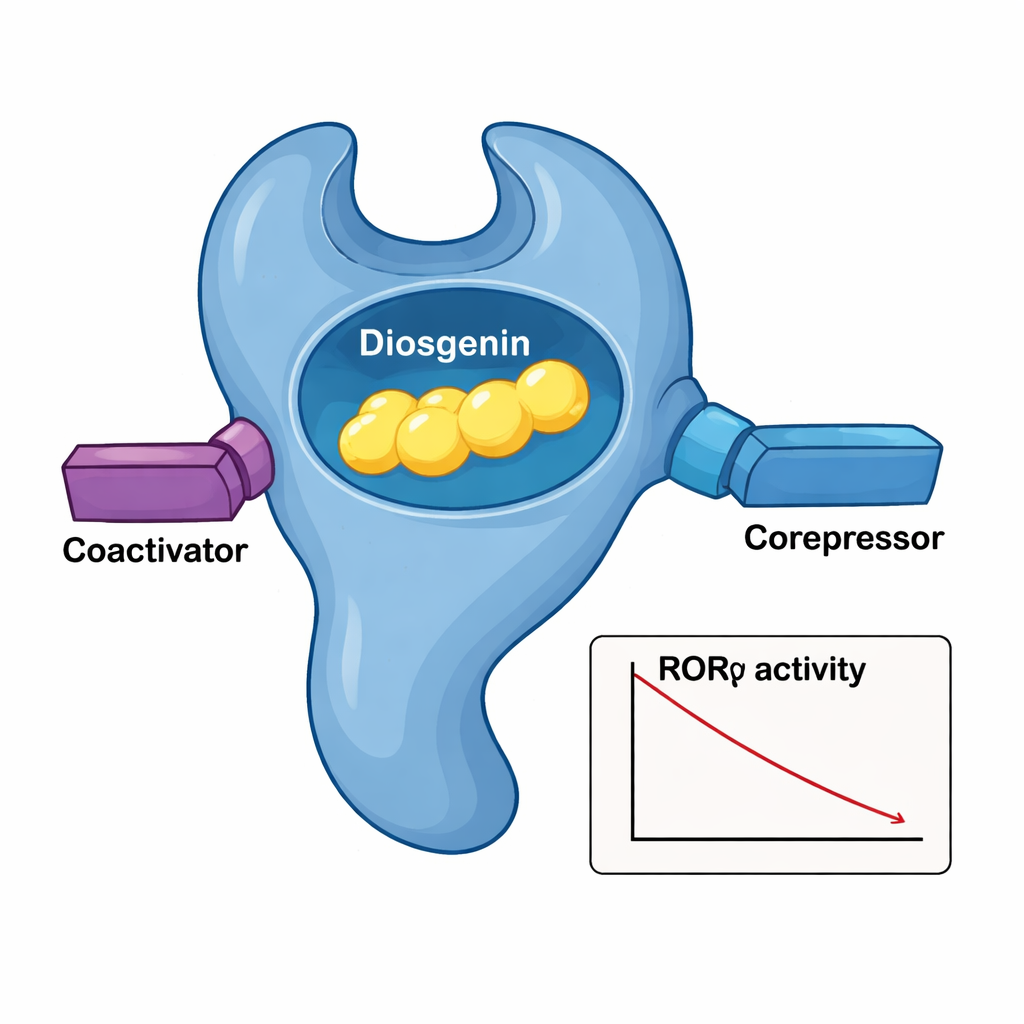
Gros plan sur la poignée moléculaire
Pour voir précisément comment le diosgénine s’insère dans RORγ, l’équipe a résolu la structure cristalline tridimensionnelle du domaine de liaison du ligand de la protéine avec le diosgénine logé à l’intérieur. Le récepteur se replie en un faisceau superposé d’hélices, formant une poche qui berce le noyau de type stéroïde du diosgénine. Un réseau de contacts hydrophobes serrés issus de plusieurs acides aminés agit comme un gant sur la colonne vertébrale de la molécule, tandis qu’un groupe hydroxyle critique du diosgénine forme des liaisons hydrogène médiées par l’eau avec deux résidus d’arginine. Lorsque ces résidus de la poche ont été mutés un à un, la capacité du diosgénine à réduire l’activité de RORγ diminuait, confirmant leur importance. Les comparaisons structurelles avec le complexe RORγ–acide ursolique ont montré que le diosgénine maintient une hélice caudale clé (AF‑2) dans une position « active-like » tout en entraînant néanmoins une baisse globale de la transcription, ce qui explique pourquoi il peut attirer à la fois coactivateurs et corépresseurs.
De la structure cristalline aux médicaments de demain
La description détaillée de l’interaction diosgénine–RORγ met en évidence deux avantages notables pour la conception de médicaments. Premièrement, la poche du récepteur montre une flexibilité suffisante pour reconnaître des formes de ligands différentes, ce qui signifie que les chimistes peuvent affiner l’échafaudage du diosgénine pour améliorer la sélectivité envers RORγ et réduire les liaisons non désirées à d’autres récepteurs nucléaires. Deuxièmement, l’origine naturelle du diosgénine et sa faible toxicité intrinsèque connue dans des modèles précliniques en font un point de départ séduisant comparé à certains composés entièrement synthétiques qui ont échoué en essais. En termes simples, ce travail révèle comment une molécule d’origine végétale peut se fixer sur un commutateur central de l’immunité et du métabolisme et le faire rétrograder, offrant un modèle structural pour développer des traitements plus sûrs et plus efficaces contre les maladies liées à RORγ.
Citation: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Mots-clés: ROR gamma, diosgénine, maladie auto-immune, récepteur nucléaire, agoniste inverse