Clear Sky Science · fr
Caractérisation transcriptomique de l’épissage alternatif aberrant dans les muscles squelettiques des patients atteints de sarcopénie
Pourquoi les muscles vieillissants perdent de la force
La sarcopénie — la perte progressive de masse et de force musculaires liée à l’âge — est l’une des principales raisons pour lesquelles les personnes âgées rencontrent des difficultés dans les tâches quotidiennes, comme monter des escaliers ou porter des courses. Cette étude explore le muscle vieillissant au niveau de l’ARN, ces messages qui indiquent aux cellules quelles protéines produire. Les auteurs montrent que, dans la sarcopénie, beaucoup de ces messages ARN sont découpés et recousus de manière anormale, ce qui pourrait perturber la production d’énergie dans le muscle et pointer vers de nouvelles cibles thérapeutiques.
Perte musculaire et « édition » des gènes par la cellule
Nos gènes sont écrits dans l’ADN, mais les cellules travaillent à partir de copies ARN de ces gènes. Avant d’être utilisés, ces messages ARN sont normalement taillés et épissés — un peu comme le montage d’un film — de sorte qu’un même gène peut produire plusieurs versions d’une protéine. Ce processus, appelé épissage alternatif, est particulièrement actif dans le muscle, qui a besoin de protéines finement ajustées pour se contracter, se réparer et s’adapter à l’exercice. Quand l’épissage déraille, de mauvaises versions de protéines peuvent être produites ou des versions importantes peuvent disparaître, contribuant à des maladies comme la dystrophie musculaire et certains troubles cérébraux. Les auteurs ont émis l’hypothèse qu’un niveau similaire de mauvaise édition de l’ARN pourrait sous-tendre la sarcopénie.
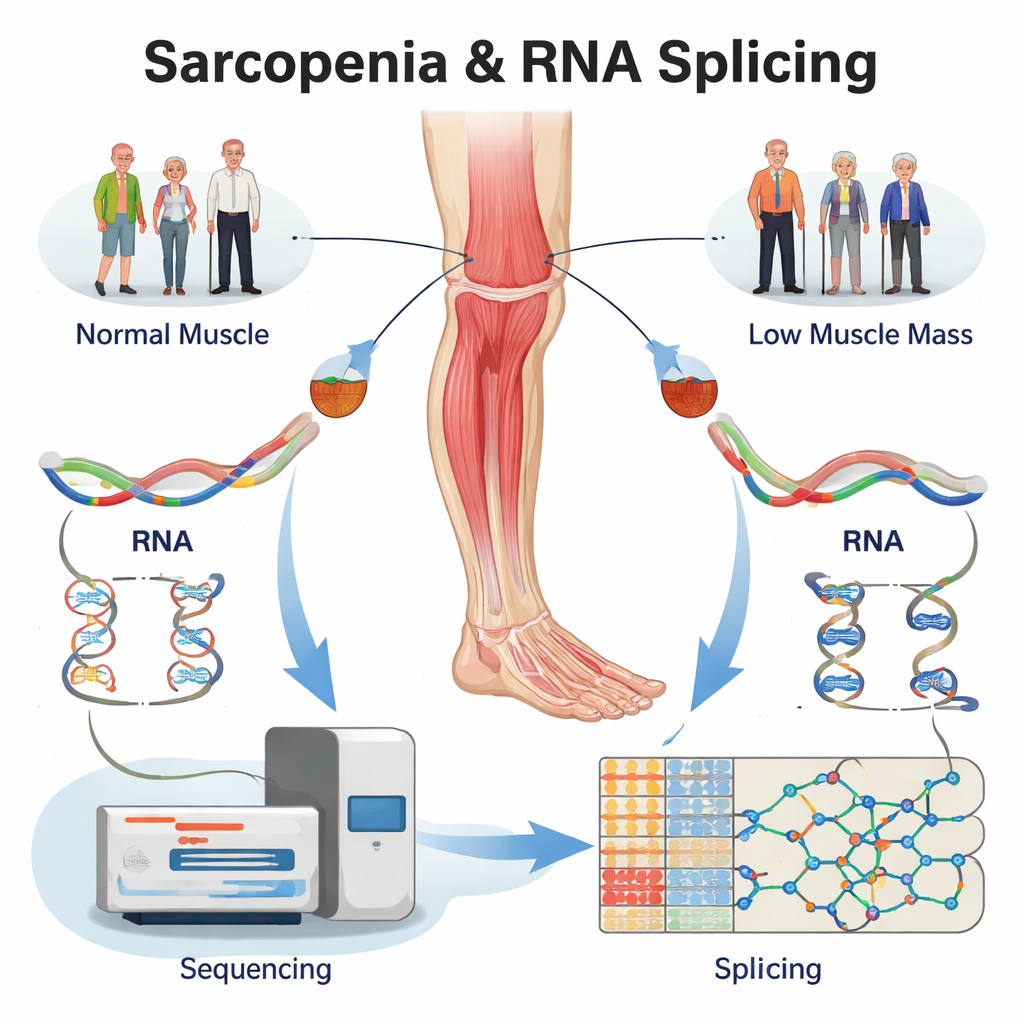
Réexploiter des données existantes pour détecter des erreurs d’ARN cachées
Plutôt que de recruter de nouveaux volontaires, l’équipe a réanalysé un important jeu de données d’ARN-seq issu de biopsies de muscles de la cuisse humaine. Les échantillons provenaient de quatre groupes : des personnes âgées atteintes de sarcopénie avérée, des personnes ayant uniquement une faible masse musculaire, des personnes ayant uniquement une faible force musculaire, et des témoins sains appariés par âge. À l’aide de logiciels spécialisés, ils ont d’abord confirmé que des centaines de gènes étaient surexprimés ou sous-exprimés dans les muscles malades. Plus important encore, ils ont ensuite examiné la façon dont l’ARN de chaque gène était épissé, répertoriant plus de 5 000 changements d’épissage dans les trois groupes problématiques comparés au muscle sain. Ces modifications se concentraient dans quelques types basiques — comme le saut d’exon ou le choix d’un site de coupure alternatif — des schémas connus pour altérer fortement la structure des protéines.
Usines d’énergie et voies « indicatrices » de carburant perturbées
Les changements d’épissage sont apparus dans des gènes centraux pour la biologie musculaire. Beaucoup de gènes affectés codent des composants des mitochondries, ces minuscules usines d’énergie qui alimentent la contraction musculaire. Dans le muscle sarcopénique, 16 gènes impliqués dans la phosphorylation oxydative — le processus qui convertit les nutriments en énergie utilisable — présentaient un épissage altéré, en particulier des composants des complexes mitochondriaux responsables du transport des électrons et du pompage des protons. D’autres modifications concernaient des gènes qui produisent ou utilisent le NAD⁺, une molécule clé pour l’énergie cellulaire et la réparation. Plutôt que de simplement varier en quantité, des enzymes importantes telles que CD38, PARP2 et plusieurs sirtuines produisaient différentes variantes d’ARN, suggérant que l’équilibre entre production et consommation de NAD⁺ est perturbé au niveau de l’épissage. Les gènes affectés se regroupaient aussi dans des voies de signalisation musculaire bien connues, notamment AMPK et FoxO, qui fonctionnent comme des jauges de carburant et des répondeurs au stress cellulaire.
Schémas partagés selon les stades — et entre espèces
De façon frappante, beaucoup des mêmes gènes montraient des changements d’épissage non seulement chez les personnes atteintes de sarcopénie complète, mais aussi chez celles qui n’avaient qu’une faible masse musculaire ou seulement une faible force. Cela suggère que l’épissage anormal commence tôt et traverse les différents visages cliniques de la maladie. Pour tester si ces changements pouvaient être reproduits dans un modèle animal, les chercheurs ont induit une fonte musculaire chez la souris avec la dexaméthasone, un stéroïde utilisé classiquement pour reproduire certains aspects de la sarcopénie. Les souris ont développé une force d’agrippement réduite et de moins bonnes performances aux tests de course et d’équilibre. Lorsque l’équipe a séquencé l’ARN musculaire des souris, elle a à nouveau trouvé des centaines de gènes à épissage altéré. Environ un cinquième de ces gènes se recoupaient avec ceux identifiés chez l’humain atteints de sarcopénie, et beaucoup étaient impliqués dans le contrôle de la transcription, la structure de la chromatine et l’épissage lui-même — des commutateurs de haut niveau capables de remodeler l’ensemble de la production protéique d’une cellule.
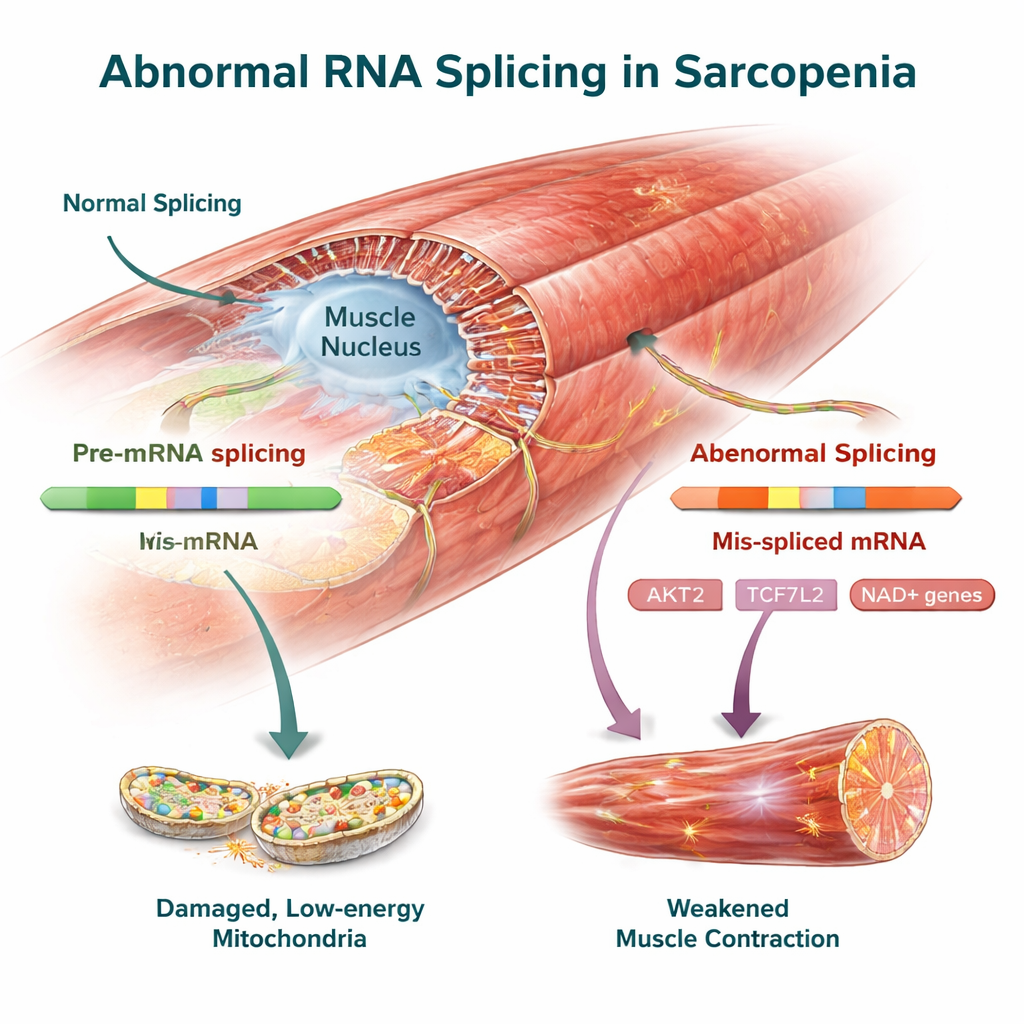
Gènes clés du contrôle musculaire comme cibles thérapeutiques potentielles
Parmi les changements conservés entre espèces figuraient plusieurs gènes déjà liés à la santé musculaire. AKT2, régulateur central de la croissance et de la synthèse protéique dans le muscle, présentait des décalages d’épissage distincts chez l’homme et la souris qui pourraient réduire sa capacité à maintenir la masse musculaire. TCF7L2, composant de la voie Wnt, ainsi que FMNL2 et USP40, qui aident à organiser l’ossature interne du muscle et le contrôle qualité des protéines, portaient aussi des variantes d’ARN altérées. L’équipe a confirmé expérimentalement ces changements d’épissage dans le muscle de souris, renforçant l’idée qu’il s’agit de caractéristiques réelles de la maladie et non d’artéfacts d’analyse de données.
Ce que cela signifie pour prévenir la fragilité
Pour un public non spécialiste, le message est que la sarcopénie ne se résume pas à des muscles qui « s’usent » ou à des gènes simplement activés ou désactivés. Elle implique aussi une mauvaise édition généralisée des messages ARN qui dirigent la façon dont les cellules musculaires fabriquent et entretiennent leurs composants, en particulier les systèmes qui génèrent l’énergie et détectent le stress. Parce que l’épissage peut, en principe, être corrigé avec des médicaments à base d’ARN conçus de façon précise, les erreurs d’épissage conservées identifiées ici — en particulier dans des gènes comme AKT2 et TCF7L2 — offrent un nouvel ensemble de pistes pour des thérapies visant à aider les muscles vieillissants à rester plus forts plus longtemps.
Citation: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Mots-clés: sarcopénie, vieillissement musculaire, épissage de l’ARN, mitochondries, AKT2