Clear Sky Science · fr
Modèle phénoménologique de stabilisation de la transthyrétine
Pourquoi cela compte pour les patients et les familles
L’amylose à la transthyrétine est une affection grave dans laquelle une protéine sanguine normale, la transthyrétine (TTR), se désassemble et ses fragments peuvent s’agglomérer en dépôts nocifs dans le cœur et les nerfs. De nouveaux médicaments comme le tafamidis et l’acoramidis sont conçus pour maintenir cette protéine sous sa forme sûre à quatre sous‑unités, et ils ont déjà amélioré le pronostic de nombreux patients. Pourtant, les cliniciens observent un effet déroutant chez les patients traités : les taux sanguins de TTR augmentent de plus de 30 %, et la raison n’est pas évidente. Cet article utilise un modèle épuré, fondé sur les mathématiques, pour explorer ce qui pourrait se passer dans l’organisme et ce que cela implique sur le mode d’action réel de ces médicaments. 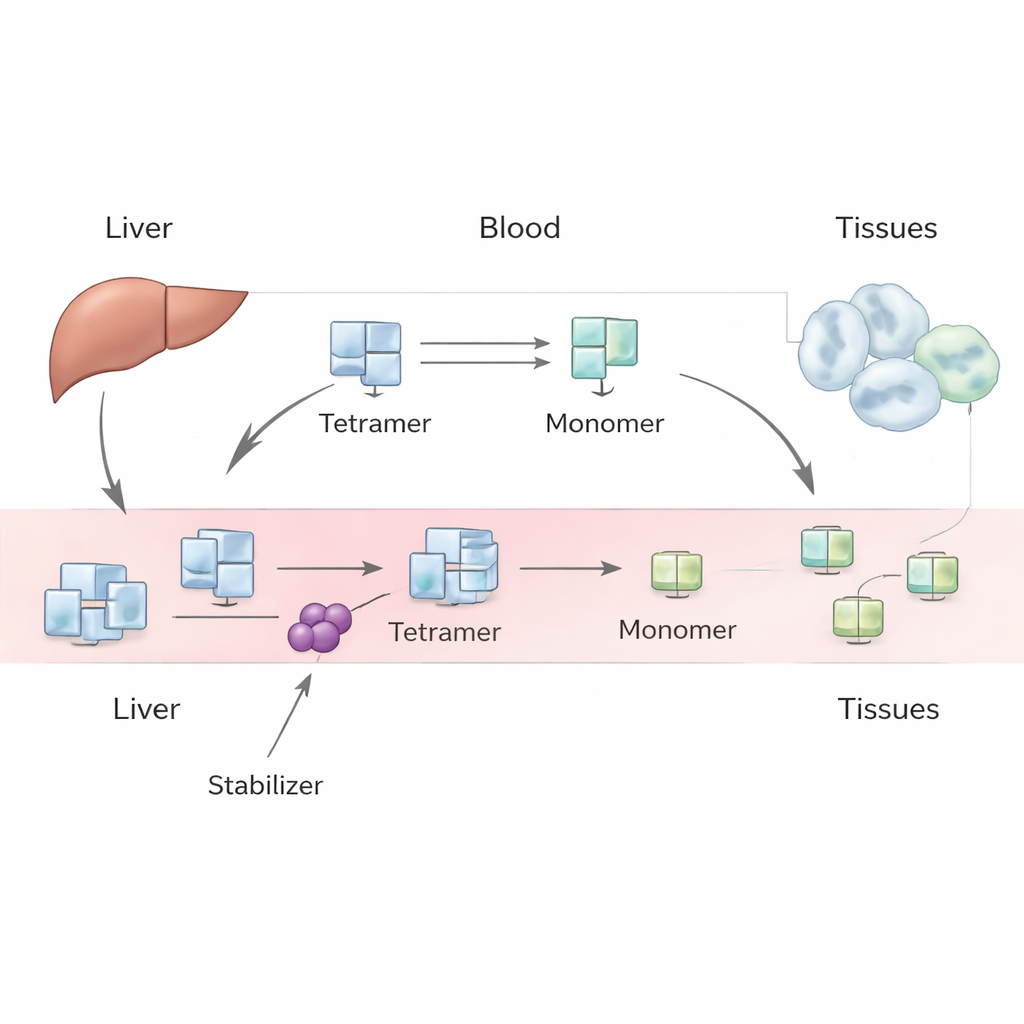
Une protéine qui peut aider ou nuire
La TTR est principalement produite par le foie et circule normalement dans le sang sous la forme stable d’un assemblage de quatre sous‑unités identiques, appelé tétramère. Elle transporte l’hormone thyroïdienne et la vitamine A. Dans certaines circonstances, notamment le vieillissement ou des variantes génétiques héréditaires, ce tétramère peut se dissocier en sous‑unités isolées, ou monomères. Ces monomères peuvent se replier de façon erronée et s’assembler en fibrilles amyloïdes, qui endommagent les tissus et conduisent à l’amylose à la transthyrétine du cœur (cardiomyopathie) ou des nerfs (neuropathie). Des médicaments comme le tafamidis et l’acoramidis sont conçus pour se lier au tétramère et rendre plus difficile sa dissociation, ralentissant ainsi la progression de la maladie. Cependant, lorsque les patients commencent ces traitements, leurs taux plasmatiques mesurés de TTR augmentent de façon régulière, et cette hausse est plus importante que ce que prédisent de simples expériences de laboratoire.
Construire une image simple d’un système complexe
Les auteurs abordent ce casse‑tête avec un modèle phénoménologique — qui se concentre sur le comportement global observable plutôt que sur chaque détail microscopique. Dans leur cadre, le foie produit des tétramères de TTR à un rythme constant, qui entrent ensuite dans la circulation sanguine. Une fois en circulation, les tétramères peuvent se dissocier en monomères et se réassembler, et tant les tétramères que les monomères peuvent être éliminés du sang par captation tissulaire et dégradation. En écrivant une paire d’équations de bilan de masse pour les tétramères et les monomères, l’équipe explore différents scénarios : l’un où les monomères rejoignent principalement les tétramères, un autre où ils sont rapidement éliminés, et un cas intermédiaire où les deux processus sont importants. Ils utilisent des études historiques de traceurs chez l’humain et des données de laboratoire modernes pour estimer des quantités clés, comme la vitesse d’élimination des tétramères, la rapidité de leur dissociation et l’intensité avec laquelle les médicaments ralentissent cette désorganisation.
Pourquoi la stabilisation du tétramère seule ne suffit pas
Armés de ces estimations, les chercheurs posent une question directe : si un médicament pouvait empêcher parfaitement la dissociation des tétramères, de combien augmenterait le taux sanguin de TTR ? Dans tous les régimes plausibles, la réponse est modeste — de l’ordre de 15 % au maximum pour des valeurs typiques des paramètres, et souvent moins, selon la façon dont les monomères sont traités. Cela est bien en deçà de l’augmentation >30 % observée chez les patients traités. Le décalage persiste même en autorisant une incertitude généreuse sur les paramètres connus. Le modèle suggère donc que ralentir la dissociation des tétramères ne peut pas, à lui seul, expliquer l’effet clinique complet. D’autres processus qui contrôlent la vitesse de production de la TTR, sa captation par les cellules ou sa dégradation doivent également changer en présence des médicaments stabilisateurs. 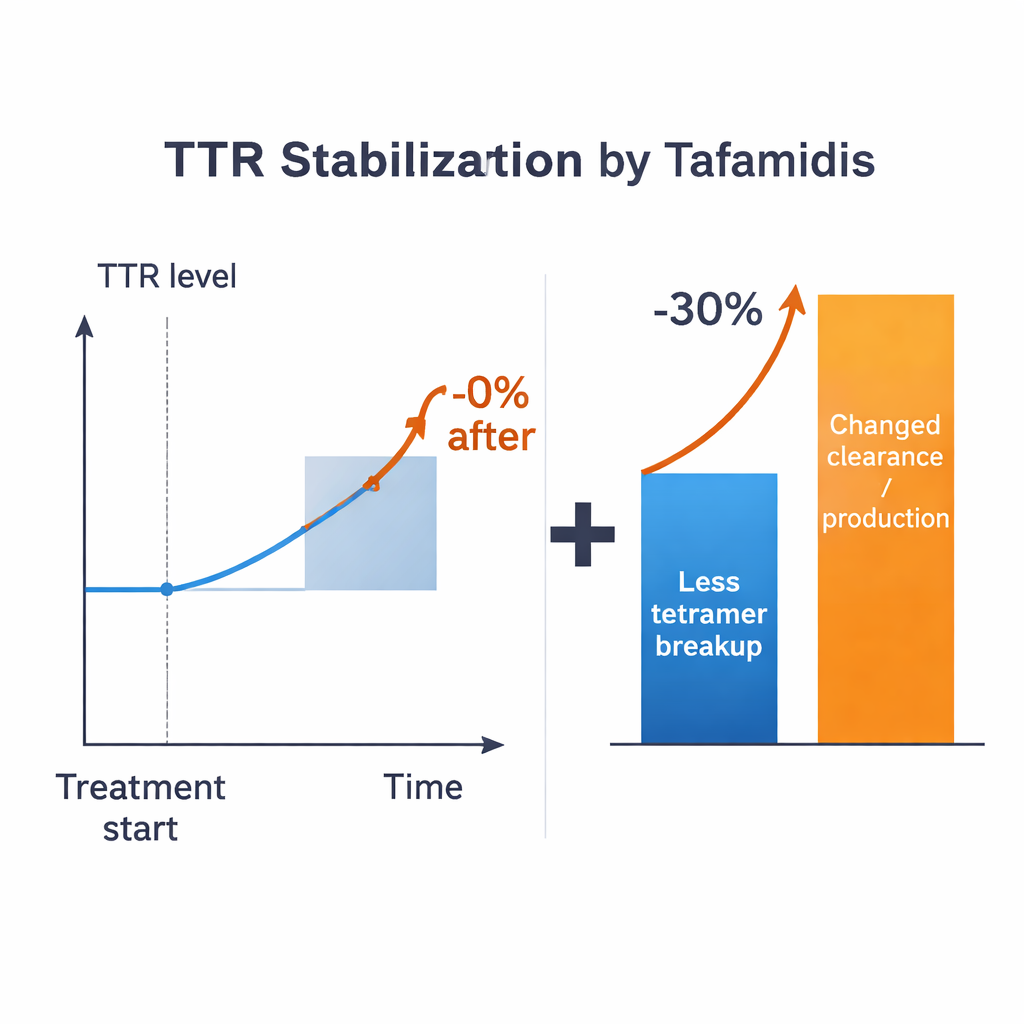
Indices tirés des niveaux de médicament et d’expériences astucieuses
Pour relier l’exposition au médicament au comportement de la TTR, les auteurs combinent un modèle pharmacocinétique de base du tafamidis (comment le médicament se déplace dans l’organisme au fil du temps) avec des essais spécialisés d’« échange de sous‑unités ». Dans ces expériences, des tétramères de TTR marqués et non marqués sont mélangés dans du plasma humain, et l’échange progressif des sous‑unités révèle à quelle fréquence les tétramères se dissocient. Mesurer ce processus à différentes concentrations de médicament fournit un lien direct et fondé sur les données entre le niveau de tafamidis et la stabilité effective du tétramère, sans avoir à connaître la part de médicament liée à l’albumine ou à l’hormone thyroïdienne. Ce lien phénoménologique alimente le modèle et évite proprement de nombreux inconnus biochimiques. Pourtant, même avec cet avantage, les calculs plafonnent encore la hausse attendue de la TTR à environ la moitié de l’augmentation clinique observée, renforçant l’idée que des changements dans l’élimination, l’internalisation, la dégradation, ou même la synthèse doivent faire partie de l’explication.
Ce que cela implique pour la suite
Pour les non‑spécialistes, le message clé est que ces médicaments stabilisateurs font probablement plus que simplement « coller » les tétramères de TTR entre eux. Ils affectent sans doute aussi la manière dont l’organisme produit, élimine ou recycle la protéine. Les auteurs soutiennent que des modèles simples et transparents comme le leur sont puissants parce qu’ils mettent en évidence de telles lacunes dans notre compréhension et indiquent des expériences concrètes — par exemple, mesurer directement la vitesse d’élimination des monomères, la rapidité avec laquelle les différentes formes de TTR sont captées par les cellules, ou si la TTR liée au médicament est traitée différemment de la protéine non liée. Mieux répondre à ces questions affinerait non seulement le traitement de l’amylose à la transthyrétine, mais pourrait aussi révéler des règles générales applicables à d’autres maladies où des protéines normales se transforment en agrégats nocifs.
Citation: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Mots-clés: amylose à la transthyrétine, stabilisation des protéines, tafamidis, modélisation pharmacocinétique, maladies amyloïdes