Clear Sky Science · fr
Combinaison de bactériophages et de composés antibiofilm issus de bactéries de la phyllosphère comme stratégie globale pour le contrôle des agents pathogènes en aquaculture et dans l’alimentation
Pourquoi ces couches bactériennes visqueuses comptent pour votre nourriture et vos poissons
Qu’il s’agisse de poissons provenant d’étangs d’aquaculture ou de produits prêts à consommer en supermarché, les deux peuvent être menacés par des communautés bactériennes invisibles qui adhèrent aux surfaces sous forme de couches résistantes et visqueuses appelées biofilms. Ces biofilms aident les bactéries nuisibles à résister au nettoyage, aux conservateurs et aux antibiotiques, contribuant aux intoxications alimentaires et aux foyers de maladie dans les élevages piscicoles. Cette étude explore une approche inspirée de la nature pour s’attaquer à ces couches tenaces en combinant des virus qui détruisent les bactéries avec des composés naturels produits par des bactéries inoffensives vivant sur les feuilles des plantes.
Boucliers cachés sur les lignes de production et dans les bassins
Les bactéries formant des biofilms telles que Bacillus cereus, responsable d’intoxications alimentaires, et Vibrio harveyi, un pathogène sérieux pour les poissons, sont particulièrement difficiles à contrôler parce que leur revêtement visqueux les protège des conditions agressives et des traitements courants. Ce bouclier, appelé matrice extracellulaire, est composé de sucres collants, de protéines et d’ADN qui cimentent les cellules entre elles et aux surfaces des tuyaux, réservoirs et équipements de transformation. Avec la hausse de l’aquaculture et de la consommation de produits de la mer dans le monde, ces films résilients représentent des risques croissants pour la santé publique et des pertes économiques. Les méthodes actuelles reposent souvent sur des antibiotiques ou des conservateurs chimiques, qui peuvent être inefficaces contre les biofilms et poser des problèmes de résistance et de résidus.
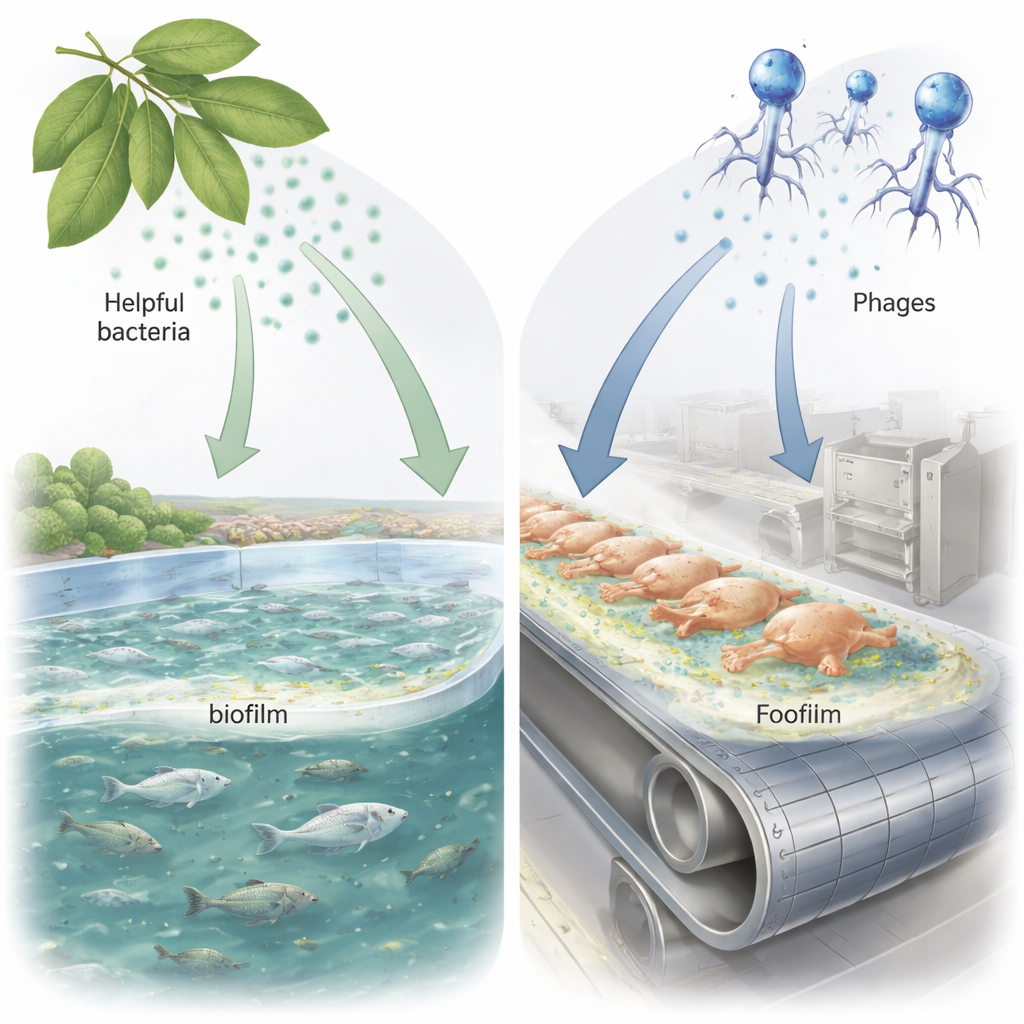
Aller chercher de l’aide auprès des microbes des feuilles et de leurs ennemis viraux
Pour trouver de nouveaux outils, les chercheurs se sont tournés vers les bactéries de la phyllosphère — des microbes qui vivent naturellement à la surface des feuilles et qui entrent en compétition avec d’autres bactéries dans cet environnement exposé et contraignant. Deux souches, Pseudomonas fluorescens JB 3B et Proteus myxofaciens JB 20B, produisent des mélanges de petites molécules dans le milieu liquide qui les entoure, appelés surnageants. L’équipe a testé ces surnageants aux côtés de deux bactériophages très concentrés, des virus qui infectent et lysent des bactéries spécifiques : l’un ciblant B. cereus et l’autre ciblant V. harveyi. Plutôt que de vérifier seulement si ces traitements tuaient les bactéries en suspension, les chercheurs se sont concentrés sur leur capacité à prévenir la formation de biofilms et à dissoudre des biofilms matures déjà établis.
Démanteler les parois des biofilms par des mécanismes différents
Les surnageants des bactéries de feuilles ne se comportaient pas comme des antibiotiques classiques : ils ne créaient pas de zones d’inhibition nettes sur des plaques et ne bloquaient pas le « quorum sensing » bactérien, la signalisation chimique souvent utilisée pour coordonner la construction du biofilm. Pourtant, lorsque les scientifiques ont cultivé des biofilms dans de petits puits d’essai, ces surnageants ont réduit de manière significative à la fois la formation de nouveaux films et la destruction des films existants pour les deux espèces ciblées. Pour B. cereus, le surnageant de la souche JB 3B seul a réduit l’accumulation de biofilm d’environ 41 % et démantelé les films matures d’environ 55 %. Les phages seuls ont également montré une forte activité. Lorsqu’ils étaient combinés aux surnageants, les effets sur B. cereus étaient similaires ou légèrement meilleurs, suggérant que les deux outils pouvaient parfois agir en synergie. En revanche, pour V. harveyi, les meilleurs résultats provenaient souvent de traitements uniques — soit le phage, soit le surnageant — tandis que leur combinaison réduisait en fait l’efficacité, montrant qu’une recette universelle ne convient pas à toutes les espèces.
Ce que révèlent le microscope et la chimie
La microscopie optique et la microscopie électronique à balayage ont fourni un aperçu visuel avant-après de l’effet de ces traitements sur les biofilms. Les échantillons non traités montraient des couches épaisses et compactes de cellules enchâssées dans une matrice dense. Les échantillons traités, que ce soit par surnageant, par phage ou par les deux, présentaient des films plus minces et plus clairsemés, avec des lacunes nettes et une structure perturbée, en accord avec la diminution mesurée de la masse de biofilm. L’analyse chimique des surnageants de bactéries de feuilles par chromatographie en phase gazeuse couplée à la spectrométrie de masse a identifié plusieurs petites molécules — acide acétique, sarcosine, 4‑octadécénal et, dans une souche, érythritol — connues ou suspectées d’affaiblir les surfaces bactériennes, d’interférer avec l’attachement ou d’endommager des composants cellulaires. Ces résultats suggèrent que, plutôt que d’empoisonner directement les bactéries, les mélanges desserrent la « colle » et sapent la stabilité de la matrice du biofilm, facilitant ainsi l’action des phages et d’autres stress.
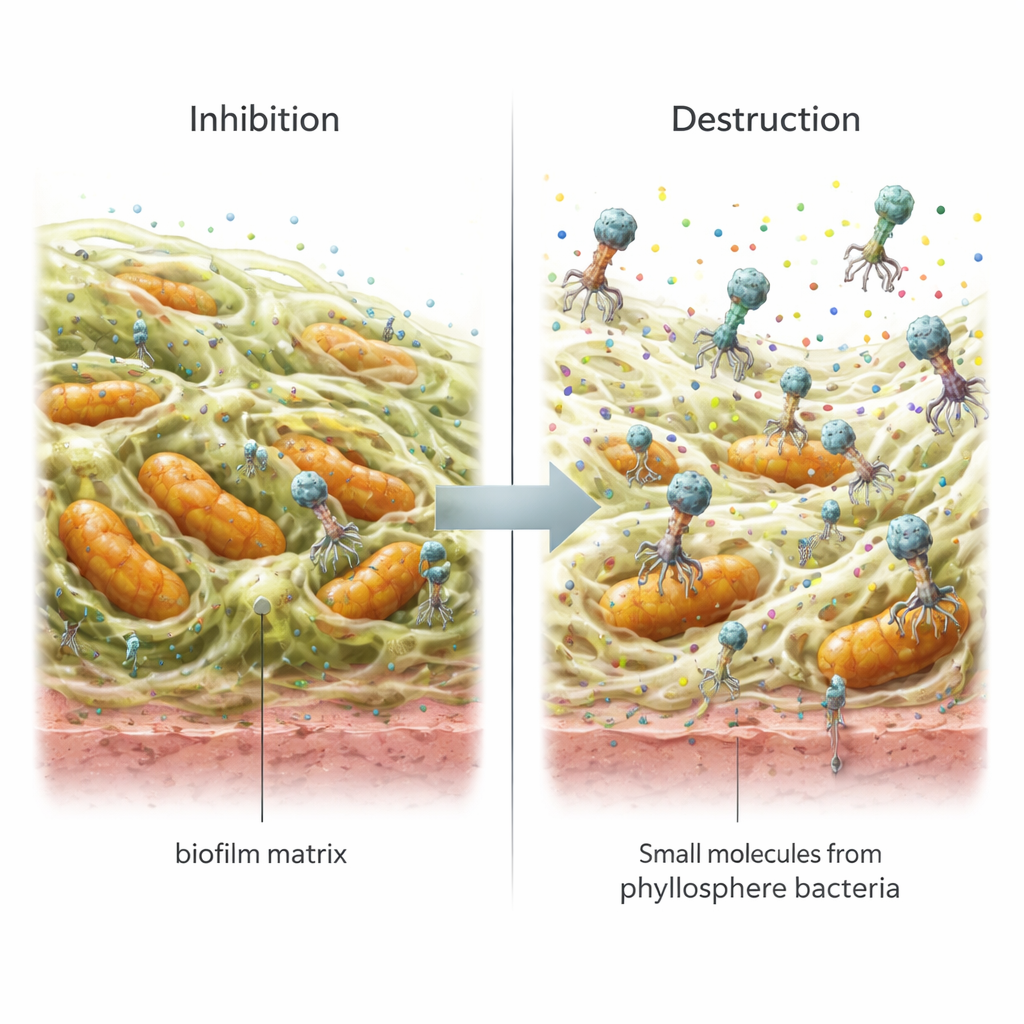
Ce que cela pourrait signifier pour une alimentation plus sûre et des poissons en meilleure santé
Pour un non-spécialiste, le message principal est que la nature offre des outils prometteurs pour gérer les films bactériens tenaces sans s’appuyer uniquement sur les antibiotiques traditionnels ou des produits chimiques agressifs. Les bactéries vivant sur les feuilles produisent des composés doux capables d’affaiblir les biofilms, et les bactériophages peuvent ensuite atteindre et tuer les cellules protégées. Toutefois, l’étude montre aussi que mélanger ces outils ne renforce pas toujours l’effet ; le succès dépend de l’espèce bactérienne ciblée et de la composition exacte du cocktail de composés. En pratique, cela signifie que les stratégies futures de lutte contre les biofilms en transformation alimentaire et en aquaculture pourront utiliser des combinaisons sur mesure de microbes « amicaux », de leurs produits naturels et de phages, soigneusement adaptées au pathogène visé. Avec des travaux complémentaires sur la sécurité et l’efficacité, de telles approches pourraient contribuer à réduire les maladies d’origine alimentaire et les pertes piscicoles tout en réduisant la pression sur les antibiotiques conventionnels.
Citation: May, J., Waturangi, D.E., Tan, W.A. et al. Combination of bacteriophage and antibiofilm compounds from phyllosphere bacteria as a comprehensive strategy for aquaculture and food pathogen control. Sci Rep 16, 4757 (2026). https://doi.org/10.1038/s41598-026-34989-6
Mots-clés: biofilms, bactériophages, aquaculture, sécurité alimentaire, bactéries de la phyllosphère