Clear Sky Science · fr
Les NP d’LBPs suppriment la progression du cancer du sein en inhibant l’expression de YAP1 pour induire la ferroptose et modifier le métabolisme énergétique
Des composés de baie face au cancer du sein
Beaucoup de gens connaissent les baies de goji comme un « superaliment » dans les thés et les mélanges de collations. Cette étude va bien au-delà des étagères d’épicerie en se demandant si des chaînes de sucres clés extraites de ces baies peuvent être transformées en un médicament minuscule et ciblé contre le cancer du sein. En étudiant le comportement de ces molécules naturelles lorsqu’elles sont encapsulées dans des nanoparticules et délivrées à des cellules mammaires en laboratoire, les chercheurs découvrent une nouvelle façon de pousser les cellules cancéreuses vers l’autodestruction tout en réduisant le potentiel de malignité des cellules normales.
Allumer et éteindre un interrupteur de croissance
Au cœur du travail se trouve une protéine appelée YAP1, qui fonctionne comme un interrupteur de croissance à l’intérieur des cellules. Lorsque YAP1 est trop active, les cellules mammaires normales commencent à se comporter davantage comme des cellules cancéreuses : elles se multiplient plus rapidement, résistent à la mort, réorganisent leur cytosquelette et deviennent plus aptes à envahir les tissus voisins. L’équipe a forcé des cellules mammaires normales à produire davantage de YAP1 et a observé tous ces changements dangereux, ainsi qu’une augmentation de leurs organites productrices d’énergie, les mitochondries. Lorsque les cellules ont été traitées avec des polysaccharides de Lycium barbarum (LBPs), extraits des baies de goji, ces comportements de type cancéreux ont été fortement réduits et les niveaux de YAP1 ont diminué. En d’autres termes, les sucres de la baie pouvaient ramener cet interrupteur de croissance vers la position « off ».
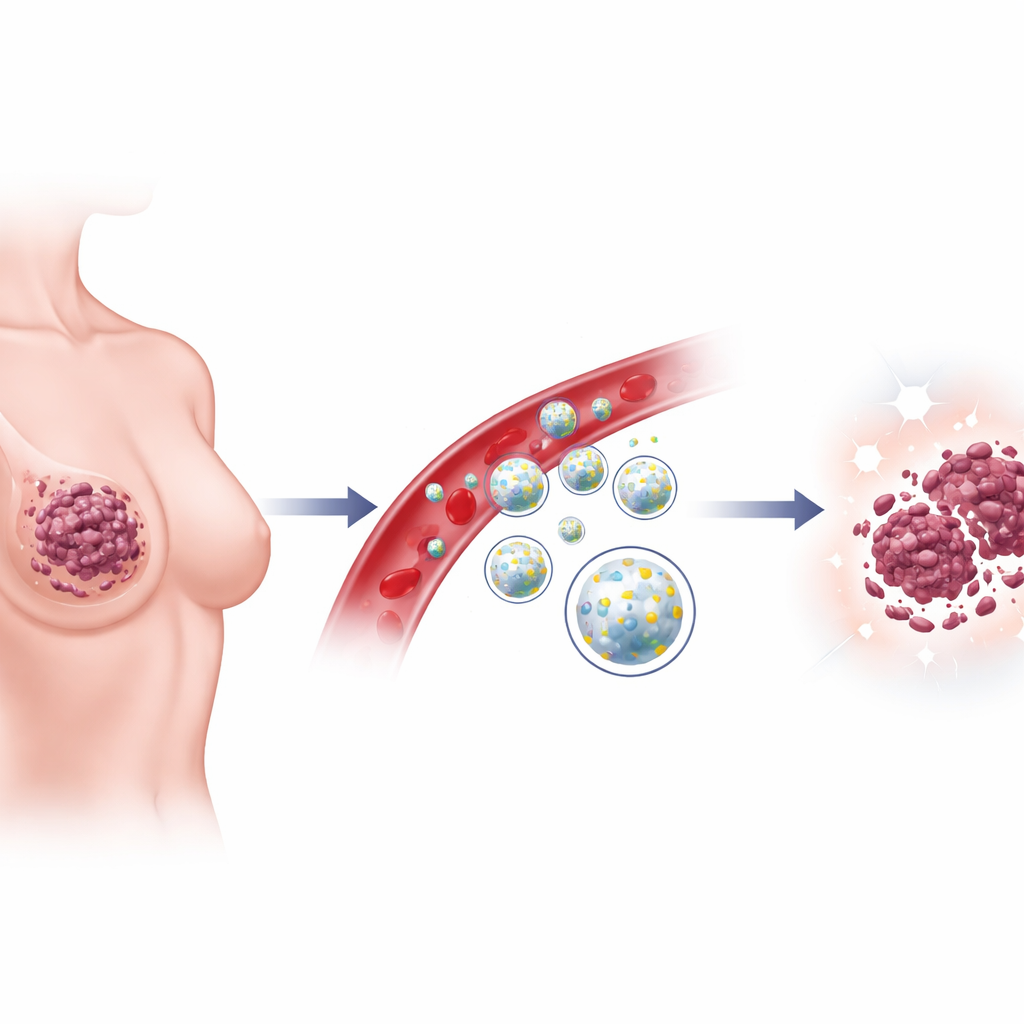
Faire basculer les cellules cancéreuses vers un type particulier de mort
Les scientifiques se sont ensuite intéressés à des cellules de cancer du sein agressives. Là aussi, des niveaux élevés de YAP1 allaient de pair avec une croissance rapide, une forte résistance à la mort cellulaire et une puissante capacité d’invasion. Le traitement par les LBPs a ralenti la division cellulaire, affaibli le échafaudage interne des cellules et réduit l’invasion. Fait important, ces composés ont incité les cellules cancéreuses vers la ferroptose, une forme de mort cellulaire alimentée par le fer et les dommages aux composants lipidiques des membranes cellulaires. Les marqueurs qui protègent normalement contre ce type de mort ont diminué, tandis que les signaux qui la favorisent ont augmenté et que le fer s’est accumulé à l’intérieur des cellules. La réduction de YAP1 par des outils génétiques produisait des effets similaires, et la combinaison de ces outils avec les LBPs renforçait encore l’impact, reliant étroitement l’action des composés de la baie à cet unique interrupteur de croissance.
Concevoir un vecteur de délivrance plus intelligent
Pris seuls, les LBPs ne sont pas des médicaments idéaux : ce sont de grosses molécules hydrophiles qui se dégradent facilement et ne circulent pas efficacement dans l’organisme. Pour surmonter ces limites, les chercheurs les ont encapsulés dans de petites sphères faites d’un plastique biodégradable appelé PLGA, créant des nanoparticules chargées en LBPs (LBPs NPs). Ces particules étaient uniformes en taille, stables en milieu liquide et facilement internalisées par les cellules de cancer du sein, où elles s’accumulaient dans le cytoplasme. Comparée aux LBPs libres, la forme nanoparticulaire ralentissait plus fortement la croissance des cellules cancéreuses, perturbait leur cytosquelette, réduisait l’invasivité et augmentait la proportion de cellules en voie de mort programmée. Les nanoparticules faisaient aussi un meilleur travail pour diminuer YAP1 et son partenaire TAZ, tout en augmentant la forme « éteinte » de YAP1 marquée par phosphorylation.
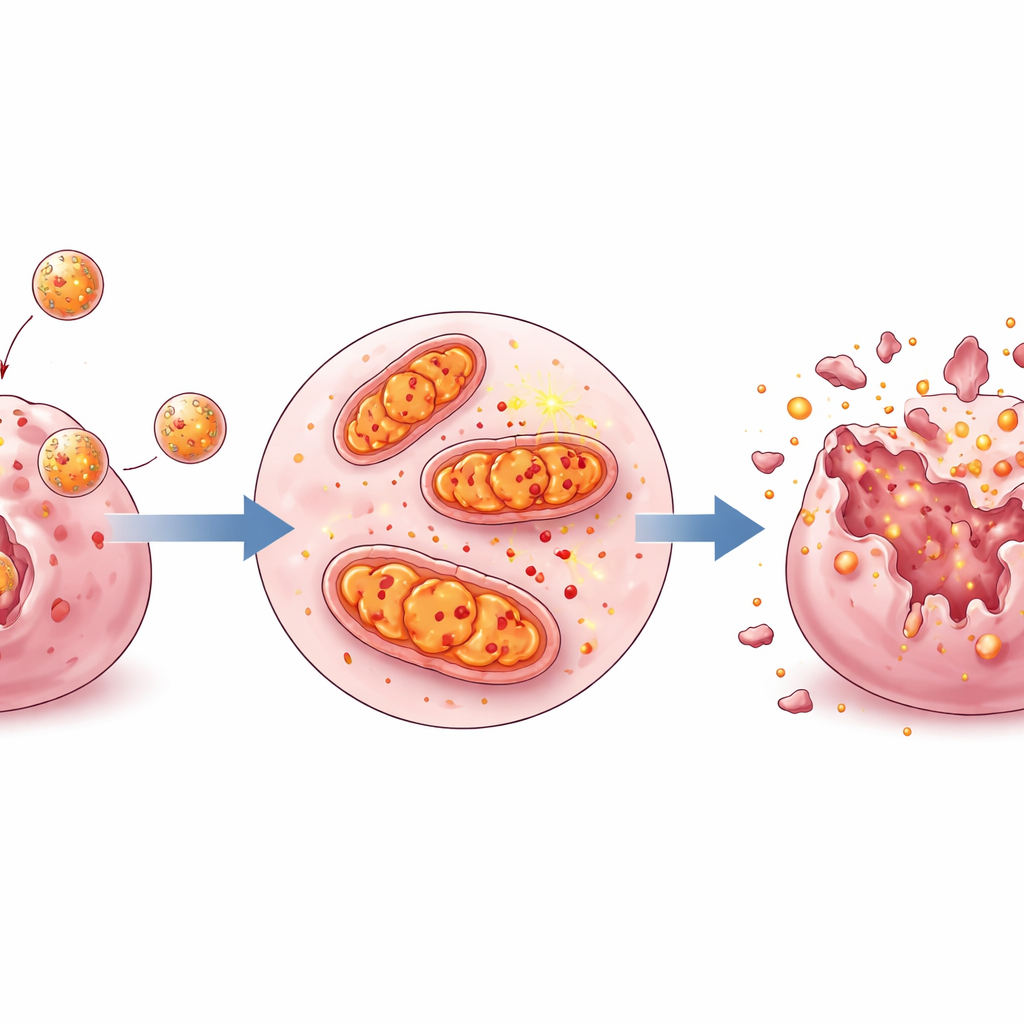
Épuiser l’énergie cellulaire et augmenter le fer
En examinant les cellules cancéreuses traitées, l’équipe a constaté que les LBPs et surtout les LBPs NPs affaiblissaient la fonction mitochondriale et la production d’énergie. Le potentiel de membrane mitochondriale, une mesure clé du bon fonctionnement de ces centrales, a chuté après traitement, et les cellules produisaient moins d’ATP, la monnaie énergétique de base. Parallèlement, des colorants sensibles au fer et des colorations ont montré une accumulation accrue de fer, préparant les cellules à la ferroptose. Les protéines qui protègent normalement les cellules contre ces dommages liés au fer ont diminué, tandis que celles qui les favorisent ont augmenté. Lorsque les chercheurs ont ajouté un bloqueur connu de la ferroptose, ces changements ont été partiellement inversés, confirmant que les nanoparticules induisaient bien cette forme spécifique de mort cellulaire.
Ce que cela pourrait signifier pour les soins futurs
En termes simples, l’étude suggère que des sucres de goji soigneusement conçus et délivrés par nanoparticules peuvent éteindre un moteur de croissance clé dans les cellules mammaires, priver les cellules cancéreuses d’énergie et les pousser vers un effondrement contrôlé alimenté par le fer. Les travaux ont été réalisés sur des cultures cellulaires, non chez l’animal ou le patient, il s’agit donc d’une étape précoce de preuve de concept plutôt que d’un traitement prêt à l’emploi. Néanmoins, cela ouvre la voie à un futur où des composés naturels seraient associés à des systèmes de délivrance intelligents pour désarmer sélectivement la machinerie de croissance du cancer et activer ses programmes d’auto-destruction intégrés.
Citation: Zhao, F., Yang, S., He, T. et al. LBPs NPs suppress breast cancer progression by inhibiting YAP1 expression to induce ferroptosis and alter energy metabolism. Sci Rep 16, 9257 (2026). https://doi.org/10.1038/s41598-025-34454-w
Mots-clés: cancer du sein, nanoparticules, polysaccharides de baie de goji, ferroptose, voie Hippo YAP1