Clear Sky Science · fr
La stabilisation ciblée du facteur inductible par l'hypoxie 1-alpha (HIF1A) pendant la maturation in vitro des complexes cumulus‑ovocyte bovins augmente les taux de blastocystes
Pourquoi ajuster la détection de l'oxygène dans les ovocytes importe
L'élevage bovin moderne repose largement sur des embryons produits en laboratoire, mais le succès est loin d'être garanti : seulement environ un tiers des ovocytes atteignent le stade crucial du blastocyste, moment où ils sont prêts à être transférés dans une vache. Cette étude pose une question apparemment simple mais de large portée pour l'élevage et la reproduction assistée : si l'on reproduit de façon plus fidèle les conditions de faible oxygène vécues naturellement par les ovocytes dans l'ovaire — en renforçant légèrement une protéine clé de détection de l'oxygène — peut‑on aider davantage d'embryons à se développer avec succès ?
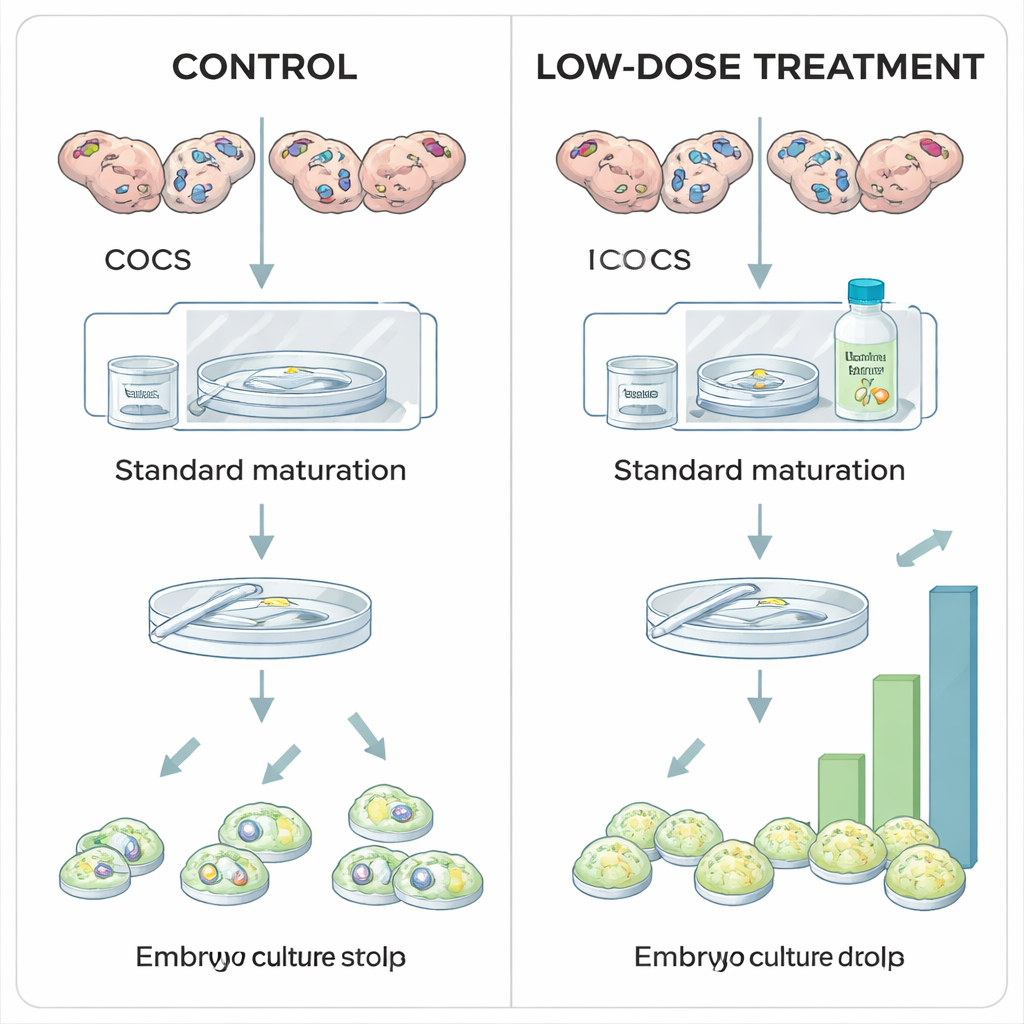
La vie commence dans une niche pauvre en oxygène
Dans l'ovaire, chaque ovocyte en développement est entouré d'un amas de cellules de soutien appelé cumulus, formant ensemble un complexe cumulus‑ovocyte. Bien que l'irrigation sanguine de l'ovaire augmente à mesure que les follicules grandissent, les vaisseaux sanguins ne pénètrent pas jusqu'aux abords immédiats de l'ovocyte. L'oxygène doit diffuser, créant une zone légèrement hypoxique autour de l'ovocyte en maturation. Dans cette niche, un détecteur intracellulaire nommé HIF1A aide les cellules à s'adapter en ajustant le métabolisme et la production hormonale. Des travaux antérieurs ont montré que bloquer HIF1A nuit à la maturation des ovocytes et réduit drastiquement la formation d'embryons, ce qui place cette protéine au centre de la coordination de la compétence ovocytaire — la capacité d'un ovocyte à être fécondé et à se développer en embryon sain.
Utiliser un médicament pour ajuster le détecteur d'oxygène de l'ovocyte
Les chercheurs ont exploré si la stabilisation modérée de HIF1A pendant la maturation in vitro des ovocytes bovins pouvait améliorer les rendements embryonnaires. Dans les protocoles in vitro standards, les complexes cumulus‑ovocyte sont maturés sous des niveaux d'oxygène atmosphérique normaux, principalement pour des raisons pratiques plutôt que biologiques. Ici, des ovocytes prélevés sur des ovaires de boucherie ont été répartis en groupes et exposés pendant leur période de maturation de 24 heures à différentes doses de Roxadustat, un médicament déjà utilisé en médecine humaine pour traiter l'anémie. Le Roxadustat agit en bloquant une famille d'enzymes appelées prolyl‑hydroxylases (PHD) qui marquent normalement HIF1A pour destruction lorsque l'oxygène est abondant. En inhibant les PHD, le Roxadustat permet l'accumulation de la protéine HIF1A même à des niveaux d'oxygène plus élevés, recréant partiellement le signal hypoxique que l'ovocyte percevrait in vivo.
Plus de blastocystes à la bonne dose, effets néfastes à des doses élevées
Lorsque l'équipe a examiné l'issue des ovocytes et des embryons après traitement, un schéma clair est apparu. Une faible dose de Roxadustat (25 micromolaire) n'a pas modifié le nombre d'ovocytes ayant terminé la maturation ni le nombre d'ovocytes fécondés ayant commencé la division, mais elle a augmenté de manière significative la proportion atteignant le stade blastocyste. Autrement dit, les premières étapes n'étaient pas affectées, et pourtant davantage d'embryons ont réussi à compléter le parcours exigeant menant au blastocyste — ce qui suggère qu'une stabilisation modeste de HIF1A améliore la qualité intrinsèque de l'ovocyte. En revanche, la dose la plus élevée (100 micromolaire) a réduit le pourcentage d'ovocytes parvenant à maturité, et lorsque le même inhibiteur a été appliqué plus tard, durant la culture embryonnaire de huit jours, les fortes doses ont fortement réduit la formation de blastocystes sans altérer la division cellulaire précoce. Ces résultats indiquent qu'une activité de HIF1A « juste suffisante » pendant la maturation est bénéfique, tandis qu'une activation trop importante ou trop prolongée est délétère.
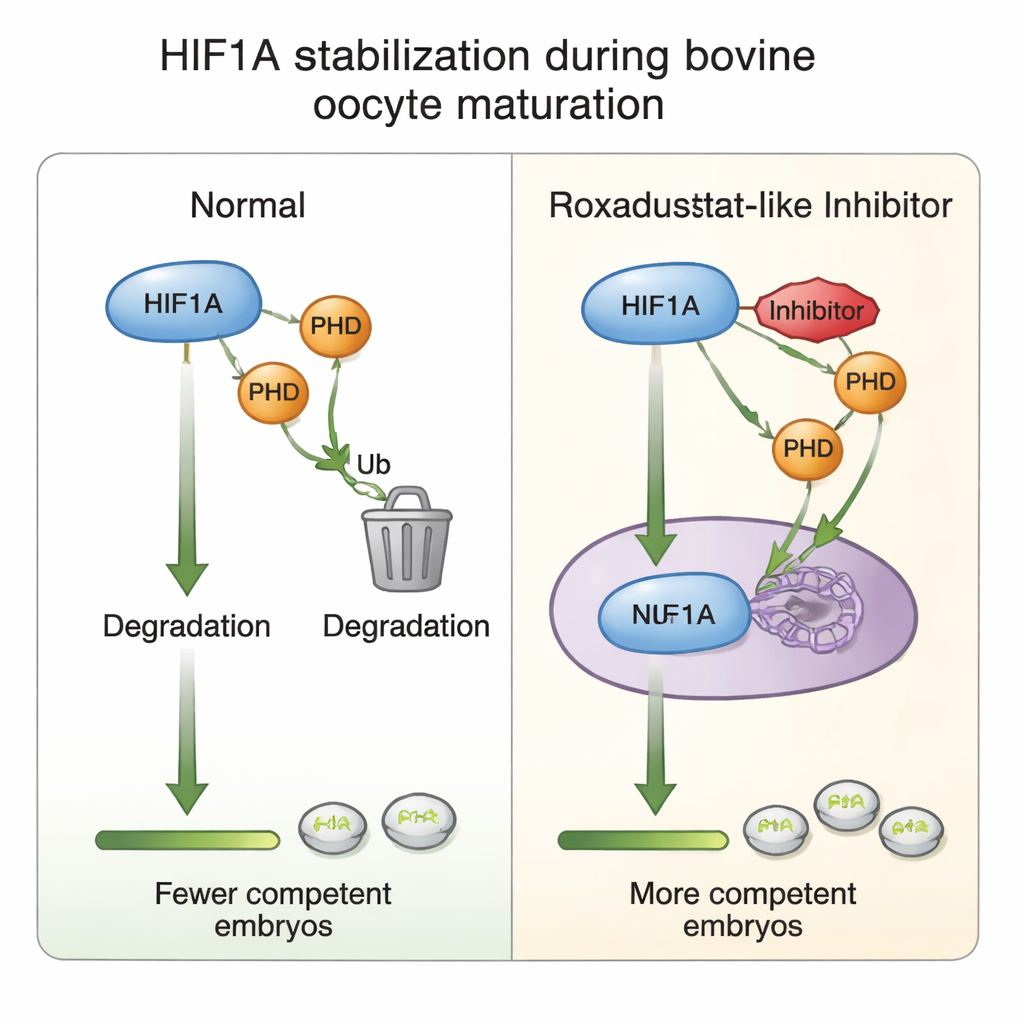
Que se passe‑t‑il dans les cellules de soutien de l'ovocyte
Pour comprendre comment fonctionne cet ajustement chimique, les auteurs ont sondé les cellules du cumulus qui entourent chaque ovocyte. Ils ont constaté que la maturation augmente en général l'activité du gène HIF1A, mais l'ajout de Roxadustat diminuait paradoxalement l'ARN messager de HIF1A tout en maintenant les niveaux de protéine HIF1A — indice que les cellules peuvent réduire la production génétique une fois la protéine suffisamment stabilisée, une sorte de frein intégré contre la suractivation. Les niveaux de PHD2, l'une des PHD la plus sensible à l'oxygène, ont augmenté en réponse au médicament, renforçant son rôle dans la boucle de détection de l'oxygène. À des doses plus élevées, des marqueurs de prolifération cellulaire et de la matrice adhésive qui permet l'expansion des cellules du cumulus autour de l'ovocyte ont été réduits, en accord avec le déclin observé de la maturation et de la formation embryonnaire. Tout cela soutient l'idée qu'une activité de HIF1A finement équilibrée règle le dialogue entre l'ovocyte et les cellules du cumulus, dialogue qui sous‑tend le succès du développement ultérieur.
Implications pour l'élevage et au‑delà
Ce travail montre que la stabilisation douce du détecteur d'oxygène de l'ovocyte pendant la courte fenêtre de maturation in vitro peut augmenter de manière significative et stabiliser les rendements en blastocystes chez le bovin, sans modifier la fécondation ni la clivage précoce. En termes pratiques, cela pourrait se traduire par une production d'embryons plus fiable pour les programmes d'élevage, en utilisant un médicament ciblé plutôt que des modifications grossières du taux d'oxygène ou des produits chimiques plus toxiques. L'étude souligne également une leçon plus large, pertinente pour les traitements de la fertilité humaine : reproduire l'environnement nuancé et pauvre en oxygène de l'ovaire ne se résume pas à augmenter ou diminuer l'oxygène, mais à respecter l'équilibre délicat des molécules de signalisation comme HIF1A. Ajuster finement cet équilibre, plutôt que de le pousser à l'extrême, pourrait être une voie clé vers des embryons en meilleure santé.
Citation: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Mots-clés: production d'embryons in vitro, maturation des ovocytes, signalisation hypoxique, stabilisation de HIF1A, reproduction bovine