Clear Sky Science · fr
Vers des jumeaux numériques en électrophysiologie cardiaque avec un solveur évolutif, open source et efficace sur grappes GPU
Pourquoi construire des cœurs virtuels est important
Quand les médecins traitent des troubles du rythme cardiaque, ils travaillent souvent en partie à l’aveugle : ils peuvent mesurer des signaux électriques à la surface du corps mais ne voient pas facilement comment ces signaux se propagent profondément dans le cœur. Cette étude décrit de nouveaux outils informatiques puissants capables de simuler en détail le battement du cœur d’une personne, suffisamment rapidement pour explorer de nombreux scénarios « et si ». En combinant une anatomie cardiaque réaliste avec des processeurs graphiques de pointe, les auteurs nous rapprochent d’expériences virtuelles sûres et peu coûteuses sur des copies numériques des cœurs de patients individuels.
Des modèles simples aux jumeaux numériques
Les simulations cardiaques modernes peuvent représenter l’activité depuis le niveau des cellules individuelles jusqu’à l’organe entier, mais reproduire fidèlement la propagation de l’électricité dans le cœur est à la fois mathématiquement complexe et coûteux en calcul. Un objectif clé pour la médecine est le « jumeau numérique cardiaque » : un modèle informatique personnalisé qui reflète le cœur d’un patient donné et peut être utilisé pour tester des médicaments, des dispositifs ou des stratégies de stimulation avant leur usage clinique. Pour rendre cela réalisable, le logiciel qui exécute ces simulations doit être à la fois rapide et précis, inclure des structures anatomiques importantes, et être disponible en open source afin que des chercheurs du monde entier puissent le vérifier, l’améliorer et le réutiliser.
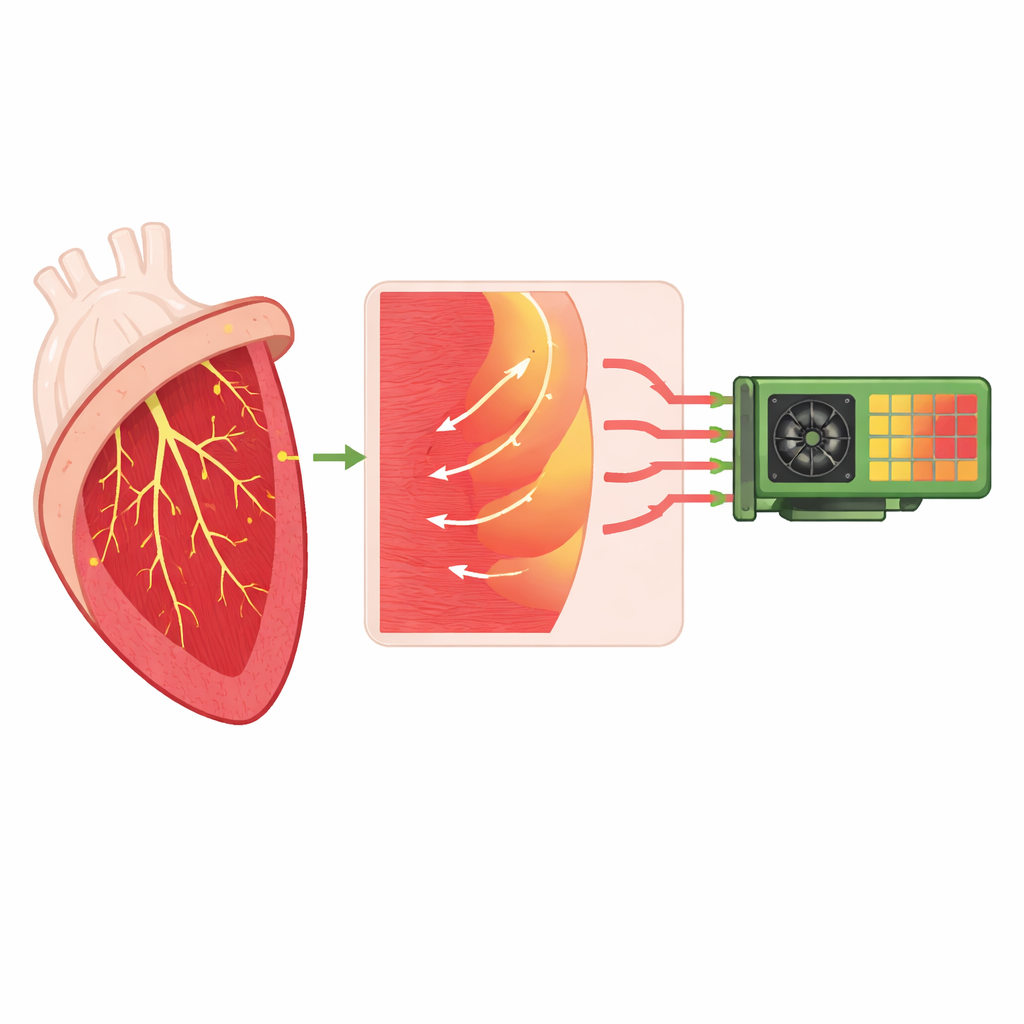
Capturer le câblage caché du cœur
Le travail se concentre sur un simulateur open source appelé monoalg3d, qui modélise la façon dont les signaux électriques se propagent à travers le muscle cardiaque et son réseau de conduction spécialisé. Ce réseau, connu sous le nom de système de Purkinje, délivre rapidement le signal déclencheur du battement depuis les voies de conduction supérieures vers de nombreux points de connexion minces répartis à la surface interne des ventricules. À chacun de ces jonctions, une fibre de Purkinje fine doit exciter une masse bien plus importante de muscle cardiaque, introduisant un retard naturel et, dans certaines conditions, un risque de blocage ou de conduction anormale. Les auteurs améliorent monoalg3d pour représenter ce câblage et ses jonctions de façon plus réaliste, y compris l’asymétrie entre les signaux allant de Purkinje vers le muscle et ceux revenant du muscle vers le réseau.
Transformer supercalculateurs et GPU en laboratoires cardiaques
Pour exécuter de tels modèles détaillés rapidement, l’équipe réingénie l’utilisation du matériel par le simulateur. Ils repensent le noyau numérique de sorte que la dynamique locale des cellules et la propagation de la tension à travers le cœur soient résolues directement sur des unités de traitement graphique (GPU), des dispositifs initialement conçus pour le rendu d’images mais désormais largement utilisés pour le calcul scientifique. En organisant soigneusement les données pour les bibliothèques GPU et en évitant les transferts fréquents entre CPU et GPU, ils montrent qu’une configuration entièrement basée sur GPU peut accélérer un banc d’essai standard d’un facteur proche de onze par rapport à une version traditionnelle ne s’appuyant que sur le CPU. Ils introduisent aussi un nouveau format de sortie compact pour réduire drastiquement les besoins de stockage et une fonction d’échange de messages qui peut lancer des centaines de simulations en parallèle sur un supercalculateur, chacune explorant un ensemble différent de paramètres physiologiques.
Apprendre aux cœurs virtuels à correspondre aux patients réels
Au-delà de la simple vitesse, les auteurs testent si leur solveur amélioré peut soutenir des simulations réalistes spécifiques à un patient. En utilisant une reconstruction tridimensionnelle d’un cœur humain issue d’imagerie médicale, ils attachent un réseau de Purkinje synthétique et ajustent des paramètres clés des jonctions : la résistance à chaque connexion et combien de régions musculaires voisines chaque terminal de Purkinje excite. Ils parcourent automatiquement des centaines de combinaisons de ces valeurs, exécutant des simulations démarrées par un stimulus dans le faisceau de conduction principal, et mesurent à la fois les petits retards à chaque jonction et les signaux électrocardiographiques (ECG) résultants sur la poitrine. Pour un maillage cardiaque à haute résolution, ils identifient des choix de paramètres qui produisent des temps d’activation physiologiquement plausibles et des formes d’onde ECG corrélées avec les enregistrements d’un patient réel, tout en maintenant les temps de simulation individuels à quelques heures même lorsque 512 exécutions sont lancées simultanément.
Beaucoup de cœurs possibles qui se ressemblent de l’extérieur
Un résultat intrigant est que différentes configurations internes du câblage et différentes forces de jonction peuvent conduire à des ECG très similaires à la surface du corps. Autrement dit, plusieurs cœurs numériques distincts peuvent sembler également compatibles avec les mêmes données cliniques. Les auteurs montrent que certaines jonctions de Purkinje sont particulièrement influentes, leurs délais locaux variant fortement entre des simulations tout aussi bien ajustées, tandis que le calendrier global d’activation des ventricules reste stable. Cette non-unicité suggère que les futurs cadres de jumeau numérique devront intégrer des données ou des contraintes supplémentaires — comme une imagerie plus détaillée ou des mesures invasives — pour identifier une configuration interne la plus vraisemblable pour un patient donné.
Ce que cela signifie pour les soins futurs
En résumé, cette étude fournit un simulateur accéléré par GPU, librement disponible, capable de gérer une anatomie cardiaque détaillée, un câblage de conduction réaliste et de grands lots de simulations personnalisées sur des grappes de calcul modernes. Pour les non-spécialistes, le message clé est qu’il devient pratique d’exécuter rapidement des expériences virtuelles de haute fidélité qui ressemblent à des patients individuels, incluant de subtils retards aux jonctions du câblage interne du cœur. Bien que des travaux supplémentaires soient nécessaires pour personnaliser pleinement ces modèles et lever les incertitudes internes, les outils présentés ici constituent un bloc de construction important pour de futurs diagnostics, évaluations de risque et plans thérapeutiques basés sur des jumeaux numériques en cardiologie.
Citation: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
Mots-clés: jumeau numérique cardiaque, simulation de l’électrophysiologie cardiaque, système de conduction de Purkinje, calcul GPU, cardiologie personnalisée