Clear Sky Science · fr
Visualisation in vivo de la dynamique extracellulaire de l’adénosine cardiaque et de sa modulation pharmacologique dans des modèles de insuffisance cardiaque chez le poisson zèbre
Pourquoi cette histoire de cœur de poisson compte
L’insuffisance cardiaque reste l’une des principales causes de mortalité dans le monde, et de nombreux patients s’aggravent malgré les meilleurs traitements disponibles. Les scientifiques savent que les cellules cardiaques stressées libèrent des « signaux de détresse » chimiques dans leur environnement, mais il a été difficile d’observer ces signaux en action à l’intérieur d’un cœur battant. Cette étude utilise des poissons zèbres transparents, dont les petits cœurs reproduisent fidèlement des caractéristiques clés des cœurs humains, pour suivre ces signaux de danger en temps réel et tester une nouvelle manière de les atténuer.
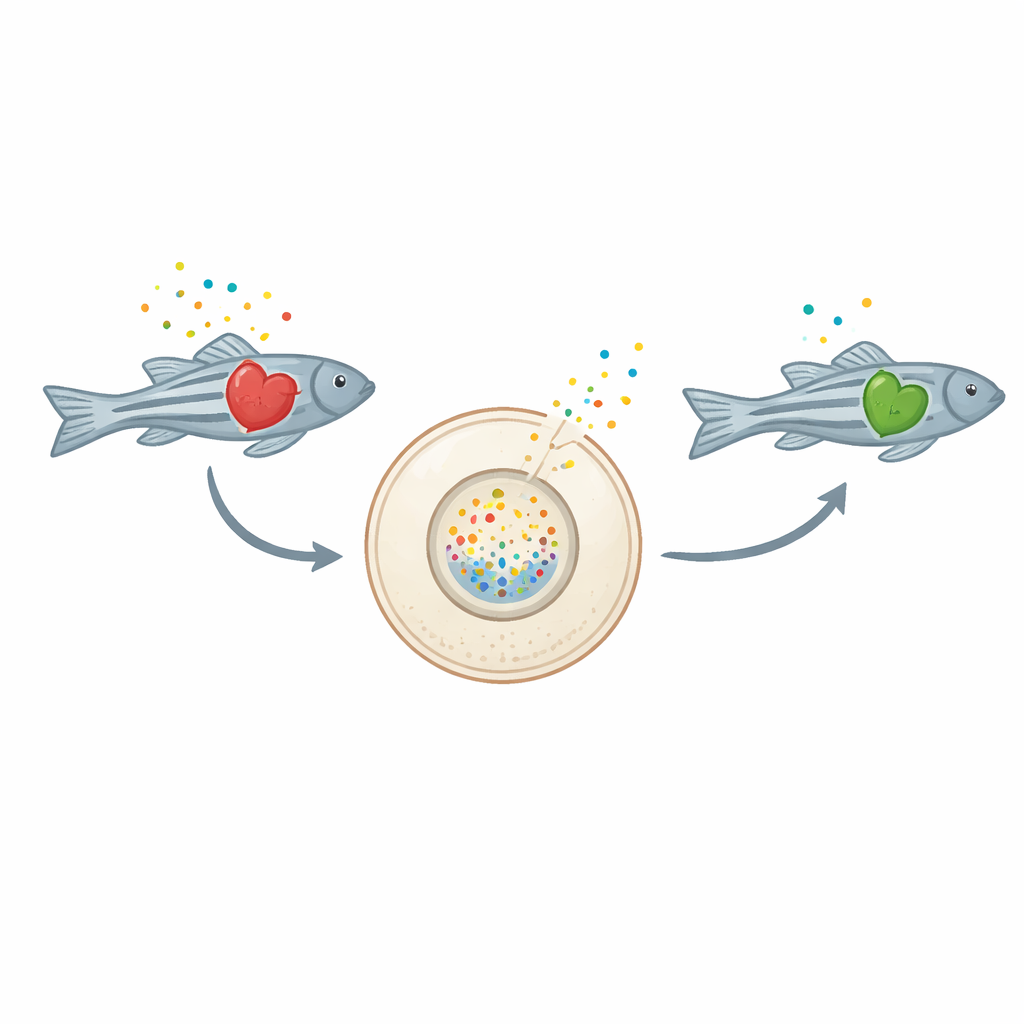
Des signaux d’un cœur en détresse
Lorsque les cellules cardiaques sont endommagées, elles libèrent des molécules porteuses d’énergie comme l’ATP et son produit de dégradation, l’adénosine, dans l’espace extracellulaire. Hors de la cellule, ces mêmes molécules cessent de jouer leur rôle énergétique et se comportent plutôt comme des messages urgents qui peuvent attiser l’inflammation. Dans l’insuffisance cardiaque chronique, cette réponse inflammatoire peut devenir excessive et endommager davantage le cœur. Jusqu’à présent, les chercheurs manquaient de preuves directes, in vivo, montrant comment ces molécules évoluent au fil du temps dans un cœur en défaillance.
Transformer le poisson zèbre en caméra chimique vivante
L’équipe a modifié génétiquement des poissons zèbres dont les cellules cardiaques expriment à leur surface une protéine capteur fluorescente spéciale appelée GRABAdo. Lorsque l’adénosine s’accumule à l’extérieur des cellules, ce capteur s’illumine en vert, transformant ainsi chaque petit cœur en sa propre caméra chimique en direct. Les chercheurs ont ensuite déclenché une insuffisance cardiaque chez les poissons par l’administration de térfénadine, un médicament connu pour perturber le rythme cardiaque et affaiblir la contraction. Au fur et à mesure que les poissons présentaient des signes nets d’insuffisance cardiaque — battements plus lents, ventricules dilatés et affaiblis, œdème autour du cœur et diminution de la performance de nage — leurs capteurs cardiaques se sont illuminés, révélant une augmentation marquée de l’adénosine extracellulaire. Des mesures chimiques réalisées sur des larves entières ont confirmé que les niveaux totaux d’adénosine étaient plus élevés dans les cœurs en défaillance.
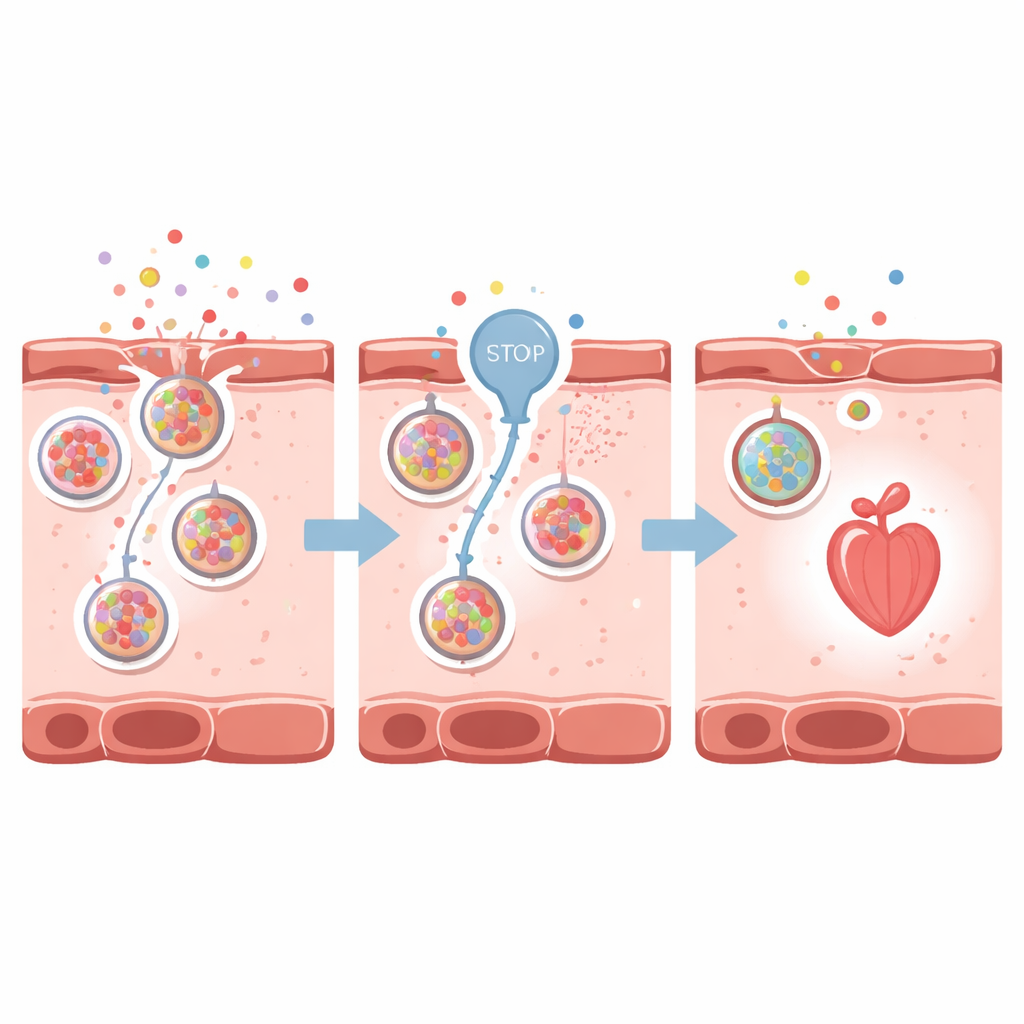
Bloquer la soupape de libération
Les scientifiques se sont ensuite demandé si atténuer ces signaux de danger pouvait protéger le cœur. Ils se sont concentrés sur VNUT, un transporteur qui charge l’ATP dans de petites vésicules cellulaires en vue de sa libération hors de la cellule. En utilisant le clodronate, un médicament qui bloque VNUT, ils ont réduit la libération d’ATP et, indirectement, l’accumulation d’adénosine autour des cellules cardiaques. Chez les poissons zèbres présentant une insuffisance cardiaque induite par un médicament, l’inhibition de VNUT a préservé la morphologie cardiaque, limité la dilatation des cavités, amélioré la fréquence et la force de contraction et maintenu un meilleur débit sanguin. Le capteur fluorescent de l’adénosine s’est affaibli, indiquant une réduction du signal de détresse extracellulaire. Des effets protecteurs similaires ont été observés chez des poissons zèbres adultes atteints d’une forme aiguë et rapidement évolutive d’insuffisance cardiaque.
Plusieurs leviers protecteurs qui agissent ensemble
L’insuffisance cardiaque implique plusieurs voies, aussi les chercheurs ont-ils testé comment le blocage de VNUT interagit avec d’autres acteurs connus. Des médicaments bloquant certains récepteurs de l’adénosine et des récepteurs de l’ATP, ainsi qu’un composé limitant la fuite passive d’ATP via des canaux membranaires, ont chacun amélioré la fonction cardiaque chez le poisson zèbre. Associés à l’inhibition de VNUT, nombre de ces traitements ont produit des bénéfices additifs, suggérant que réduire la signalisation des purines à plusieurs niveaux peut être particulièrement efficace. L’inhibition de VNUT a également contribué à rétablir l’équilibre calcique dans les cellules cardiaques, essentiel au battement normal, et a réduit à la fois la mort cellulaire et l’activité de gènes liés à l’inflammation. Ensemble, ces résultats présentent VNUT comme un interrupteur central liant la libération d’ATP, l’inflammation, la perturbation du contrôle calcique et la progression des lésions cardiaques.
Du bac à poissons aux thérapies futures
Pour le grand public, le message clé est que l’étude visualise directement la montée d’un signal chimique de stress dans les cœurs en défaillance et montre que bloquer sa libération peut préserver la fonction cardiaque chez un animal vivant. Bien que les cœurs de poisson zèbre soient plus simples que les cœurs humains, ils partagent suffisamment de mécanismes biologiques pour constituer un banc d’essai puissant pour de nouvelles idées. En révélant VNUT comme une cible prometteuse au carrefour de l’inflammation et de l’instabilité électrique, ce travail suggère que les futures thérapies de l’insuffisance cardiaque pourraient faire plus que soutenir le débit sanguin — elles pourraient calmer activement les conversations cellulaires nuisibles qui poussent le cœur vers la défaillance.
Citation: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Mots-clés: insuffisance cardiaque, signalisation de l’adénosine, modèle de poisson zèbre, inflammation, protection cardiaque