Clear Sky Science · fr
Intermédiaires télomériques en G-quadruplex révélés par une analyse avancée de réseau de Markov
Nœuds cachés aux extrémités de notre ADN
Aux extrémités de nos chromosomes se trouvent des capuchons protecteurs appelés télomères, souvent comparés aux embouts en plastique des lacets. Dans ces régions, l’ADN peut se replier en structures inhabituelles à quatre brins appelées G-quadruplexes. Ces petites architectures peuvent influencer le comportement des gènes et la façon dont les cellules vieillissent ou deviennent cancéreuses. Cette étude examine en coulisses la façon dont l’un de ces nœuds se défait progressivement, en utilisant des simulations informatiques détaillées et des analyses de données avancées pour révéler des conformations éphémères presque impossibles à capturer expérimentalement.
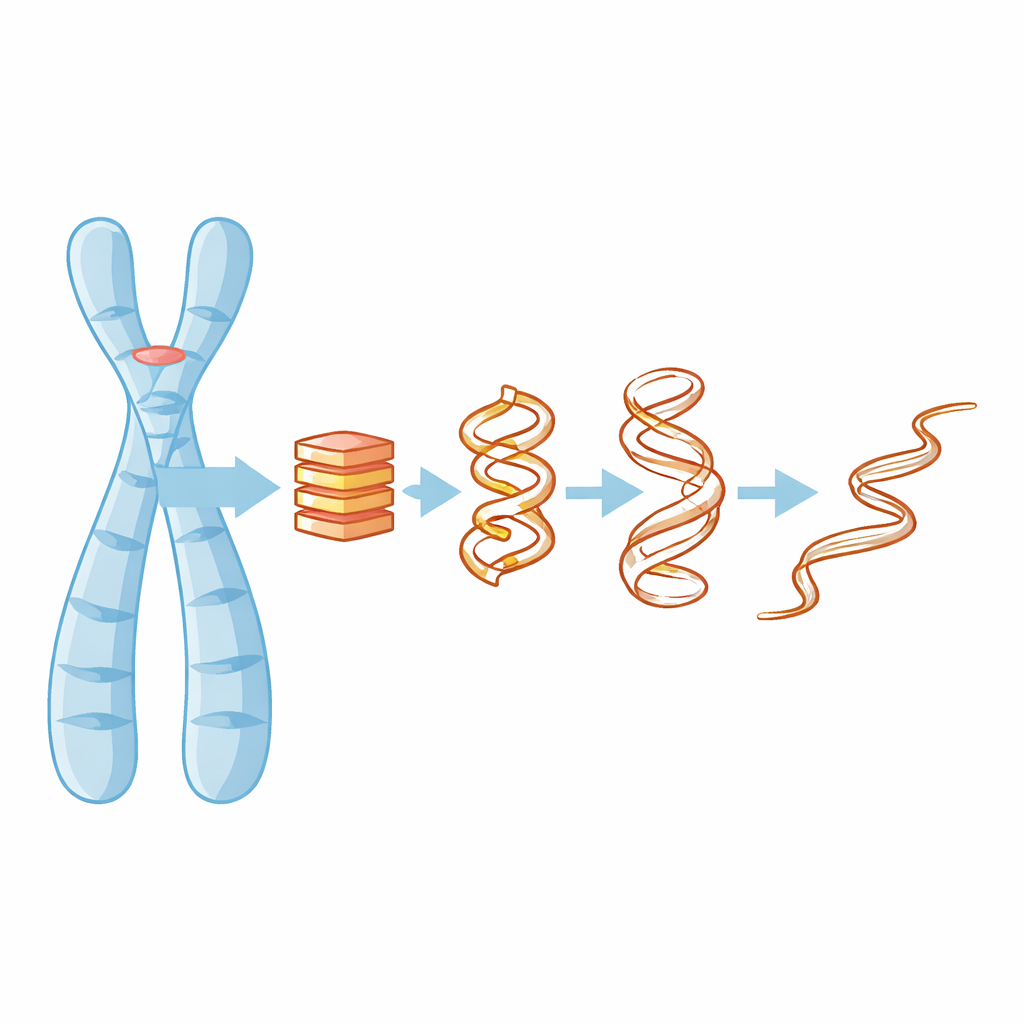
Pourquoi les nœuds d’ADN à quatre brins ont de l’importance
La plupart d’entre nous apprennent que l’ADN est une double hélice, mais dans les régions riches en guanine — comme celles des télomères — la molécule peut se plier en empilements compacts à quatre brins appelés G-quadruplexes. Ces empilements sont maintenus par des couches planes de bases guanine et de petits ions positifs, comme le potassium, qui se logent au centre et contribuent à lier l’ensemble. Quand un G-quadruplex se forme ou se défait, il peut masquer ou exposer des portions du génome, affectant l’activité des gènes, la réplication de l’ADN et même la manière dont les cellules cancéreuses entretiennent leurs télomères. Comprendre comment ces structures perdent leur conformation est donc essentiel pour savoir comment les cibler par des médicaments ou prédire quand elles peuvent céder.
Observer un nœud moléculaire se défaire
Les chercheurs se sont concentrés sur un G-quadruplex télomérique humain dans lequel quatre segments d’un seul brin d’ADN s’alignent en parallèle et s’empilent en une colonne compacte. Ils ont utilisé des simulations de dynamique moléculaire tout atome — des expériences virtuelles qui suivent le mouvement de chaque atome — pour chauffer huit copies de cette structure à des températures proches de son point de fusion. Pour aider le système à explorer différentes conformations, ils ont utilisé une stratégie appelée replica exchange, où des simulations à différentes températures échangent occasionnellement leurs configurations. Dans sept des huit cas, le G-quadruplex est resté stable ; dans un seul, il s’est complètement déroulé. Cet événement d’effondrement rare est devenu une étude de cas détaillée, montrant non seulement l’avant et l’après, mais toute une séquence de formes intermédiaires le long du processus.
Le rôle crucial des petits ions
Une conclusion centrale est que les petits ions à l’intérieur du G-quadruplex jouent le rôle de pivot. Tant qu’au moins un ion reste niché entre les couches de guanine, la structure reste globalement intacte, peut‑être un peu relâchée mais encore reconnaissable. Lorsque les deux ions finissent par quitter le canal central, en revanche, l’empilement se déstabilise rapidement. Les couches de guanine se déforment, des brins individuels se détachent, et l’ensemble de la molécule d’ADN devient plus étiré et flexible. D’autres molécules simulées qui n’ont perdu qu’un ion ont adopté des états instables mais encore partiellement ordonnés, ce qui suggère que le déroulement complet exige la perte des deux ions stabilisants — un indice expliquant pourquoi certains G-quadruplexes sont si résistants dans la cellule.
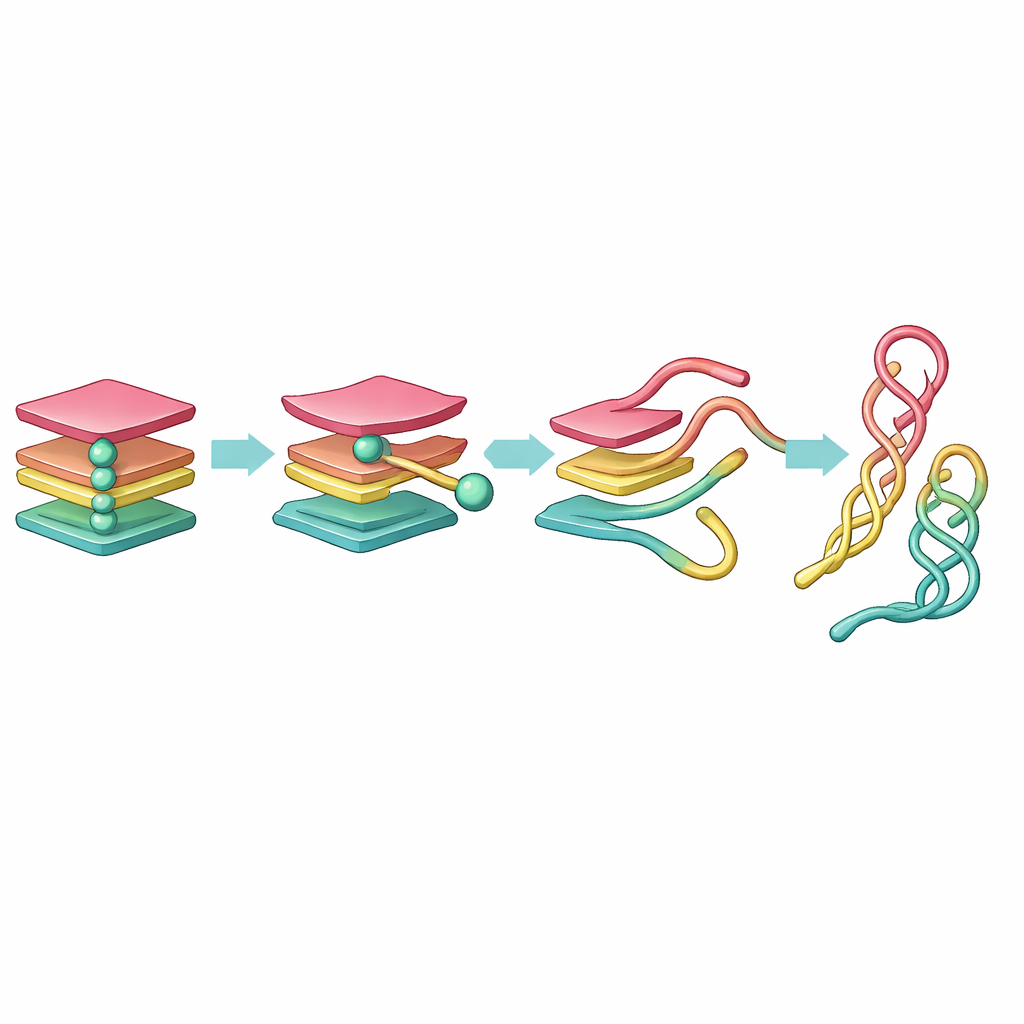
Découvrir des étapes cachées du parcours
Les simulations brutes ont produit une quantité gigantesque de données, bien trop complexe pour être interprétée à l’œil nu. Pour maîtriser cela, l’équipe a d’abord simplifié l’ADN en représentant chaque base par une seule bille, puis a utilisé des outils mathématiques pour réduire le mouvement à quelques coordonnées clés. Ils ont appliqué deux méthodes : l’analyse en composantes principales (PCA), qui met en évidence les directions de mouvement les plus importantes, et l’analyse en composantes indépendantes temporelles (tICA), qui filtre les changements lents et durables marquant de véritables transitions structurelles. À partir de ces coordonnées réduites, ils ont construit des réseaux conformations de Markov, où chaque nœud représente une forme typique de l’ADN et les liens montrent comment la molécule saute d’une conformation à une autre.
Un trajet privilégié du nœud vers le brin lâche
Cette vue en réseau a révélé une voie claire de déroulement. À partir d’un G-quadruplex complètement replié, un brin se détache d’abord, formant un état « triplex » à trois brins. Ce triplex se réorganise ensuite en un « hairpin » à deux brins et un ensemble de brins lâches voisins. Le hairpin et une configuration apparentée en « cross-hairpin » s’avèrent étonnamment durables, agissant comme des étapes stables sur le trajet du nœud serré vers une configuration d’ADN plus relâchée. Alors que la PCA morcellait cette progression en de nombreux états à l’apparence similaire, la tICA l’a distillée en un petit nombre d’étapes distinctes et d’importance cinétique, montrant que les formes de type triplex sont de courte durée, tandis que les formes de type hairpin persistent beaucoup plus longtemps.
Ce que cela implique pour la biologie et la médecine
Pour un non-spécialiste, le message clé est que les G-quadruplexes télomériques ne passent pas simplement d’un état plié à un état déroulé. Ils fondent plutôt à travers une série de conformations de durées variables, les petits ions agissant comme des gardiens de la stabilité. Les simulations suggèrent que les intermédiaires à trois brins sont fugitifs, tandis que les hairpins à deux brins et les formes en croix sont des points d’arrêt plus stables. Parce que ces états intermédiaires peuvent aussi apparaître dans la direction inverse, celle du repliement, ils sont probablement cruciaux pour la formation, la conversion et les interactions des G-quadruplexes avec de potentiels médicaments. Cartographier ce paysage caché de conformations rapproche les scientifiques de la conception de molécules capables de stabiliser ou de déstabiliser sélectivement ces nœuds d’ADN dans la lutte contre le cancer et d’autres maladies.
Citation: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Mots-clés: G-quadruplex, ADN télomérique, dynamique moléculaire, repliement de l’ADN sans protéines, thérapeutiques anticancéreuses