Clear Sky Science · fr
Intégration génomique fonctionnelle des réseaux de gènes liés à la glycolyse révèle des biomarqueurs pronostiques et la régulation du microenvironnement immunitaire dans le cancer du sein
Pourquoi les tumeurs « consommatrices de sucre » comptent pour les patientes
Les cellules du cancer du sein brûlent souvent le sucre d’une façon inhabituelle, même lorsque l’oxygène est abondant. Cet usage énergétique altéré, connu sous le nom de glycolyse, ne se contente pas d’alimenter la croissance tumorale : il peut remodeler les cellules immunitaires qui entourent la tumeur et influencer le pronostic des patientes. Cette étude combine de vastes bases de données génétiques, des mesures en cellule unique et des modèles informatiques pour montrer comment des tumeurs mammaires avides de sucre sont associées à des paysages immunitaires distincts, à des différences de survie et à de nouvelles pistes thérapeutiques potentielles.
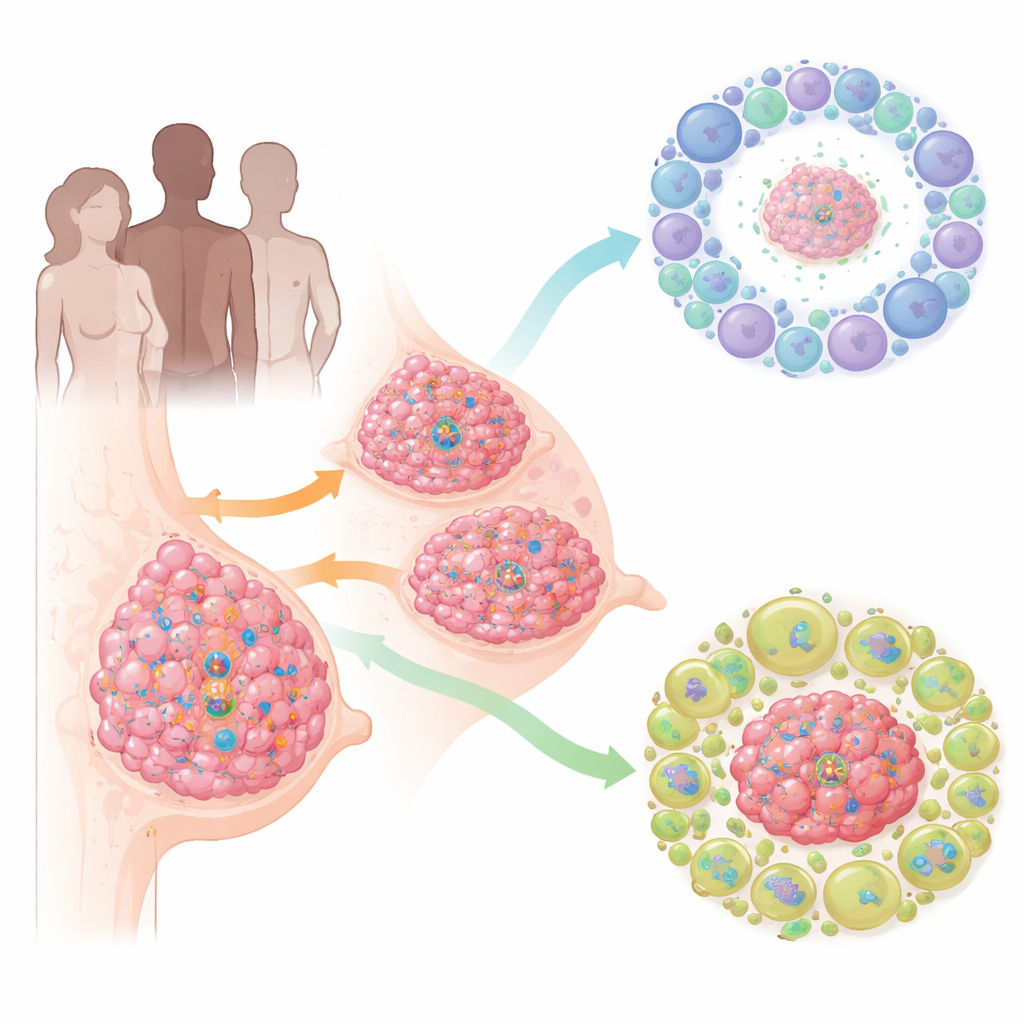
Observer les tumeurs à travers de multiples jeux de données
Les chercheurs ont commencé par rassembler plusieurs types de données provenant de milliers de femmes atteintes de cancer du sein. Ils ont utilisé des profils tumoraux globaux issus de grands consortiums (TCGA et METABRIC), des séquençages ARN en cellule unique détaillés à partir d’échantillons de patientes, et des études génétiques reliant des variants d’ADN à des changements d’activité génique. À partir de ces sources, ils ont constitué une liste de plus de quatre mille gènes impliqués dans la glycolyse, puis l’ont réduite à quelques centaines de gènes à la fois altérés dans les tumeurs et fortement liés à la biologie du cancer du sein. Grâce à l’apprentissage automatique, ils ont construit un « score de glycolyse » à 16 gènes calculable pour chaque tumeur.
Groupes de risque définis par l’utilisation du sucre par la tumeur
Lorsque les patientes ont été séparées en groupes à score élevé et faible, des différences nettes de résultat sont apparues. Les tumeurs avec un score de glycolyse élevé étaient plus susceptibles de présenter de nombreuses mutations, des signes de division cellulaire rapide et d’être associées à une survie globale plus mauvaise. Ce schéma était particulièrement marqué dans les cancers hormonodépendants (Luminal A et B) et les cancers triple négatifs, où des scores élevés signalaient des patientes avec des durées de survie nettement plus courtes. En combinant le score de glycolyse avec des informations cliniques de base comme l’âge et le stade, l’équipe a créé un graphique facile à lire, appelé nomogramme, qui estimait de façon plus précise qu’avant la probabilité de survie à un, trois ou cinq ans.
Quartiers immunitaires façonnés par le métabolisme tumoral
L’étude s’est ensuite intéressée à la façon dont ce signature métabolique se rapporte au « quartier » immunitaire entourant les tumeurs. En utilisant des algorithmes qui infèrent les cellules immunitaires présentes dans des échantillons en vrac, les tumeurs à score élevé se sont avérées riches en macrophages de type M2 et en autres cellules associées à l’immunosuppression et à l’inflammation chronique, tandis qu’elles contenaient moins de lymphocytes T CD8 cytotoxiques et de cellules dendritiques présentatrices d’antigène. En revanche, les tumeurs à score faible semblaient évoluer dans un environnement immunitaire plus « chaud », avec davantage de lymphocytes T tueurs actifs et de lymphocytes B utiles. Le séquençage en cellule unique a confirmé que, au sein du tissu tumoral, certaines cellules immunitaires — en particulier les cellules myéloïdes et les lymphocytes T — présentaient elles-mêmes une activité glycolytique plus élevée, suggérant que l’état métabolique de la tumeur et le comportement des cellules immunitaires sont étroitement liés.
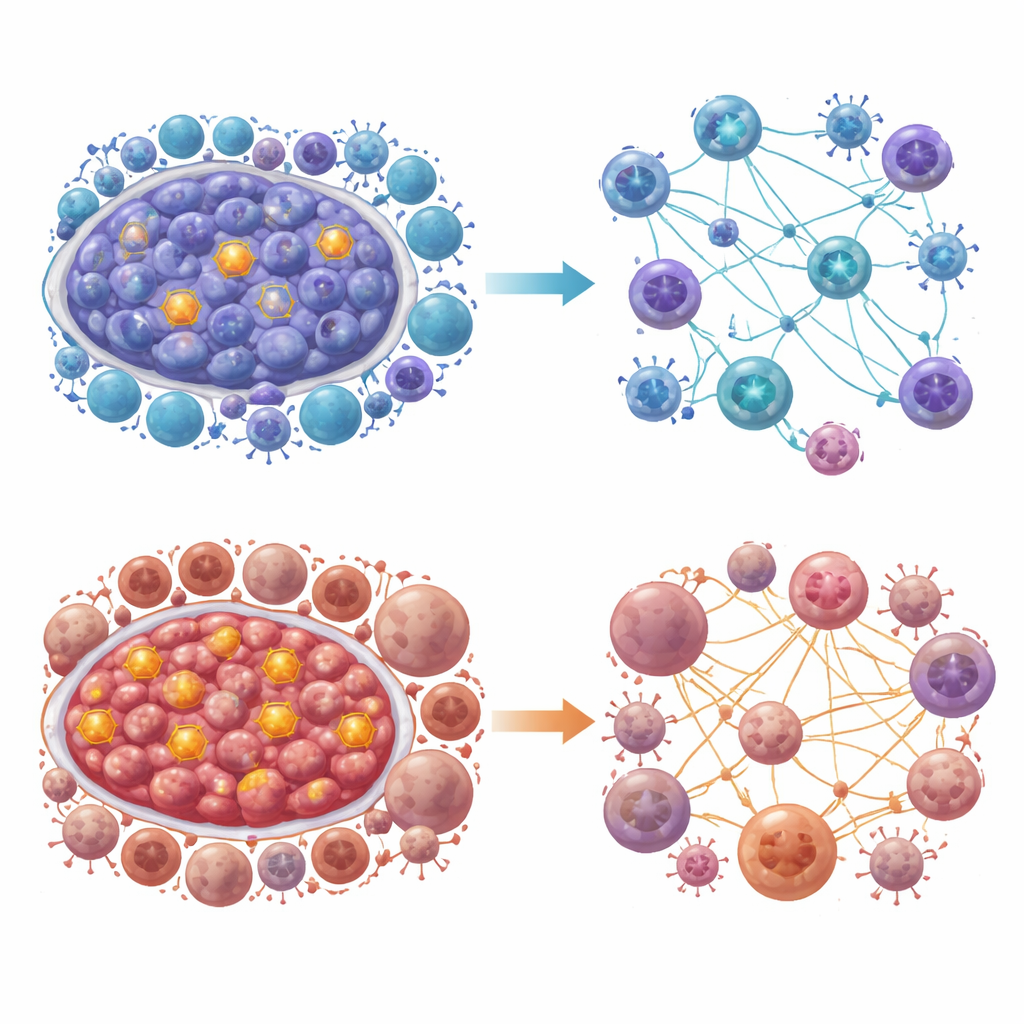
Signaux intercellulaires et gènes clés protecteurs ou à risque
En zoomant davantage, l’équipe a cartographié la communication entre différents types cellulaires via des molécules de signalisation. Les cellules myéloïdes à glycolyse élevée utilisaient fortement des voies comme le MHC-II, MIF et SPP1 pour communiquer, tandis que les lymphocytes T privilégiaient les signaux MHC-I, CCL et CXCL. Ces schémas différaient selon les états de glycolyse élevée ou faible et selon les sous-types de cancer du sein, expliquant en partie pourquoi certaines tumeurs résistent mieux à l’attaque immunitaire. Pour explorer la causalité, les chercheurs ont utilisé une approche génétique appelée randomisation mendélienne. Ils ont trouvé qu’une activité génétiquement accrue de deux gènes, NT5E et NRG1, était associée à un risque légèrement moindre de cancer du sein, tandis qu’une activité plus élevée de S100B était liée à un risque accru. Des tests en laboratoire ont confirmé que ces gènes étaient altérés dans des lignées cellulaires de cancer du sein, et des simulations de docking ont suggéré que des médicaments existants tels que le trametinib et l’AZD8055 pourraient se lier fortement à des protéines liées à ce réseau glycolytique.
Ce que cela signifie pour les traitements futurs
Pris ensemble, les résultats dessinent un paysage dans lequel les tumeurs fortement dépendantes de la glycolyse non seulement croissent plus rapidement, mais construisent aussi un environnement immunitaire plus hostile qui les protège de l’attaque. En capturant ce comportement dans un score à 16 gènes, les cliniciens pourront éventuellement mieux classer les patientes selon le risque et adapter les choix thérapeutiques. L’identification de gènes spécifiques protecteurs ou à risque, ainsi que de candidats médicaments ciblant leurs voies, ouvre la voie à des stratégies futures combinant des traitements ciblant le métabolisme et l’immunothérapie. Si ces résultats sont validés en essais cliniques, cette feuille de route métabolisme–immunité pourrait aider à convertir davantage de tumeurs mammaires « froides » en tumeurs « chaudes », améliorant les pronostics des femmes dans le monde entier.
Citation: Niu, Y., Jiang, Y., Wang, Z. et al. Functional genomics integration of glycolysis-related gene networks reveals prognostic biomarkers and immune microenvironment regulation in breast cancer. Sci Rep 16, 9583 (2026). https://doi.org/10.1038/s41598-025-29391-7
Mots-clés: cancer du sein, métabolisme tumoral, gènes de la glycolyse, microenvironnement immunitaire, oncologie de précision