Clear Sky Science · fr
Séquençage du génome entier apparié du sang (10×) et de cinq cellules spermatiques individuelles (1×) par individu chez 53 hommes
Pourquoi cette étude compte pour les familles
Pour de nombreux couples qui peinent à concevoir, l’attention se porte souvent sur les taux hormonaux ou l’état général de santé, tandis que les détails fins à l’intérieur des spermatozoïdes restent obscurs. Cette étude ouvre une nouvelle fenêtre sur ces détails en lisant soigneusement l’ADN complet à la fois du sang et de cellules spermatiques individuelles chez des dizaines d’hommes. En associant ces données génétiques à des mesures précises du mouvement des spermatozoïdes, les chercheurs ont créé une ressource partagée qui pourrait aider la communauté scientifique mondiale à mieux comprendre l’infertilité masculine et, à terme, améliorer le diagnostic et le traitement.
Examen attentif des spermatozoïdes mobiles et apathiques
Les causes de l’infertilité masculine sont nombreuses, mais l’une des plus courantes est l’asthénozoospermie, une affection dans laquelle les spermatozoïdes sont vivants mais se déplacent trop lentement ou faiblement pour atteindre et féconder un ovule. Dans ce projet, l’équipe a recruté 53 hommes d’ethnie Han chinoise : 37 présentant une qualité de sperme typique et une fertilité confirmée, et 16 dont les spermatozoïdes étaient peu mobiles malgré des concentrations normales. Tous les participants ont été minutieusement examinés pour exclure d’autres problèmes médicaux et une infection récente par la COVID‑19, afin que les différences de motilité soient moins susceptibles d’être confondues avec des maladies non liées. Pour chaque homme, les cliniciens ont enregistré un ensemble riche de données de santé, notamment l’âge, la morphologie corporelle, les habitudes de tabagisme et de consommation d’alcool, l’historique reproductif, les taux hormonaux et une large gamme de mesures du sperme telles que la motilité totale, la vitesse de nage et les schémas de mouvement.
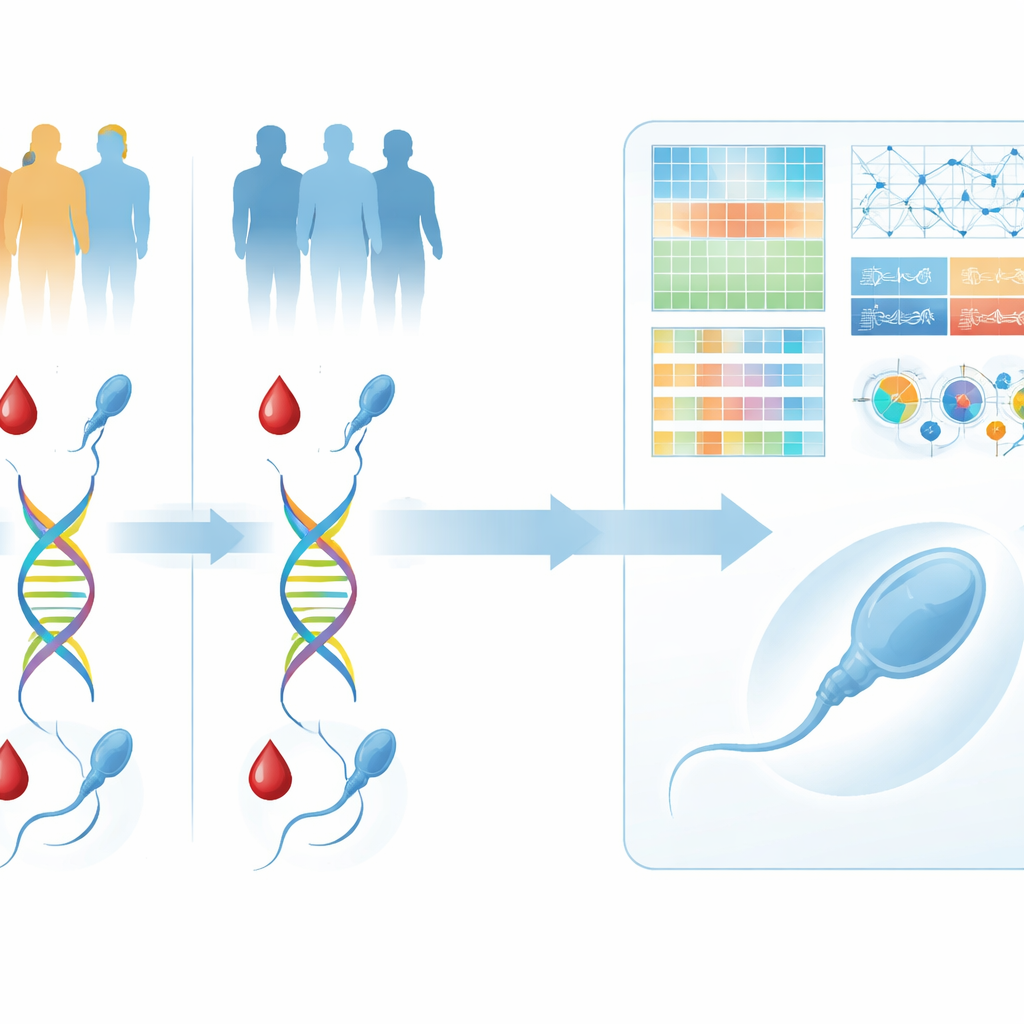
Construire une carte de l’ADN à partir du sang et de spermatozoïdes individuels
Ce qui distingue ce travail est son double axe : les chercheurs n’ont pas seulement observé le sperme au microscope, ils ont aussi collecté des informations génétiques complètes à la fois du sang et de cellules spermatiques individuelles. Les échantillons de sang ont fourni une vue du plan génétique général de chaque homme à environ dix fois de couverture, ce qui signifie que la plupart des positions du génome ont été lues plusieurs fois pour plus de fiabilité. Pour chaque participant, les techniciens ont ensuite isolé laborieusement plusieurs cellules spermatiques individuelles une à une au microscope, en évitant celles qui paraissaient manifestement anormales. Ces cellules uniques ont été traitées avec une méthode spécialisée permettant d’amplifier et de séquencer presque la totalité de leur ADN, fournissant un aperçu de faible mais exploitable couverture du génome de chaque spermatozoïde.
Transformer des lectures brutes en une ressource de données de haute qualité
Étant donné qu’il s’agit d’une étude axée sur les données plutôt que d’une expérience visant une hypothèse précise, l’issue clé est la qualité et la structure même du jeu de données. L’équipe a vérifié la concentration et l’intégrité de l’ADN, éliminé le bruit technique et confirmé que les séquences issues du sang et des spermatozoïdes respectaient les standards courants en génétique humaine. En moyenne, l’ADN sanguin a été séquencé à une profondeur légèrement supérieure à dix fois, tandis que l’ADN des spermatozoïdes a atteint environ 1,7× de couverture par cellule, un niveau adapté à la détection de motifs à grande échelle à travers de nombreuses cellules. Ils ont également confirmé que les taux hormonaux tels que la testostérone et les œstrogènes étaient similaires entre les hommes aux spermatozoïdes apathiques et ceux à fertilité typique. Les différences réelles concernaient la qualité du mouvement : le groupe fécond avait environ le double de motilité totale et des valeurs plus élevées pour le trajet de nage et les comportements de virage, soulignant que les deux groupes diffèrent de manière significative sur le plan fonctionnel même lorsque leurs profils hormonaux sont similaires.
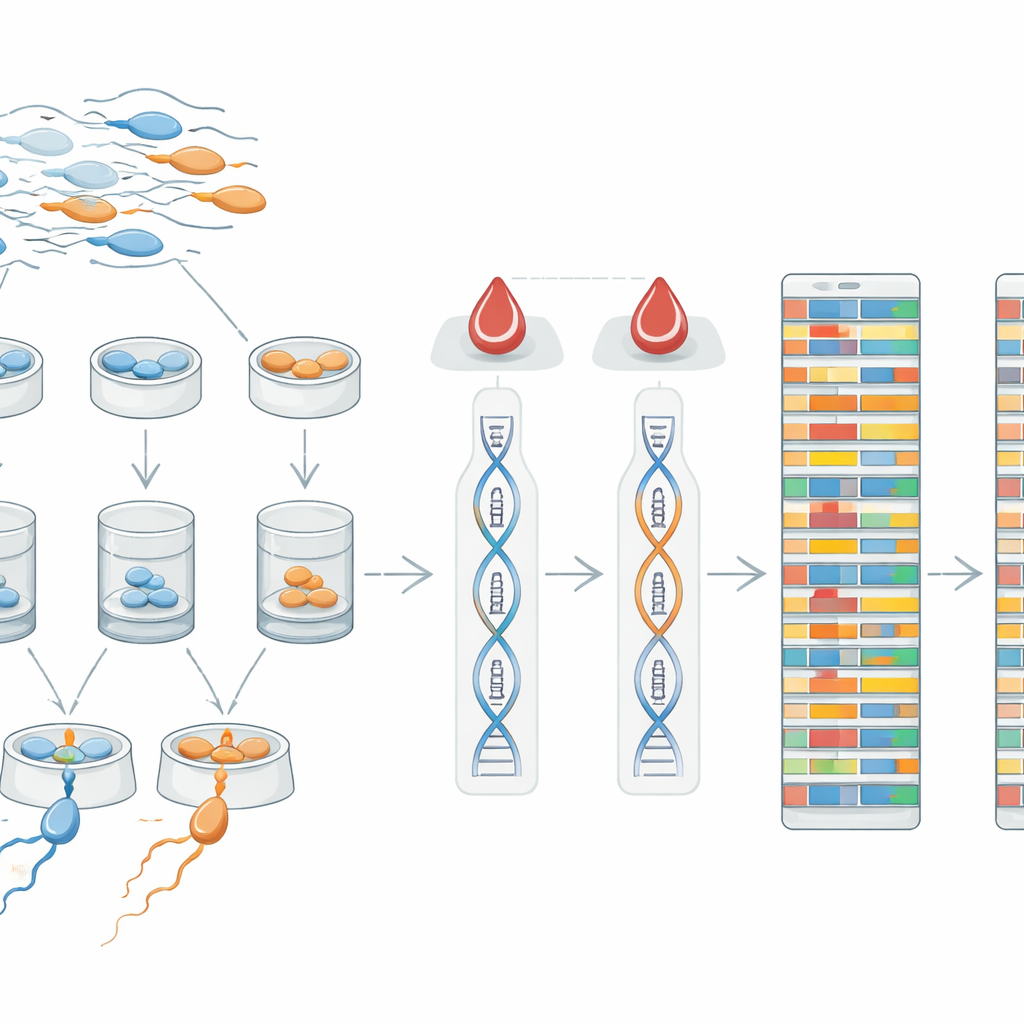
Un nouveau terrain d’essai pour les algorithmes de fertilité
En rendant toutes ces données accessibles publiquement, les auteurs visent à accélérer le développement de méthodes dans plusieurs domaines de pointe. Parce que les spermatozoïdes portent une seule copie de chaque chromosome, leur génome offre une façon claire de tracer la recombinaison de l’ADN lors de la formation des spermatozoïdes et d’examiner comment des combinaisons spécifiques de variantes génétiques pourraient se rapporter aux performances des spermatozoïdes. Les séquences appariées du sang et des spermatozoïdes fournissent également une référence pour tester de nouveaux outils informatiques qui cherchent à combler des informations manquantes dans des données à faible couverture, ou à reconstruire de longs tronçons d’ADN hérité à partir d’indices dispersés. Les chercheurs peuvent utiliser ce jeu de données pour affiner des méthodes de détection des mutations rares, suivre les événements de crossing‑over où les chromosomes parentaux échangent des segments, et comparer les motifs génétiques entre hommes avec et sans troubles de la motilité.
Ce que cela signifie pour les patients futurs
Pour les patients aujourd’hui, ce jeu de données ne se traduit pas encore par un nouveau test clinique, et il n’identifie pas un unique « gène de l’infertilité ». Il propose plutôt une base soigneusement organisée sur laquelle de nombreuses études futures pourront s’appuyer. En combinant des mesures détaillées du comportement des spermatozoïdes avec de l’ADN apparié provenant à la fois de cellules somatiques et de spermatozoïdes individuels, la ressource offre aux scientifiques une plateforme puissante pour explorer comment de subtiles différences génétiques peuvent influencer la fertilité masculine. Au fil du temps, à mesure que davantage d’équipes analyseront ces données et y ajouteront les leurs, ce travail pourrait aider à transformer des étiquettes vagues comme « infertilité masculine inexpliquée » en diagnostics plus clairs, informés par l’ADN, et à guider des choix de prise en charge reproductive plus personnalisés.
Citation: Chen, W., Yu, L., Li, R. et al. Matched whole-genome sequencing of blood (10×) and five single sperm cells (1×) per individual in 53 men. Sci Data 13, 405 (2026). https://doi.org/10.1038/s41597-026-06808-0
Mots-clés: infertilité masculine, motilité des spermatozoïdes, séquençage du génome entier, génomique unicellulaire, santé reproductive