Clear Sky Science · fr
Un ensemble de données transcriptomiques unicellulaires cartographiant les traumatismes crâniens et une thérapie génique basée sur NeuroD1 chez la souris
Pourquoi les blessures cérébrales nous concernent tous
Chaque année, des millions de personnes reçoivent des coups à la tête à la suite de chutes, d’accidents, de pratiques sportives ou de combats. Ces traumatismes crâniens peuvent laisser des séquelles durables sur la mémoire, la motricité et l’humeur, et les traitements actuels gèrent principalement les symptômes plutôt que de réparer véritablement le cerveau. Cette étude explore une approche prometteuse basée sur la thérapie génique chez la souris qui vise non seulement à limiter les dommages, mais aussi à aider le cerveau à se reconstruire de l’intérieur, en cartographiant ces changements cellule par cellule pour créer une ressource publique pour de futures thérapies.
Observer l’intérieur du cerveau blessé
Lorsqu’un cerveau est blessé, il ne se contusionne pas simplement comme un muscle. Une chaîne de réactions complexes se déclenche : des neurones meurent, la circulation sanguine est perturbée et des cellules de soutien appelées astrocytes ainsi que des cellules immunitaires affluents. Les astrocytes aident normalement à nourrir les neurones et à maintenir l’équilibre de la signalisation cérébrale, mais après un traumatisme ils peuvent former une cicatrice dense et alimenter une inflammation durable. Les auteurs ont utilisé une lésion contrôlée par incision du cortex chez la souris pour reproduire certaines formes de blessures pénétrantes du cerveau, puis ont examiné comment chaque type cellulaire majeur du tissu affecté réagissait au fil du temps. Ils ont appliqué une technique appelée séquençage ARN unicellulaire, qui lit les gènes activés dans des dizaines de milliers de cellules individuelles, permettant un recensement détaillé de l’évolution de la communauté cellulaire du cerveau après la lésion.
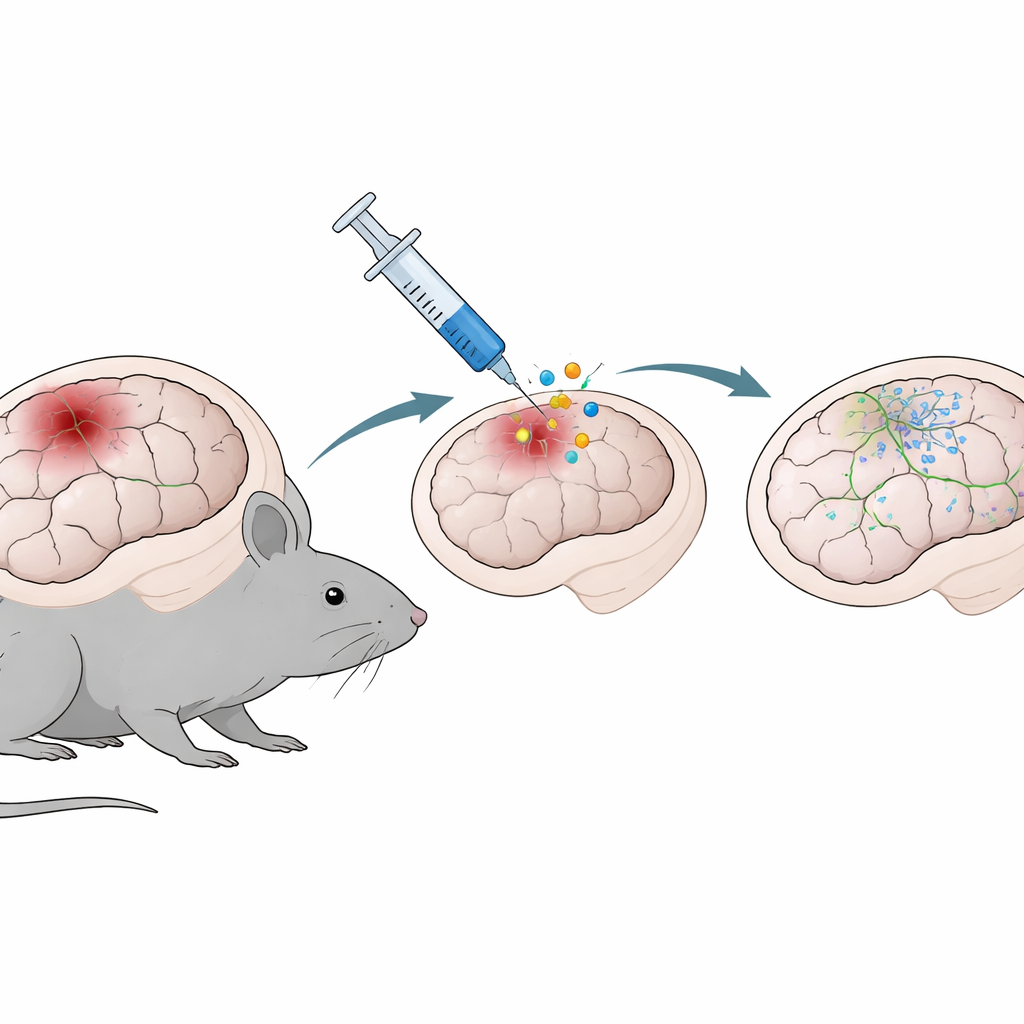
Une thérapie génique qui mobilise les cellules de soutien cérébral
Parce que les astrocytes sont abondants et se trouvent directement sur le site de la lésion, ils constituent des cibles attrayantes pour des stratégies de réparation. L’équipe a testé une thérapie génique basée sur NeuroD1, un gène connu pour pousser les cellules vers un état proche de celui des neurones. À l’aide d’un vecteur viral inoffensif injecté dans la zone corticale endommagée trois jours après la blessure, ils ont délivré soit un marqueur neutre (GFP), soit NeuroD1 aux astrocytes. Lorsqu’ils ont examiné les cerveaux une et deux semaines plus tard, les souris ayant reçu NeuroD1 présentaient des cavités tissulaires plus petites là où les dégâts s’étaient produits et moins de cellules immunitaires activées appelées microglies autour de la lésion. En d’autres termes, la thérapie réduisait non seulement les dommages structuraux visibles, mais calmait aussi la réponse inflammatoire locale.
Suivre les types cellulaires un par un
Pour comprendre ce qui sous-tendait ces améliorations, les chercheurs ont comparé trois groupes d’échantillons corticaux : des souris saines, des souris blessées recevant le virus témoin et des souris blessées recevant le virus NeuroD1. Ils ont séquencé plus de 97 000 cellules individuelles au total et les ont regroupées selon leurs profils d’expression génique en habitants cérébraux familiers, y compris les neurones, les astrocytes, les oligodendrocytes (qui isolent les fibres nerveuses), les microglies et les cellules tapissant les vaisseaux sanguins et les cavités cérébrales. La seule blessure a déplacé cet équilibre vers davantage d’astrocytes et de microglies et moins de neurones et de cellules productrices de myéline, reflétant la cicatrisation et l’inflammation. Avec le traitement NeuroD1, ce déséquilibre a commencé à s’inverser : les fractions de neurones, d’oligodendrocytes et de cellules épithéliales du plexus choroïde ont augmenté, tandis que les astrocytes et les microglies sont devenus moins dominants dans la zone lésée.
Le travail caché des sous-types d’astrocytes
Il s’est avéré que les astrocytes ne constituent pas une population uniforme. En les ré-analysant séparément, l’équipe a identifié sept sous-clusters d’astrocytes distincts, chacun avec sa propre signature génique et son comportement à travers les trois conditions. Certains sous-clusters étaient courants dans le tissu sain mais quasi absents après la blessure, tandis que d’autres n’apparaissaient qu’après le traumatisme. Dans les cerveaux blessés traités avec le virus témoin, plusieurs groupes d’astrocytes ont activé des programmes impliqués dans la construction et la restructuration des synapses — les jonctions où communiquent les neurones — tout en réduisant l’expression de gènes liés à la production d’énergie mitochondriale. Ce schéma suggère qu’après la blessure, les astrocytes favorisaient des modifications anormales du câblage tout en fonctionnant sur une puissance métabolique réduite.
Comment NeuroD1 rééquilibre énergie cellulaire et câblage
Le traitement par NeuroD1 a remodelé ces sous-clusters d’astrocytes dans une direction différente. Dans plusieurs groupes d’astrocytes liés à la blessure, des gènes associés à l’activité mitochondriale, à la respiration cellulaire et au métabolisme énergétique général ont été à nouveau stimulés, tandis que les gènes liés à une construction synaptique excessive et au remodelage de la myéline ont été atténués. En d’autres termes, NeuroD1 semblait rétablir les moteurs énergétiques de ces cellules et tempérer des tentatives incontrôlées de rebranchement qui pourraient autrement contribuer à la dysfonction. Certains sous-types d’astrocytes qui s’étaient fortement développés après la blessure ont diminué en présence de NeuroD1, tandis que d’autres associés à des fonctions plus saines ont augmenté. Ces changements fins fournissent des indices sur les états d’astrocytes nuisibles et ceux qui pourraient soutenir la réparation.
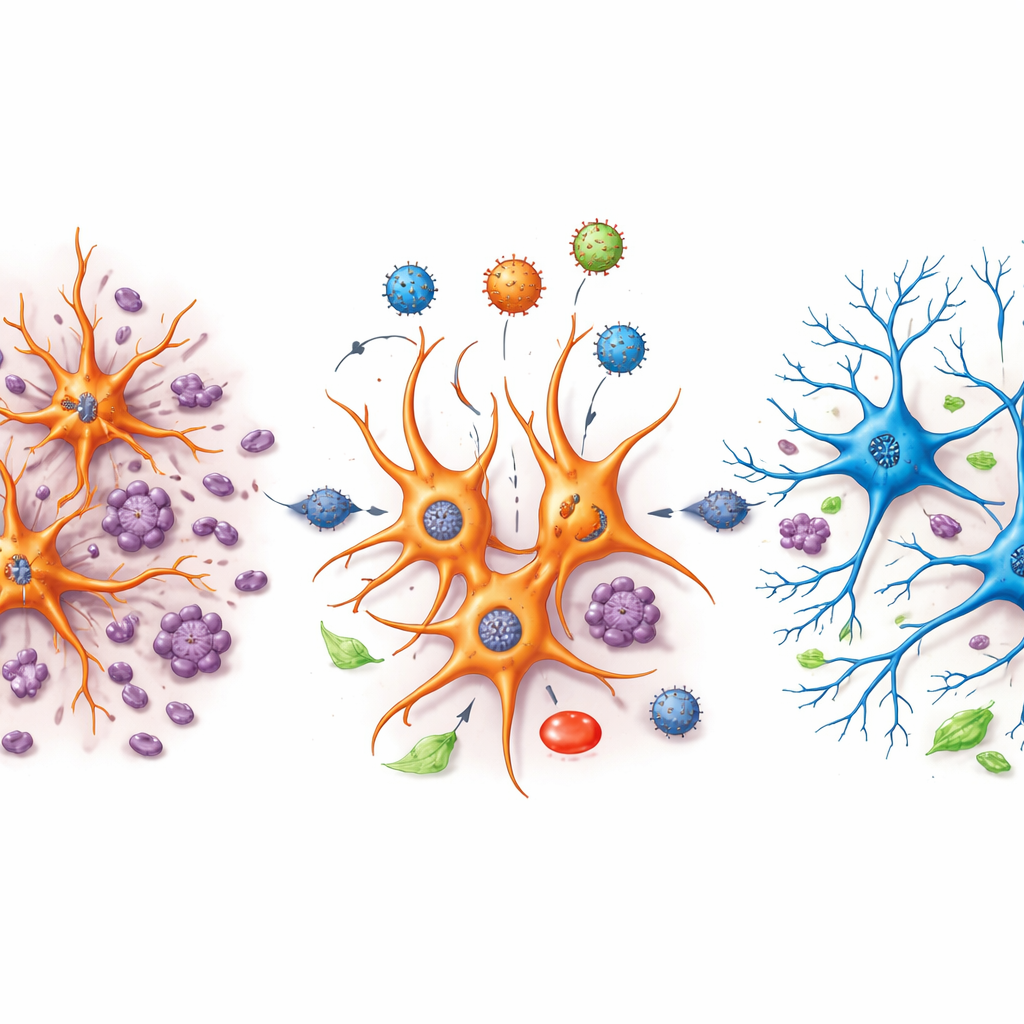
Ce que cela signifie pour la réparation cérébrale future
Ce travail n’offre pas encore de remède clé en main pour les traumatismes crâniens humains, mais il apporte deux avancées importantes. D’abord, il montre, dans un cerveau mammifère vivant, qu’une thérapie génique ciblée peut diminuer la perte tissulaire et l’inflammation tout en poussant les populations cellulaires et l’utilisation d’énergie vers un état plus sain. Ensuite, il met à disposition un riche ensemble de données unicellulaires public que d’autres scientifiques peuvent exploiter pour identifier des types cellulaires, des gènes et des voies spécifiques qui entraînent les dommages ou la récupération après un traumatisme. Pour les lecteurs hors laboratoire, le message clé est que les cellules de soutien du cerveau peuvent potentiellement être recrutées et reprogrammées pour aider à reconstruire les circuits lésés, nous rapprochant d’un pas vers des traitements qui restaurent, plutôt que se contentent de stabiliser, la fonction cérébrale après un coup traumatique.
Citation: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Mots-clés: traumatisme crânien, thérapie génique, astrocytes, séquençage unicellulaire, NeuroD1