Clear Sky Science · fr
Assemblage du génome au niveau chromosomique de Homatula variegata du bassin du Yangtsé
Un petit poisson de ruisseau au grand récit génétique
Dans les ruisseaux rapides et caillouteux qui alimentent le Haut‑Yangtsé en Chine vit une petite loache rayée, Homatula variegata. Elle est prisée à la fois pour la consommation et pour les aquariums domestiques, mais jusqu’à présent son plan d’ADN était quasiment inconnu. Cette étude fournit la première carte presque complète, chromosome par chromosome, du génome de l’espèce, ouvrant la voie à une conservation plus éclairée, à un élevage plus efficace et à une compréhension approfondie de la manière dont la vie s’adapte aux eaux froides et tumultueuses de montagne.
Pourquoi cartographier l’ADN d’un poisson modeste ?
Bien que cette loache n’atteigne qu’environ 14 centimètres, elle joue un rôle disproportionné dans les écosystèmes fluviaux locaux et dans l’aquaculture régionale. Elle prospère dans des ruisseaux d’altitude moyenne au fond graveleux et au courant soutenu, se nourrissant d’insectes, de débris organiques et de petits poissons. Parce qu’elle est à la fois savoureuse et colorée, l’intérêt grandit pour sa culture comme espèce ornementale et alimentaire locale. Pourtant, élever et protéger une espèce est bien plus difficile sans référence génétique précise. Un génome complet agit comme une liste détaillée de pièces et un schéma électrique, révélant les gènes qui déterminent la croissance, la couleur, la résistance aux maladies et la capacité à supporter des eaux rapides et fraîches. Jusqu’ici, aucune loache de cette branche de la famille des poissons ne disposait d’une telle référence de haute qualité, laissant un angle mort important dans la génétique des poissons d’eau douce.
Construire une carte d’ADN chromosome par chromosome
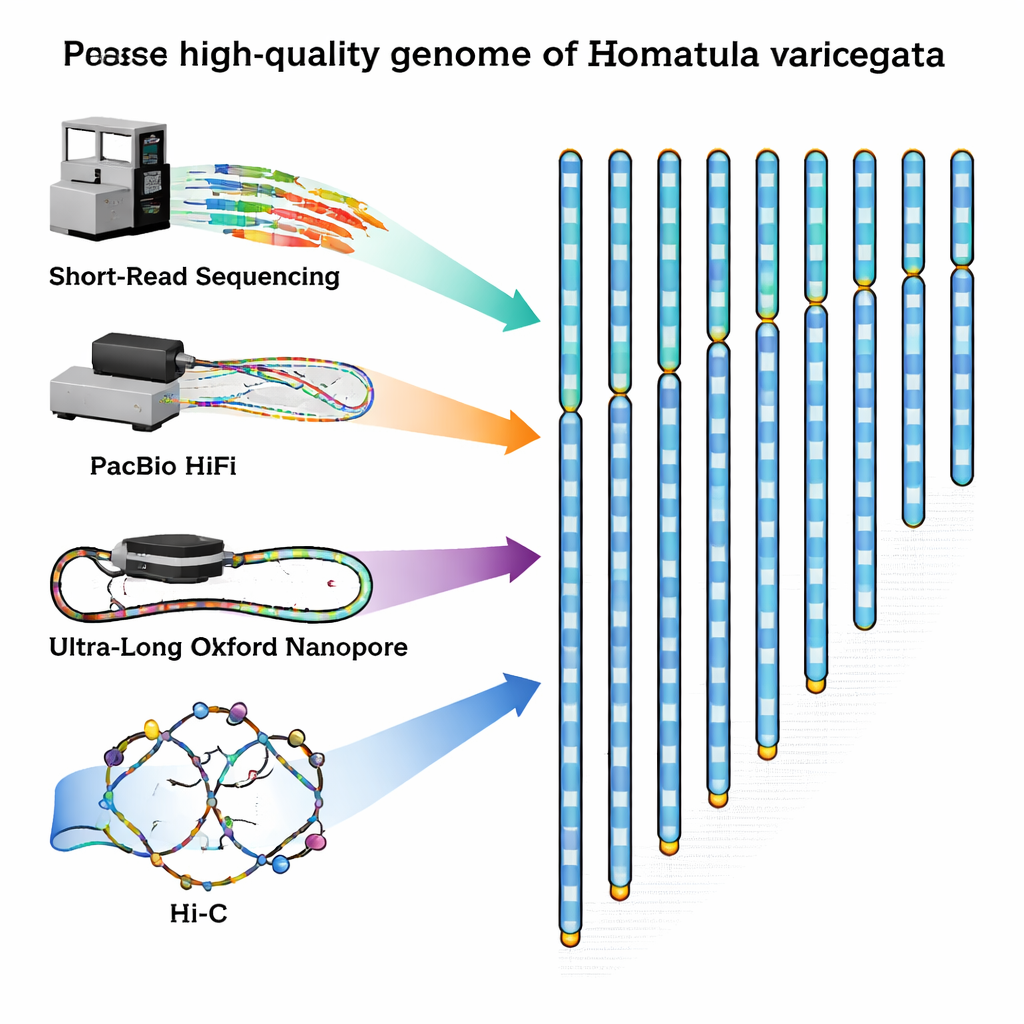
Pour combler cette lacune, les chercheurs ont capturé un mâle adulte en bonne santé dans la rivière Qingyi, un affluent du Yangtsé, et ont extrait avec soin l’ADN et l’ARN de son sang. Ils ont ensuite combiné plusieurs méthodes de séquençage de pointe, chacune ayant des atouts différents. Les machines à lectures courtes d’Illumina ont produit un grand nombre de fragments d’ADN très précis. La technologie PacBio HiFi a fourni des fragments plus longs avec une excellente exactitude, tandis que les appareils Oxford Nanopore ont généré des brins ultra‑longs capables de couvrir des régions répétitives difficiles à déchiffrer. Enfin, une méthode appelée Hi‑C a capturé la manière dont les brins d’ADN se replient et interagissent à l’intérieur du noyau cellulaire, fournissant une carte de contact 3D qui aide à relier les fragments en chromosomes complets dans le bon ordre.
Ce que révèle le nouveau génome
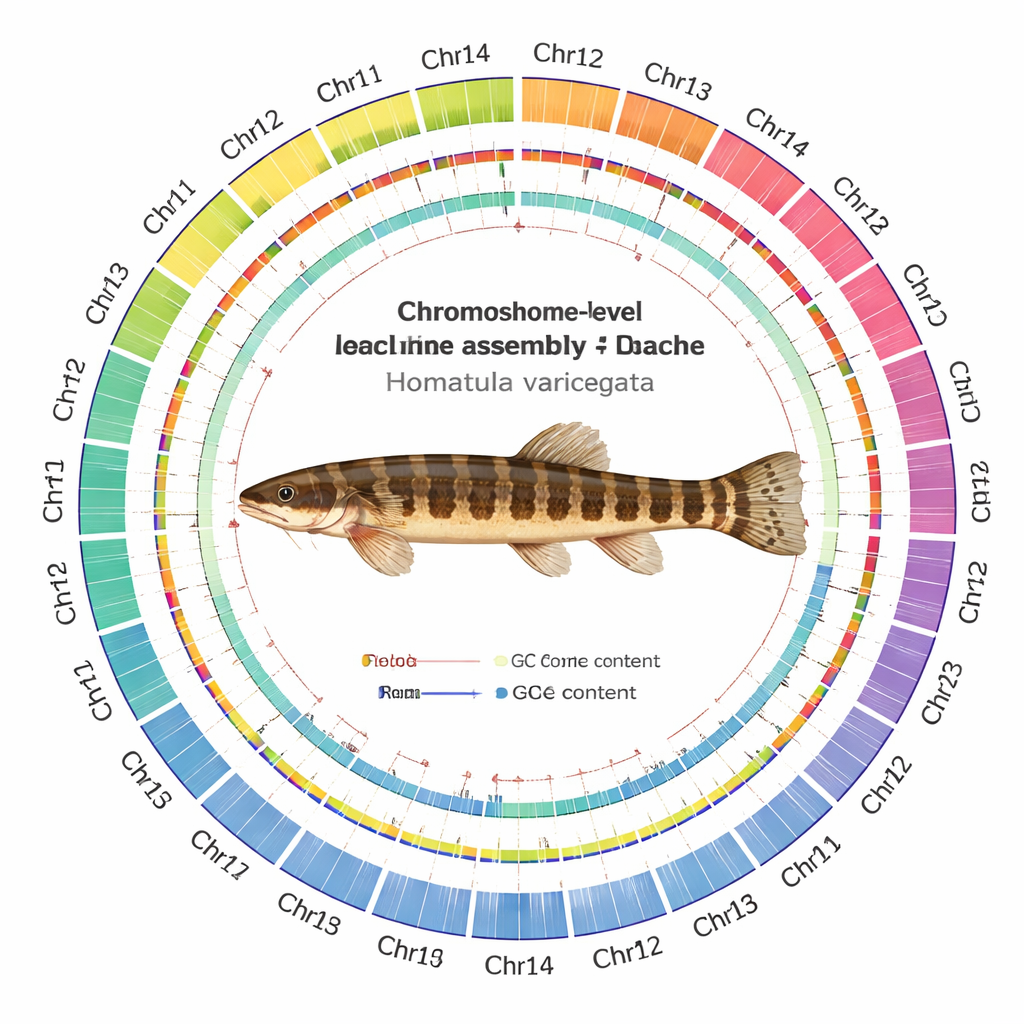
En tissant ces données avec des logiciels d’assemblage modernes et des contrôles de qualité rigoureux, l’équipe a produit un génome de 641 millions de lettres d’ADN, soigneusement organisé en 24 chromosomes. De manière remarquable, chaque chromosome est assemblé en une seule pièce continue, 22 d’entre eux ne présentant aucun espace et deux seulement comportant de très petits écarts. Ils ont pu localiser 24 centromères probables — la « ceinture » centrale de chaque chromosome — et détecter la plupart des télomères protecteurs aux extrémités chromosomiques. Les scientifiques ont répertorié 24 479 gènes codant pour des protéines et ont pu attribuer des fonctions probables à environ 93 % d’entre eux en les comparant à de grandes bases de données internationales. Ils ont aussi cartographié le paysage de l’ADN répétitif, constatant que plus d’un quart du génome est composé d’éléments génétiques mobiles, en particulier des transposons à ADN, qui peuvent sauter dans le génome et parfois impulser l’évolution.
Tester la qualité sous le capot
Les chiffres d’ensemble ne valent que si la carte sous‑jacente est fiable. L’équipe a donc soumis l’assemblage à une batterie de tests. Les lectures provenant de toutes les plateformes de séquençage se réalignent sur le nouveau génome à des taux très élevés, avec une couverture uniforme sur la plupart des chromosomes. Des outils indépendants qui comptent les courts motifs d’ADN ont suggéré que presque tout le contenu attendu est présent, et les tests standard de complétude des gènes ont montré que la grande majorité des gènes universels des poissons sont intacts. Les cartes de contact Hi‑C ont formé des motifs carrés nets le long de chaque chromosome, avec peu de signal parasite entre eux, indiquant que les segments sont correctement assemblés et non mélangés.
De la carte d’ADN à l’impact concret
Pour un non‑spécialiste, ce travail peut sembler un triomphe technique pour lui‑même, mais ses implications sont pratiques et larges. Disposer d’un génome quasi complet pour Homatula variegata fournit aux scientifiques une référence contre laquelle comparer les populations sauvages, suivre la diversité génétique et repérer des signes de consanguinité ou d’adaptation locale. Les éleveurs peuvent rechercher des marqueurs d’ADN liés à des traits désirables tels qu’une croissance rapide, la robustesse ou une coloration marquée, accélérant la sélection tout en préservant le caractère naturel de l’espèce. Les écologues peuvent examiner comment cette loache a évolué pour vivre dans des ruisseaux de montagne frais et rapides, des enseignements qui peuvent aussi éclairer la gestion d’espèces apparentées. En bref, ce génome au niveau chromosomique transforme un modeste poisson de rivière en un modèle puissant pour comprendre — et protéger — la richesse de la vie dans les écosystèmes d’eau douce asiatiques.
Citation: Tang, Y., Wu, Q., Wang, Y. et al. A chromosome level genome assembly of Homatula variegata from the Yangtze River basin. Sci Data 13, 303 (2026). https://doi.org/10.1038/s41597-026-06667-9
Mots-clés: génome de poisson, assemblage chromosomique, biodiversité d’eau douce, génétique de l’aquaculture, loache du Yangtsé