Clear Sky Science · fr
Le jeu de données 2024 du défi de segmentation des tumeurs cérébrales pour la radiothérapie des méningiomes (BraTS-MEN-RT)
Pourquoi cartographier les tumeurs cérébrales importe
Lorsqu’une personne est traitée pour une tumeur cérébrale, les médecins doivent viser la radiation avec précision : suffisamment pour tuer les cellules tumorales, mais pas au point d’endommager le tissu cérébral sain. Pour un type courant de tumeur cérébrale appelé méningiome, cette étape de ciblage dépend des experts qui tracent la tumeur manuellement sur des scans IRM en trois dimensions. Ce travail est lent, minutieux et peut varier d’un spécialiste à l’autre. Cet article décrit un vaste nouveau jeu de données international qui capture la manière dont les experts délimitent les méningiomes pour la radiothérapie, jetant les bases de programmes informatiques capables d’effectuer ce travail plus rapidement et de façon plus homogène.
Une tumeur cérébrale fréquente au traitement complexe
Les méningiomes proviennent des enveloppes du cerveau et sont les tumeurs cérébrales primaires les plus fréquentes chez l’adulte. Beaucoup sont à croissance lente et non cancéreuses, mais d’autres peuvent récidiver après chirurgie ou se comporter de façon agressive, rendant la radiothérapie une composante importante des soins. Avant d’administrer la radiation, les cliniciens doivent définir le « volume cible » sur l’IRM : l’étendue complète de la tumeur et, dans les cas post-opératoires, la cavité chirurgicale où des cellules tumorales peuvent subsister. Ce n’est pas aussi simple qu’il y paraît. Les tissus cicatriciels, les modifications liées à la chirurgie, les implants métalliques et les cadres crâniens spécialisés utilisés pour la radiothérapie focalisée peuvent déformer les images et rendre la délimitation de la tumeur difficile à discerner, même pour des experts chevronnés.
Constituer une bibliothèque d’images partagée
Pour améliorer cette étape cruciale, des chercheurs de sept grands centres aux États-Unis et au Royaume-Uni se sont associés pour créer le jeu de données BraTS-MEN-RT. Il contient 750 examens IRM utilisés dans de vrais plans de radiothérapie pour des patients atteints de méningiome, dont 570 scans et 500 volumes cibles tracés par des experts sont rendus publics. Les scans sont des images IRM 3D rehaussées au contraste qui correspondent étroitement à ce que les médecins utilisent réellement en salle de planification : ils conservent la résolution et l’orientation d’origine et incluent l’ensemble de la tête, pas seulement le cerveau. Les cas couvrent une large tranche d’âge, hommes et femmes, tumeurs intactes et situations post-opératoires, et plusieurs types de traitements radiothérapeutiques. Cette diversité est essentielle pour entraîner des modèles informatiques qui doivent fonctionner de manière fiable dans différents hôpitaux et sur différents appareils.
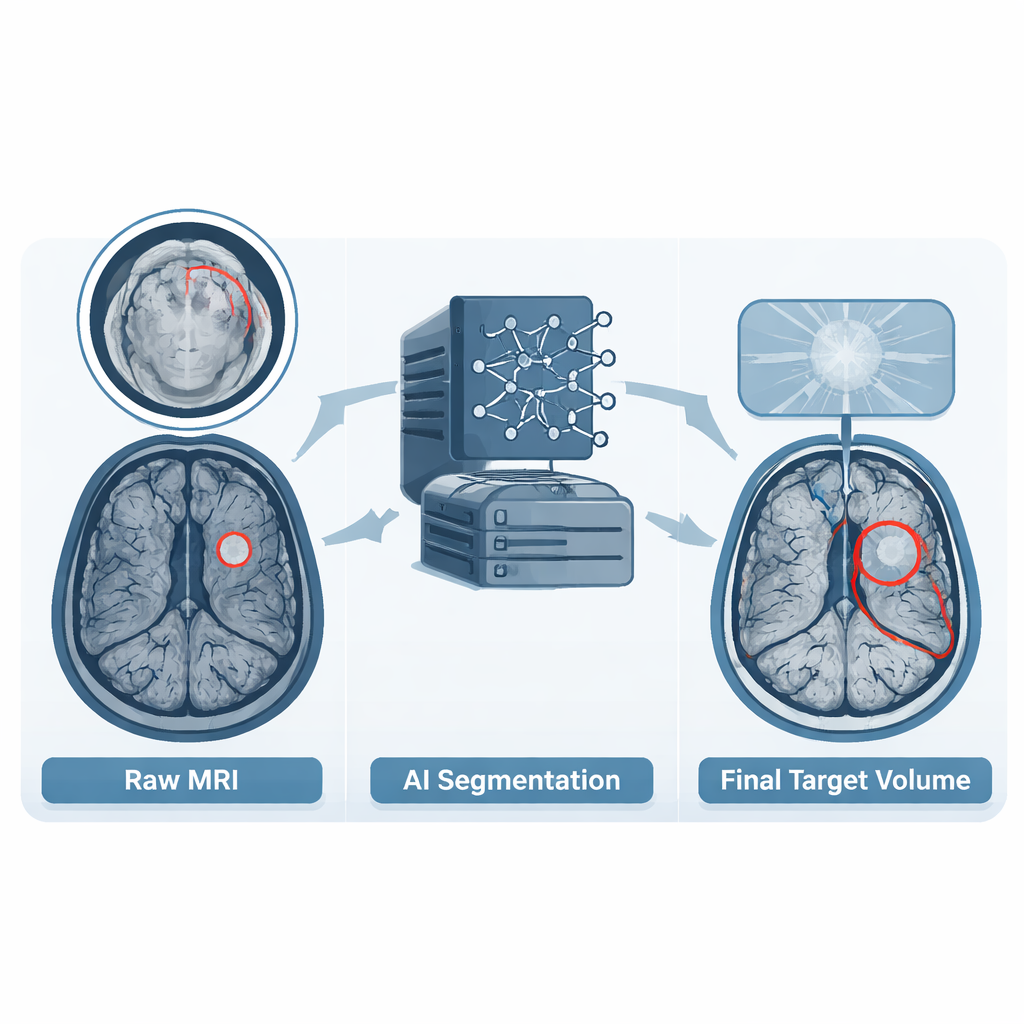
Protéger la vie privée tout en conservant l’essentiel
Parce que chaque IRM capture aussi le visage d’une personne, l’équipe a pris un soin particulier à protéger l’identité des patients. Ils ont utilisé une méthode automatisée qui supprime les traits du visage sur les images tout en laissant intact le crâne, le cerveau et les tumeurs. Chaque scan « défiguré » a ensuite été vérifié coupe par coupe par un neuroradiologue et un oncologue radiothérapeute pour s’assurer qu’aucun tissu tumoral n’avait été retiré par erreur, notamment pour les tumeurs proches de la base du crâne. Si une tumeur s’étendait trop dans la région supprimée et ne pouvait pas être restaurée en toute sécurité, le cas était exclu. Cet équilibre entre confidentialité et utilité médicale est central pour rendre de grandes collections d’images partageables de manière sûre.
Transformer le jugement d’experts en matériau d’entraînement
Outre les images, le jeu de données comprend des contours détaillés des régions tumorales connus sous le nom de volumes tumoraux bruts. Lorsque les hôpitaux avaient déjà tracé ces volumes dans leur planification de routine, ces contours ont servi de point de départ. Dans d’autres cas, ou lorsque les contours ne suivaient pas les directives convenues, l’équipe a utilisé un modèle d’apprentissage profond moderne pour produire une estimation initiale. Un interne en oncologie radiothérapeutique a ensuite examiné chaque cas coupe par coupe, ajustant les limites pour correspondre aux normes de traitement actuelles et ajoutant les éventuels foyers tumoraux supplémentaires qui auraient été manqués. Enfin, un neuroradiologue diplômé a vérifié chaque contour et a demandé des ajustements supplémentaires si nécessaire. Ce processus en plusieurs étapes a transformé des pratiques réelles variées en un ensemble de référence unique et cohérent dont les ordinateurs peuvent apprendre.
Comment cela améliore les soins aux patients
En rendant public ce jeu de données soigneusement sélectionné à la communauté de recherche, les auteurs fournissent l’ingrédient manquant pour concevoir et évaluer des algorithmes capables de cartographier automatiquement les cibles de méningiome sur les scans de planification en radiothérapie. Si de tels outils se révèlent précis, ils pourraient faire gagner du temps aux cliniciens, réduire les différences entre experts et établissements, et contribuer à ce qu’un plus grand nombre de patients reçoivent une radiation précisément ciblée. En termes concrets, ce travail transforme des milliers d’heures d’efforts de spécialistes en une ressource réutilisable qui pourrait rendre le traitement des tumeurs cérébrales plus sûr, plus homogène et plus accessible.
Citation: LaBella, D., Schumacher, K., Mix, M. et al. The 2024 Brain Tumor Segmentation Challenge Meningioma Radiotherapy (BraTS-MEN-RT) dataset. Sci Data 13, 306 (2026). https://doi.org/10.1038/s41597-026-06649-x
Mots-clés: méningiome, radiothérapie, IRM, segmentation de tumeur, jeu de données d'imagerie médicale