Clear Sky Science · fr
Données multiomiques temporelles d'expression génique lors de la différenciation en cellules polyhormonales dérivées de cellules souches embryonnaires humaines
Comment les cellules apprennent à former des organes
Nos corps commencent comme de petits amas de cellules identiques qui, d'une manière ou d'une autre, apprennent à devenir des tissus très différents, du cerveau au pancréas. Cette étude suit ce processus d'apprentissage en laboratoire, en utilisant des cellules souches embryonnaires humaines guidées pour devenir des cellules pancréatiques précoces. En suivant l'activité de milliers de gènes au fil du temps et à plusieurs niveaux, le travail crée une carte de référence riche qui peut aider les scientifiques à mieux comprendre le développement humain et, à terme, améliorer les stratégies de traitement de maladies comme le diabète.
Observer les cellules choisir une trajectoire
Les cellules souches embryonnaires humaines sont particulières parce qu'elles peuvent se transformer en presque n'importe quel type cellulaire de l'organisme. Dans cette étude, les chercheurs ont orienté ces cellules vers un destin précis : une lignée pancréatique appelée cellules polyhormonales, capables de produire des hormones clés comme l'insuline et le glucagon. Ils ont reproduit le développement précoce dans une boîte de culture en changeant progressivement le milieu de croissance, faisant passer les cellules d'un état primitif semblable à l'intestin (l'endoderme) puis vers des cellules pancréatiques productrices d'hormones sur une période de 17 jours. Des échantillons ont été prélevés à dix points temporels soigneusement choisis pour capturer tout le parcours, de la cellule souche plastique à la cellule spécialisée productrice d'hormones. 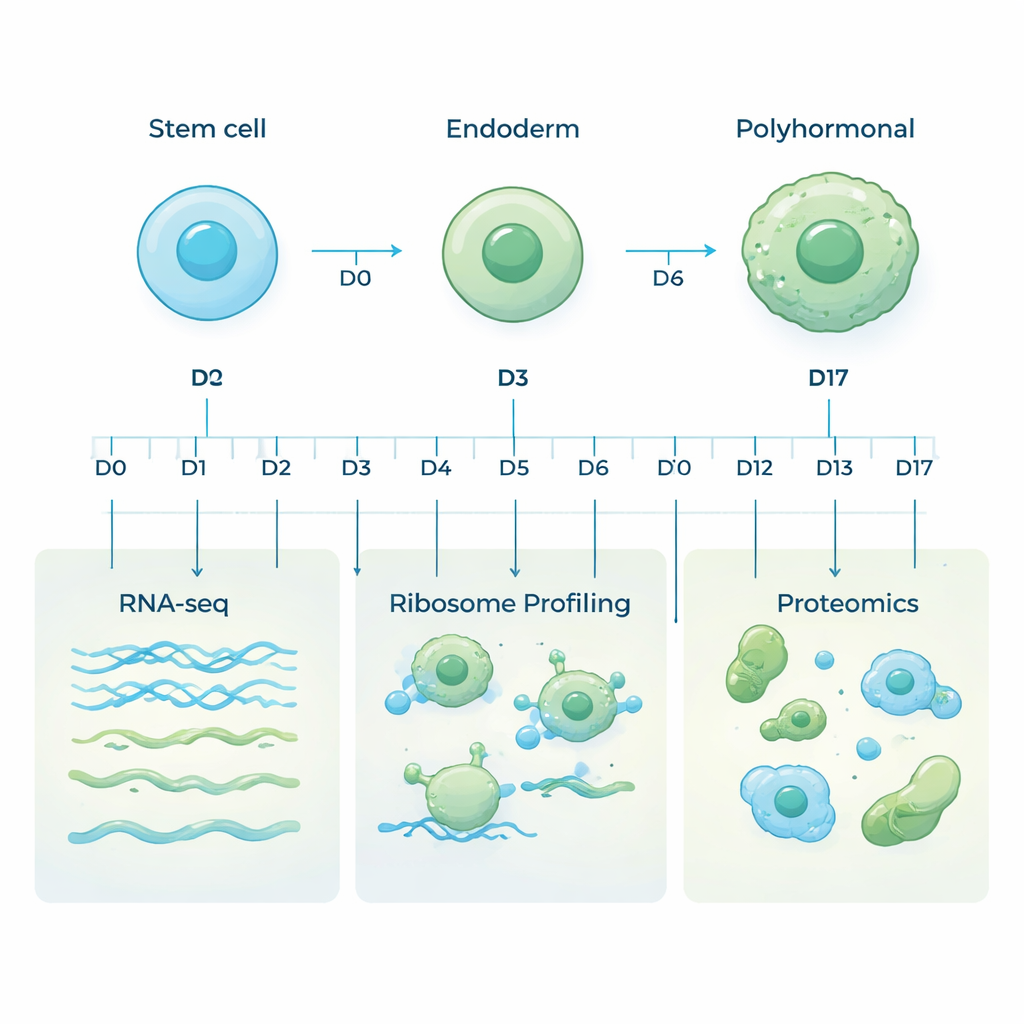
Regarder sous le capot à trois niveaux
La plupart des études ne regardent que l'ARN messager (ARNm), les molécules qui portent les instructions des gènes. Mais l'ARNm n'est qu'une partie de l'histoire : tous les messages ne sont pas traduits en protéines, et les protéines elles-mêmes peuvent être synthétisées ou dégradées à des rythmes différents. Pour obtenir une vue plus complète, l'équipe a utilisé trois approches complémentaires sur les mêmes échantillons. Le séquençage ARN a mesuré quels gènes étaient transcrits en ARNm. Le profilage des ribosomes a suivi quels messages étaient activement lus par les machines de fabrication des protéines de la cellule. La protéomique par spectrométrie de masse a ensuite mesuré les protéines réellement présentes. Ensemble, ces couches révèlent comment l'activité génétique est contrôlée lorsque les cellules changent d'identité.
Suivre les signaux clés de l'identité cellulaire
Pour vérifier que les cellules suivaient bien la trajectoire de développement prévue, les scientifiques ont surveillé des gènes marqueurs bien connus. Au début, des marqueurs classiques des cellules souches tels que OCT4 et NANOG étaient élevés puis ont diminué au fur et à mesure de la différenciation. Lorsque les cellules sont entrées dans le stade d'endoderme, des marqueurs comme KIT et SOX17 ont augmenté. Aux stades finaux, les marqueurs polyhormonaux insuline (INS) et glucagon (GCG) sont apparus fortement tant au niveau de l'ARN que des protéines, confirmant que les cellules avaient adopté une identité pancréatique productrice d'hormones. Bien que l'une des réplicas biologiques ait progressé légèrement plus lentement que l'autre, les deux ont suivi la même trajectoire générale, reflétant de petites différences naturelles plutôt que des problèmes techniques. 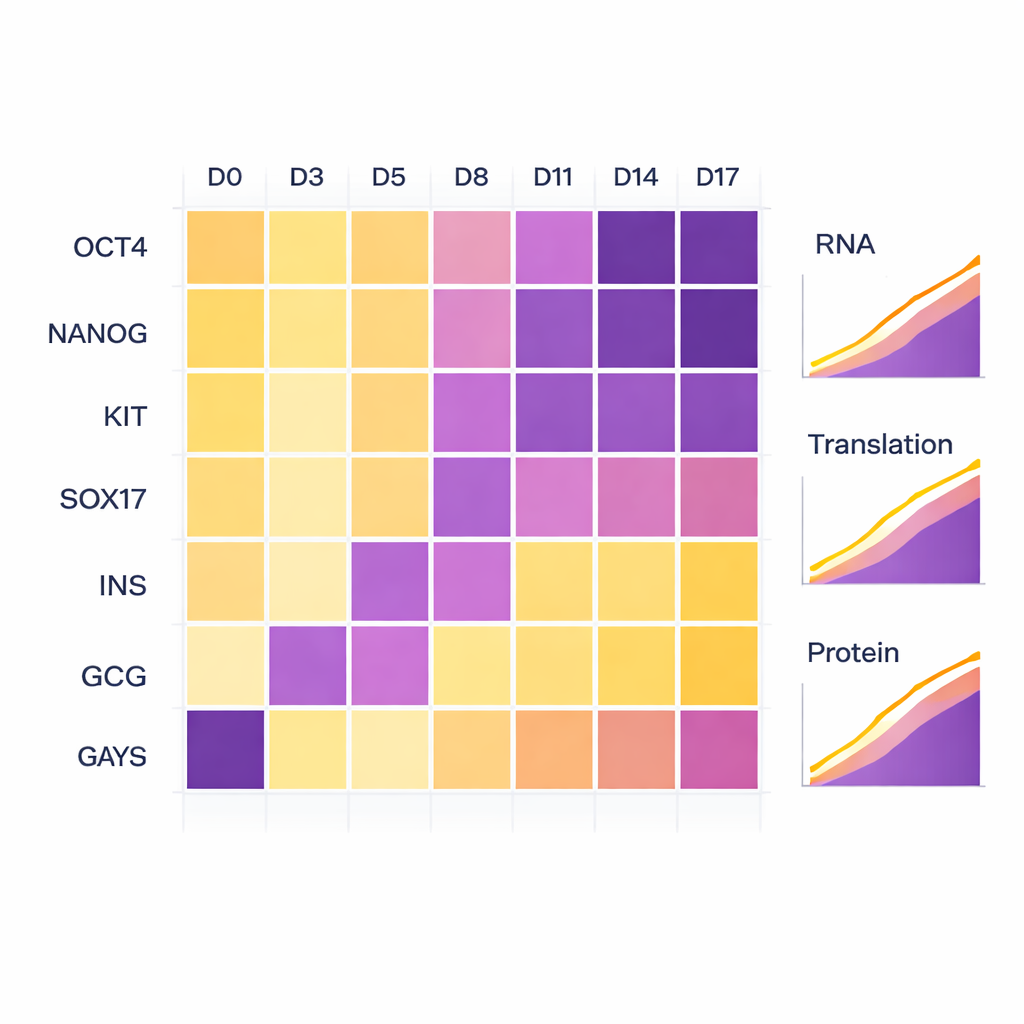
Contrôles de qualité pour une ressource fiable
Parce que ce travail vise à servir de ressource pour la communauté, les auteurs ont consacré de grands efforts à vérifier la qualité et la cohérence des données. Pour chacune des trois méthodes, ils ont évalué la précision du séquençage et des mesures, la couverture des gènes et l'accord entre expériences répétées. Les stades cellules souches et polyhormonales ont montré des différences claires et reproductibles aux niveaux de l'ARN, de la traduction et des protéines. Des analyses en composantes principales — des cartes statistiques regroupant les échantillons similaires — ont montré que les points temporels s'alignaient dans l'ordre, avec des stades précoces et tardifs clairement séparés et des réplicas biologiques fortement groupés. Les données de protéomique ont seules suivi de manière fiable près de 7 500 protéines à travers tous les points temporels, avec relativement peu de mesures manquantes, soulignant la profondeur de l'ensemble de données.
Une base pour des découvertes futures
Les auteurs rendent toutes les données brutes et traitées publiquement disponibles, ainsi que les scripts d'analyse et les fichiers de référence, afin que d'autres chercheurs puissent réutiliser et réanalyser l'ensemble de données. Au-delà de la description de la transformation d'un type cellulaire en un autre, ce travail offre une image temporelle détaillée de la façon dont les messages génétiques, leur traduction et les protéines résultantes interagissent durant une transition développementale majeure. Pour les non-spécialistes, l'idée essentielle est que le destin cellulaire est contrôlé par plusieurs couches de régulation qui agissent ensemble au fil du temps, et que cet ensemble de données fournit un « film » haute résolution de ces changements. Les scientifiques peuvent désormais utiliser cette ressource pour explorer pourquoi certains gènes changent tôt et d'autres tard, comment différents organes peuvent suivre des règles similaires ou distinctes, et comment mieux guider les cellules souches vers des destins utiles en médecine.
Citation: Keskin, A., Shayya, H.J., Patel, A. et al. Temporal multiomics gene expression data across human embryonic stem cell-derived polyhormonal cell differentiation. Sci Data 13, 278 (2026). https://doi.org/10.1038/s41597-026-06606-8
Mots-clés: cellules souches, développement du pancréas, expression génique, multiomiques, cellules polyhormonales