Clear Sky Science · fr
Atlas cérébral du marmoset Brain/MINDS 2.0 : parcellisation corticale populationnelle avec modèles multimodaux
Pourquoi le cerveau d’un petit singe compte
Le marmoset commun est un petit singe, mais son cerveau ressemble étonnamment au nôtre par son organisation et son câblage. Les chercheurs utilisent de plus en plus le marmoset pour étudier des affections comme la maladie d’Alzheimer et le déclin cérébral lié à l’âge, car des expériences impossibles à réaliser chez l’humain peuvent être conduites en toute sécurité chez l’animal. Cet article présente une nouvelle carte numérique 3D de haute précision du cerveau de marmoset, appelée Brain/MINDS Marmoset Brain Atlas 2.0 (BMA2.0). Elle fournit un système de référence commun permettant de comparer et de combiner des données issues de nombreux laboratoires, appareils et expériences — une étape essentielle pour comprendre le fonctionnement des cerveaux de primates et leurs dysfonctionnements en pathologie.
D’un cerveau unique à une vue populationnelle
Les atlas cérébraux de marmoset antérieurs étaient généralement construits à partir d’un seul animal. C’est comme tenter de définir le visage « typique » d’un humain à partir d’une seule photo : on ignore les variations naturelles de taille, de forme et de détails. BMA2.0 moyenne au contraire les informations provenant de nombreux individus — 91 IRM ex vivo (post‑mortem), 446 IRM in vivo et des colorations tissulaires détaillées de 10 cerveaux. En alignant soigneusement tous ces cerveaux dans un même système de coordonnées, l’atlas capture le patron de plis et de régions le plus fréquent tout en lissant les idiosyncrasies. Le résultat est un modèle symétrique, fondé sur la population, qui reflète mieux l’aspect d’un cerveau de marmoset « typique ».
Vues en couches de la structure cérébrale
Pour diviser le cerveau en parties signifiantes, l’équipe a combiné plusieurs types d’images. La coloration au myéline à haute résolution met en évidence le câblage, tandis que la coloration de Nissl montre la distribution des corps cellulaires. Les IRM ex vivo et in vivo apportent une couverture de l’ensemble du cerveau comparable à ce qui est utilisé en milieu hospitalier humain. En utilisant ces contrastes ensemble, des experts ont délimité manuellement 117 régions dans la « matière grise » externe par hémisphère et affiné 156 structures profondes ainsi que 45 régions cérébelleuses. Des logiciels avancés d’enregistrement et des modèles d’intelligence artificielle ont ensuite recollé des milliers de coupes tissulaires 2D en volumes 3D cohérents, les ont appariés aux IRM et les ont moyennés entre animaux. L’atlas final segmente chaque hémisphère en 323 régions et est accompagné de cartes planes et de modèles de surface permettant aux scientifiques de visualiser le cortex comme s’il avait été déroulé sur une feuille.
Algorithmes intelligents en coulisses
Construire un atlas aussi détaillé est exigeant techniquement. Les coupes tissulaires peuvent se déformer, les colorations varient selon les méthodes et les images provenant de scanners différents ne s’alignent pas automatiquement. Pour surmonter ces problèmes, les auteurs ont utilisé des algorithmes modernes d’alignement d’images associés à des outils d’apprentissage profond. Un réseau apprend à transformer les images Nissl en images de type myéline afin que deux colorations très différentes paraissent plus comparables. Un autre réseau apprend à marquer les frontières entre le cortex, les structures profondes et l’arrière‑plan, fournissant des « repères » supplémentaires qui aident l’alignement à verrouiller les structures en place. Pour garantir que les régions suivent la direction naturelle en colonnes du cortex, une approche mathématique basée sur l’équation de Laplace trace des lignes de courant depuis la surface externe du cerveau jusque’à la substance blanche, assignant à chaque petit élément de volume la région la plus probable le long de ces trajectoires.
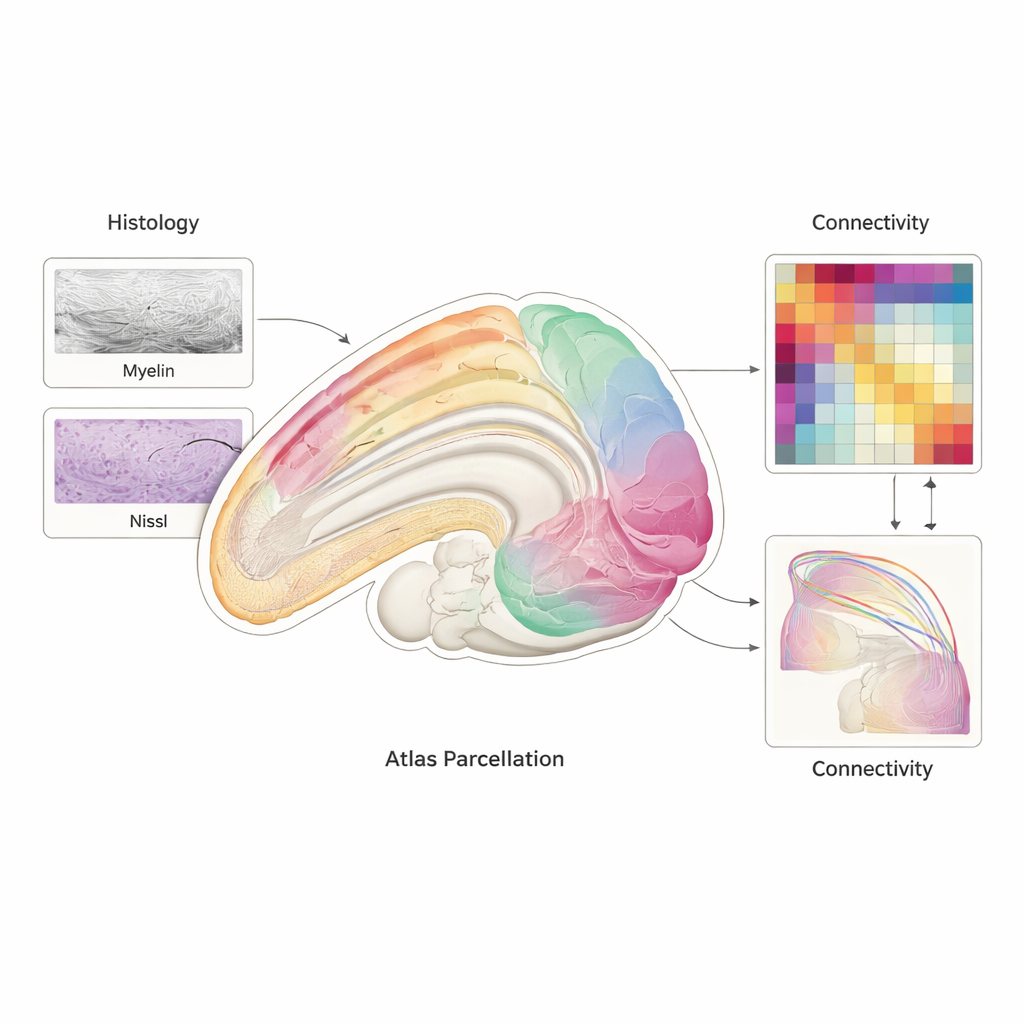
Relier l’anatomie à la fonction
BMA2.0 n’est pas qu’une image statique ; il est conçu pour relier structure et activité. Les auteurs montrent que lorsqu’ils utilisent les régions de l’atlas pour résumer les signaux d’IRMf au repos chez des marmosets éveillés, les motifs d’activité au fil du temps sont plus cohérents entre sessions et entre animaux que lorsque le cerveau est découpé en morceaux arbitraires basés sur la distance. Ils construisent également une carte moyenne populationnelle des connexions de la substance blanche à partir d’IRM de diffusion de 126 animaux, et la comparent à un jeu de données séparé d’injections de traceurs qui suivent les axones réels. Les deux cartes indépendantes concordent bien, ce qui soutient l’idée que l’atlas capture un câblage biologiquement pertinent. Parce que BMA2.0 peut être traduit dans les systèmes de coordonnées de plusieurs autres atlas de marmoset, il sert aussi de hub pour fusionner les jeux de données passés et futurs.
Ce que cela signifie pour la recherche cérébrale
Pour les non‑spécialistes, le message clé est que BMA2.0 offre aux scientifiques une « carte géographique » beaucoup plus fiable du cerveau de marmoset, basée non sur un seul animal mais sur une population et sur plusieurs méthodes d’imagerie. Cela facilite la comparaison des résultats entre études, la mise en relation d’une anatomie fine avec les signaux cérébraux et le comportement, et l’exploration de la manière dont les maladies et les traitements reconfigurent les réseaux cérébraux. Comme les marmosets sont des parents proches des humains et déjà largement utilisés dans la recherche sur le vieillissement et la démence, cet atlas devrait aider à traduire les découvertes chez ces petits singes en réponses aux grandes questions sur le cerveau humain.
Citation: Gong, R., Ichinohe, N., Abe, H. et al. Brain/MINDS Marmoset Brain Atlas 2.0: Population Cortical Parcellation With Multi-Modal Templates. Sci Data 13, 274 (2026). https://doi.org/10.1038/s41597-026-06601-z
Mots-clés: atlas cérébral de marmoset, neuroimagerie populationnelle, IRM multimodale, parcellisation corticale, connectome de primate