Clear Sky Science · fr
Profilage complet du transcriptome des carcinomes médullaires thyroïdiens sporadiques
Pourquoi ce cancer thyroïdien rare est important
Le carcinome médullaire de la thyroïde est une forme rare de cancer thyroïdien qui évolue de façon plus agressive que la plupart des tumeurs thyroïdiennes et touche souvent des patients à un stade déjà avancé. Parce qu’il est peu fréquent, médecins et chercheurs disposaient de données limitées pour comprendre pourquoi certaines tumeurs croissent et se propagent plus rapidement que d’autres, ou pourquoi certains patients répondent mieux aux traitements. Cette étude comble cette lacune en examinant de façon approfondie, à l’échelle du génome, l’activité de milliers de gènes dans 72 tumeurs, créant ainsi l’un des instantanés moléculaires les plus complets à ce jour de cette maladie.
Plongée dans les cellules tumorales
Plutôt que de se concentrer uniquement sur les mutations de l’ADN, les chercheurs ont analysé le « transcriptome » tumoral — l’ensemble des messages ARN produits par les gènes actifs dans les cellules cancéreuses. Ces messages ARN fonctionnent comme des rapports d’état en temps réel sur l’activité cellulaire. En séquençant l’ARN à partir d’échantillons tumoraux congelés rapidement, l’équipe a pu voir quels gènes étaient surexprimés, lesquels étaient sous-exprimés, et comment les messages génétiques étaient assemblés. Cette approche aide à révéler des schémas cachés que les tests génétiques classiques peuvent manquer, comme des modifications de la régulation ou de l’assemblage des gènes.
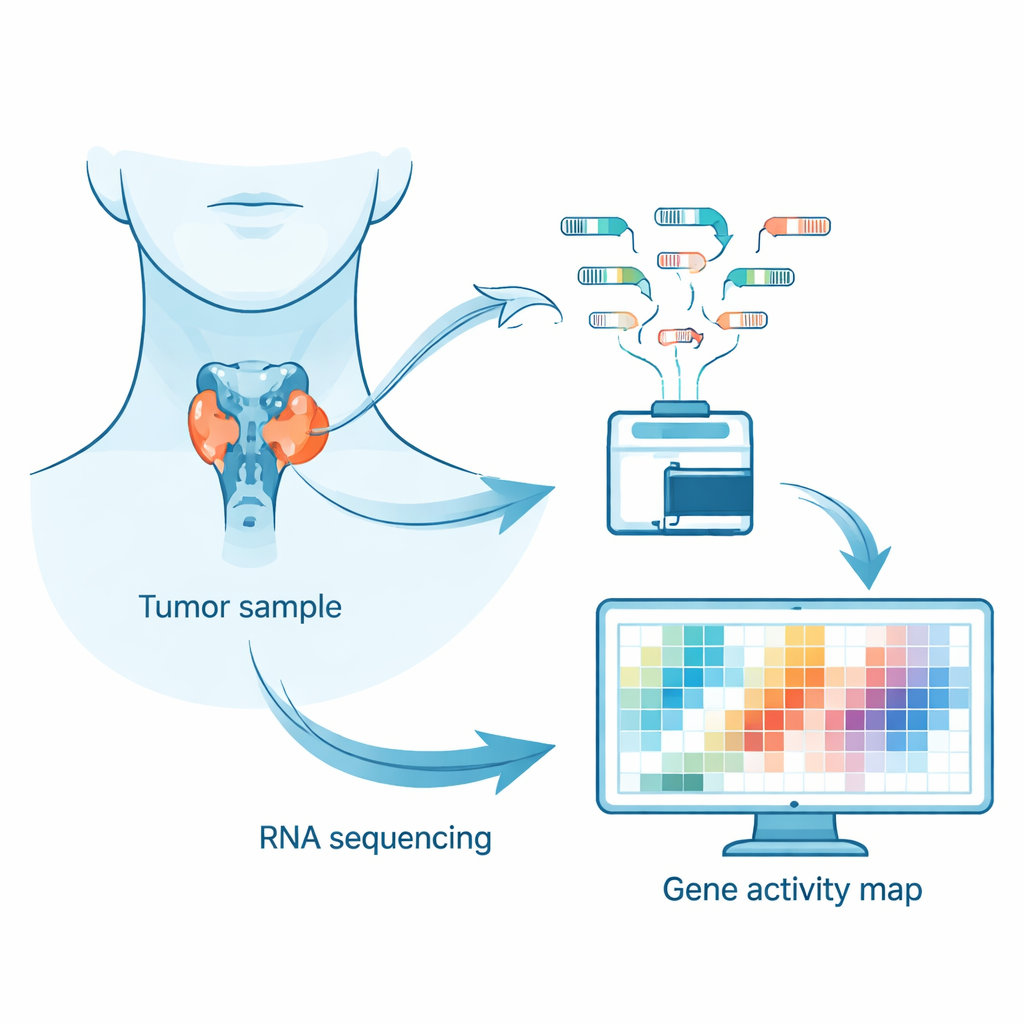
Qui a été étudié et ce qui a été mesuré
L’équipe a analysé les tumeurs de 72 personnes atteintes d’un carcinome médullaire sporadique (non familial). Un peu plus de la moitié étaient des femmes et l’âge médian au moment de la chirurgie était de 61 ans. Environ 58 % des tumeurs présentaient des altérations d’un gène appelé RET et environ 24 % portaient des mutations dans des gènes de la famille RAS, tous deux reconnus comme moteurs de ce cancer. Les scientifiques ont d’abord vérifié que les échantillons tumoraux étaient de haute qualité et relativement peu contaminés par du tissu thyroïdien normal ou des cellules immunitaires en examinant des marqueurs clés tels que la calcitonine, élevée dans ces cancers, et la thyroglobuline, propre aux cellules thyroïdiennes normales et restant faible. Ils ont ensuite utilisé des outils informatiques bien établis pour aligner les lectures d’ARN sur le génome humain, quantifier l’activité génique et rechercher des différences entre groupes cliniques et génétiques.
Activité génique liée au stade et aux mutations
En comparant les tumeurs de stade précoce (stade I–II) avec celles plus avancées (stade III–IV), les chercheurs ont identifié 760 gènes dont les niveaux d’activité différaient nettement entre les deux groupes. Cela signifie que les profils d’expression génique portent des indices solides sur l’avancement du cancer. Ils ont également mis en regard les tumeurs portant des mutations RET ou RAS avec celles ne présentant ni l’une ni l’autre, mettant au jour plus de 1 200 gènes d’activité altérée. Une analyse distincte s’est concentrée sur les tumeurs portant une variation spécifique de RET, appelée M918T, longtemps associée à des pronostics particulièrement défavorables. Dans ces tumeurs, 529 gènes présentaient une activité différentielle comparée aux cancers sans altération de RET, et le gène RET lui-même était plus fortement exprimé, soulignant à quel point cette seule variation modifie le comportement cellulaire.
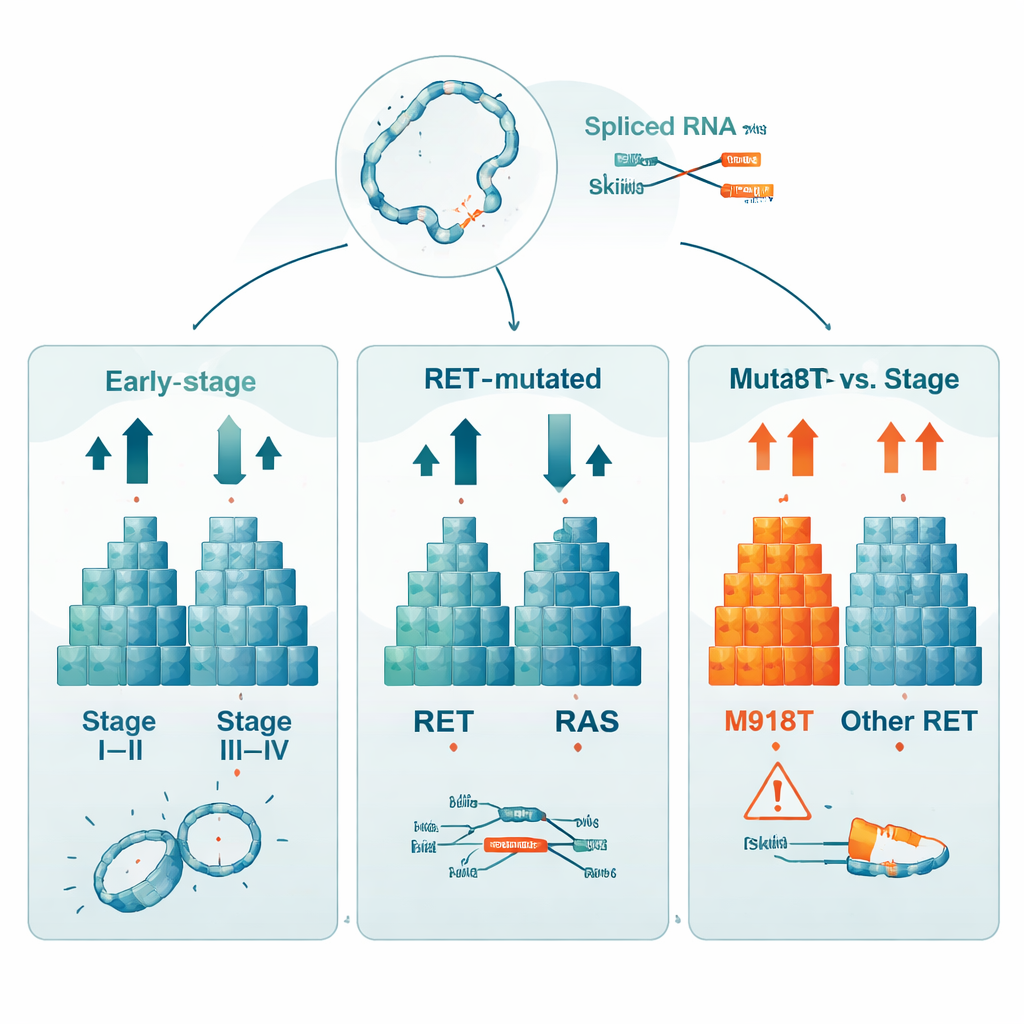
Réarrangements cachés et réécriture des messages
Au-delà des simples variations d’activation des gènes, l’étude a cherché des formes plus profondes de perturbation de l’ARN. L’équipe a détecté 59 transcrits de fusion génique distincts, où des fragments de gènes différents sont anormalement joints au niveau de l’ARN. La plupart étaient rares, et la fusion la plus fréquente pourrait refléter un artefact technique, mais ce catalogue montre que de tels réarrangements peuvent être exploités systématiquement à partir de ces données. Les chercheurs ont également cartographié des milliers d’événements d’épissage alternatif, où des segments des messages génétiques sont sautés, interchangeés ou retenus. Si chaque comparaison clinique (par stade, type de mutation ou statut M918T) présentait des totaux globaux similaires de ces changements d’épissage, les événements spécifiques différaient majoritairement, suggérant plusieurs voies, en partie indépendantes, par lesquelles les cellules tumorales réorganisent leurs messages géniques.
Ce que cette ressource apporte aux patients et aux scientifiques
Pour les patients, ce travail ne se traduit pas encore par un nouveau médicament ou test immédiat, mais il pose des bases essentielles. En rendant l’ensemble des données de séquençage ARN traitées accessibles publiquement, les auteurs fournissent une ressource riche que d’autres chercheurs peuvent exploiter pour découvrir de nouveaux biomarqueurs pronostiques, affiner la classification des carcinomes médullaires thyroïdiens ou repérer des vulnérabilités susceptibles d’être ciblées par de futures thérapies, y compris la nouvelle génération d’inhibiteurs sélectifs de RET. En termes simples, cette étude offre une « carte d’activité » détaillée des gènes tumoraux à travers de nombreux cas réels, donnant aux chercheurs les outils nécessaires pour mieux comprendre pourquoi ce cancer rare se comporte si différemment d’une personne à l’autre et comment les soins pourraient un jour être adaptés de manière plus précise.
Citation: Palumbo, D., Melone, V., Palo, L. et al. Comprehensive Transcriptome Profiling of Sporadic Medullary Thyroid Carcinomas. Sci Data 13, 234 (2026). https://doi.org/10.1038/s41597-026-06550-7
Mots-clés: carcinome médullaire de la thyroïde, génomique du cancer, séquençage ARN, mutation RET, oncologie personnalisée