Clear Sky Science · fr
Le métabolisme de la vitamine B2 favorise la stabilité de FSP1 pour prévenir la ferroptose
Comment une vitamine courante aide les cellules à choisir entre vie et mort
Nos cellules marchent en permanence sur une corde raide entre survie et autodestruction. Une forme spectaculaire de mort cellulaire, appelée ferroptose, a suscité l’intérêt car elle peut tuer sélectivement des cellules cancéreuses résistantes à d’autres traitements. Cette étude révèle qu’un nutriment du quotidien — la vitamine B2, ou riboflavine — incline discrètement la balance en stabilisant une protéine protectrice clé. Comprendre ce lien caché entre alimentation, métabolisme cellulaire et mort des cellules cancéreuses pourrait aider les chercheurs à concevoir des thérapies plus intelligentes et à affiner de futurs conseils nutritionnels.
Une forme particulière de rouille à l’intérieur des cellules
La ferroptose est un type de mort cellulaire piloté par un processus chimique comparable à la rouille des métaux : l’oxydation incontrôlée des lipides des membranes cellulaires. Lorsque ces lipides se dégradent, les membranes perdent leur intégrité et les cellules éclatent. Nos cellules déploient normalement plusieurs défenses pour éviter que cela n’arrive. Un bouclier majeur est une enzyme appelée GPX4, qui utilise une petite molécule, le glutathion, pour détoxifier les peroxydes lipidiques nocifs. Un second bouclier, parallèle, est une protéine nommée FSP1, qui se trouve sur les membranes cellulaires et utilise de petites molécules lipophiles pour intercepter les radicaux destructeurs avant qu’ils ne se propagent. Les cellules cancéreuses augmentent souvent l’expression de FSP1 pour éviter la ferroptose, faisant de cette protéine une cible privilégiée pour de nouveaux médicaments anticancéreux. Pourtant, jusqu’à présent, les scientifiques ignoraient comment les cellules contrôlent la quantité de FSP1 produite et la durée de sa survie.
Construire un « témoin de carburant » cellulaire pour un bloqueur de mort
Pour découvrir les régulateurs cachés de FSP1, les chercheurs ont d’abord modifié des cellules humaines d’ostéosarcome pour y intégrer un rapporteur fluorescent. Ils ont marqué la protéine FSP1 naturelle par un signal vert et l’ont couplée à un signal bleu qui rend compte de la quantité d’ARN messager de FSP1 produite par la cellule. Cette conception astucieuse leur a permis de distinguer les changements d’activité génique (bleu) des changements de stabilité protéique (vert). Avec ce système bicolore en place, ils ont utilisé CRISPR–Cas9 pour perturber systématiquement presque tous les gènes du génome, puis ont trié les cellules présentant des niveaux de FSP1 élevés ou faibles. En comparant les ARN guides enrichis dans chaque groupe, ils ont cartographié des centaines de gènes qui augmentent ou diminuent FSP1, agissant au niveau du contrôle génique ou du renouvellement protéique.
Le rôle caché de la vitamine B2 : créer une poignée stabilisatrice
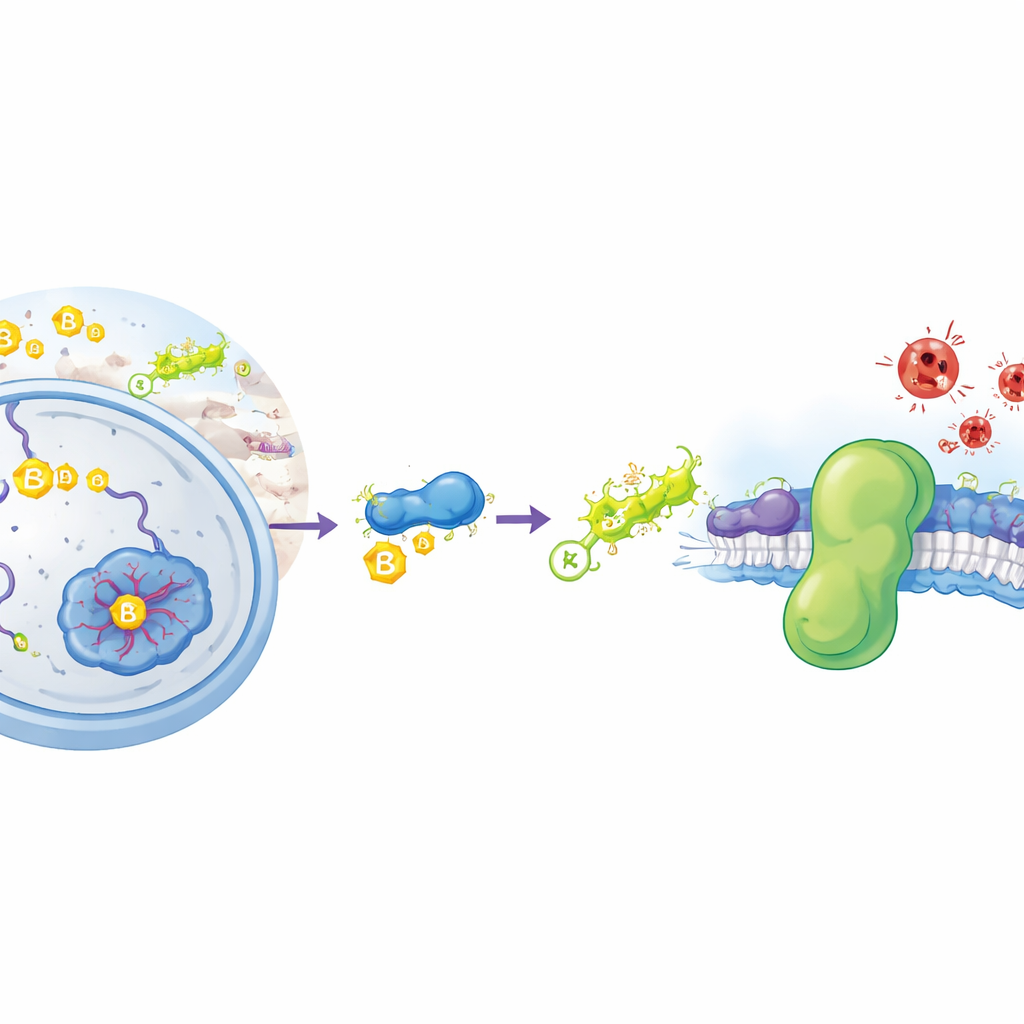
Parmi les découvertes les plus marquantes figuraient deux enzymes, la riboflavine kinase (RFK) et la FAD synthase (FLAD1), qui convertissent la vitamine B2 en un cofacteur appelé FAD. FSP1 est une flavoprotéine qui se lie normalement fermement au FAD pour accomplir ses réactions chimiques. Lorsque RFK ou FLAD1 étaient supprimés, ou lorsque les cellules étaient cultivées dans un milieu dépourvu de vitamine B2, les niveaux de protéine FSP1 chutaient fortement bien que l’activité génique reste similaire. L’équipe a montré que cette perte rendait les cellules beaucoup plus vulnérables à la ferroptose lorsque GPX4 était bloquée. Il est important de noter que la vitamine B2 elle-même n’agissait pas comme un antioxydant classique : dans un test sensible en éprouvette, elle n’a pas empêché l’oxydation des lipides, contrairement à la vitamine E. En revanche, l’ajout de FAD (et en partie de son précurseur FMN) aux cellules déficientes a restauré à la fois les niveaux de FSP1 et la résistance à la mort ferroptotique, tandis qu’un supplément de vitamine B2 seul n’aidait pas si les enzymes de transformation faisaient défaut.
Que se passe-t-il lorsque le cofacteur manque
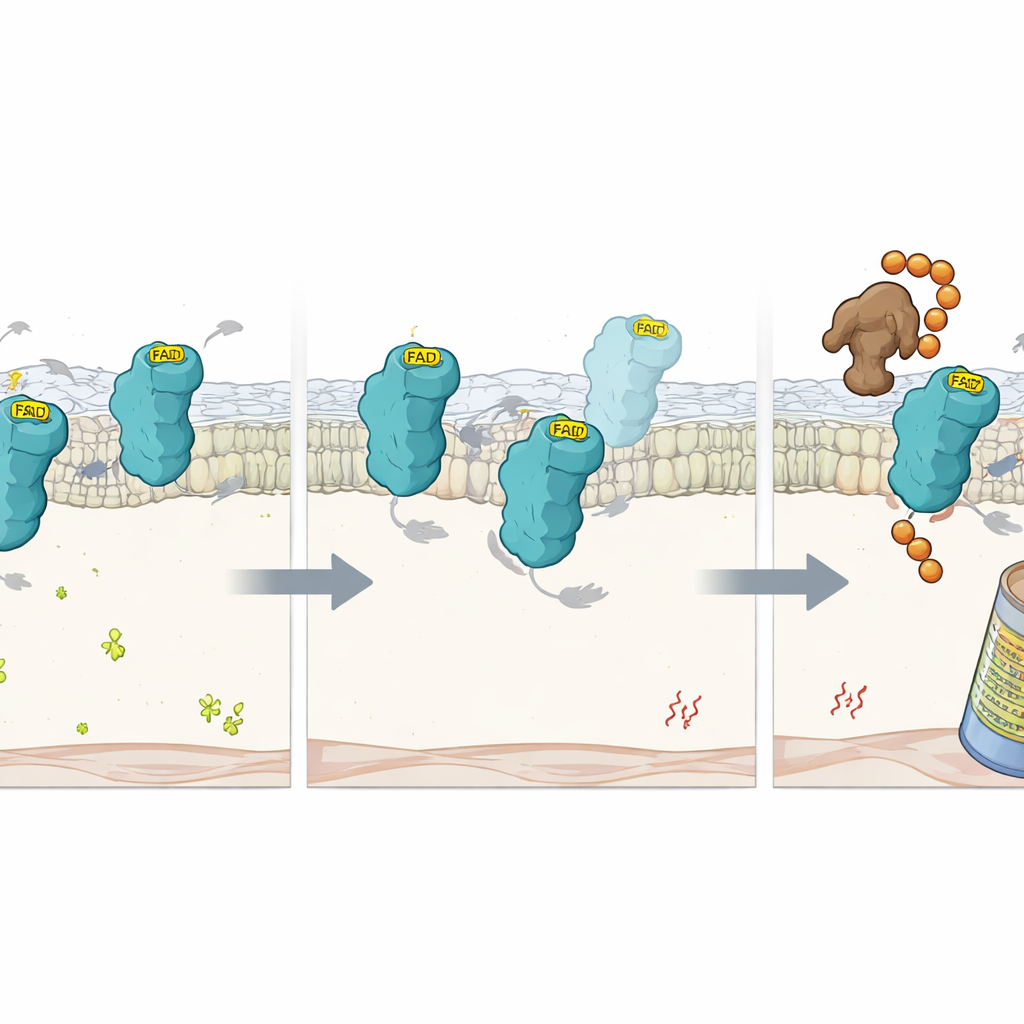
Pour aller plus loin, les scientifiques ont étudié des mutations précises de FSP1 qui empêchent sa capacité à retenir le FAD. Ces protéines mutantes se repliaient encore en formes largement normales mais perdaient leur FAD et leur activité catalytique. À l’intérieur des cellules, elles se dégradaient beaucoup plus rapidement que la FSP1 normale, sauf si le protéasome — la machinerie cellulaire de déchiquetage des protéines — était bloqué. Cela suggère que la liaison au FAD joue elle-même le rôle d’une poignée stabilisatrice qui protège FSP1 d’être signalée comme défectueuse. En utilisant un autre crible CRISPR ciblé dans des conditions de faible FAD, l’équipe a identifié une ligase E3 appelée RNF8 comme facteur clé qui reconnaît la FSP1 dépourvue de FAD. Lorsque RFK était supprimé, RNF8 ajoutait des chaînes d’ubiquitine à la protéine vide, la ciblant pour destruction par le protéasome. Supprimer RNF8 ralentissait le renouvellement de FSP1 dans les cellules pauvres en FAD, bien que cela n’ait pas pu restaurer sa fonction protectrice perdue sans le cofacteur.
De la logique moléculaire aux idées pour la thérapie du cancer
En assemblant ces éléments, les auteurs proposent un modèle simple mais puissant. La vitamine B2, après conversion en FAD par RFK et FLAD1, se lie à FSP1 et est essentielle à la fois pour son activité biochimique et sa longévité. Lorsque l’apport en vitamine B2 ou sa transformation fait défaut, la FSP1 nouvellement synthétisée ne peut pas se sécuriser avec le FAD, est repérée par RNF8 et est rapidement démantelée par le protéasome, laissant les cellules plus exposées aux dommages ferroptotiques. Les données sur le cancer suggèrent que les tumeurs avec une expression élevée de RFK sont plus résistantes aux médicaments inducteurs de ferroptose, soulignant la pertinence de cette voie dans le monde réel. Pour le grand public, le message clé est qu’une vitamine familière fait bien plus que jouer le rôle d’un simple antioxydant : elle contribue à décider si une puissante protéine anti-mort reste en poste ou est éliminée. En modulant le métabolisme de la vitamine B2 ou la stabilité de FSP1, de futurs traitements pourraient mieux exploiter la ferroptose pour éliminer les cellules cancéreuses tout en épargnant les tissus sains.
Citation: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Mots-clés: ferroptose, vitamine B2, FSP1, mort des cellules cancéreuses, métabolisme cellulaire