Clear Sky Science · fr
Cartographie, origine et rôle des chimères élément transposable–gène dans l’amélioration de la plasticité du transcriptome
Passagers cachés dans notre ADN
Une grande partie de notre ADN est constituée d’anciens passagers viraux appelés éléments transposables — des fragments de code génétique qui, autrefois, sautaient d’un endroit à l’autre du génome comme de véritables parasites voyageurs. Cette étude montre que ces vieux fragments viraux ne sont pas de simples déchets silencieux : ils peuvent s’épissurer dans nos propres gènes pour produire des messages hybrides, aider les cellules à s’adapter à des conditions changeantes et parfois alimenter des maladies. En cartographiant ces chimères au cours du développement, du vieillissement et du cancer, les auteurs révèlent une façon surprenante dont l’ADN viral continue de façonner la biologie humaine aujourd’hui.
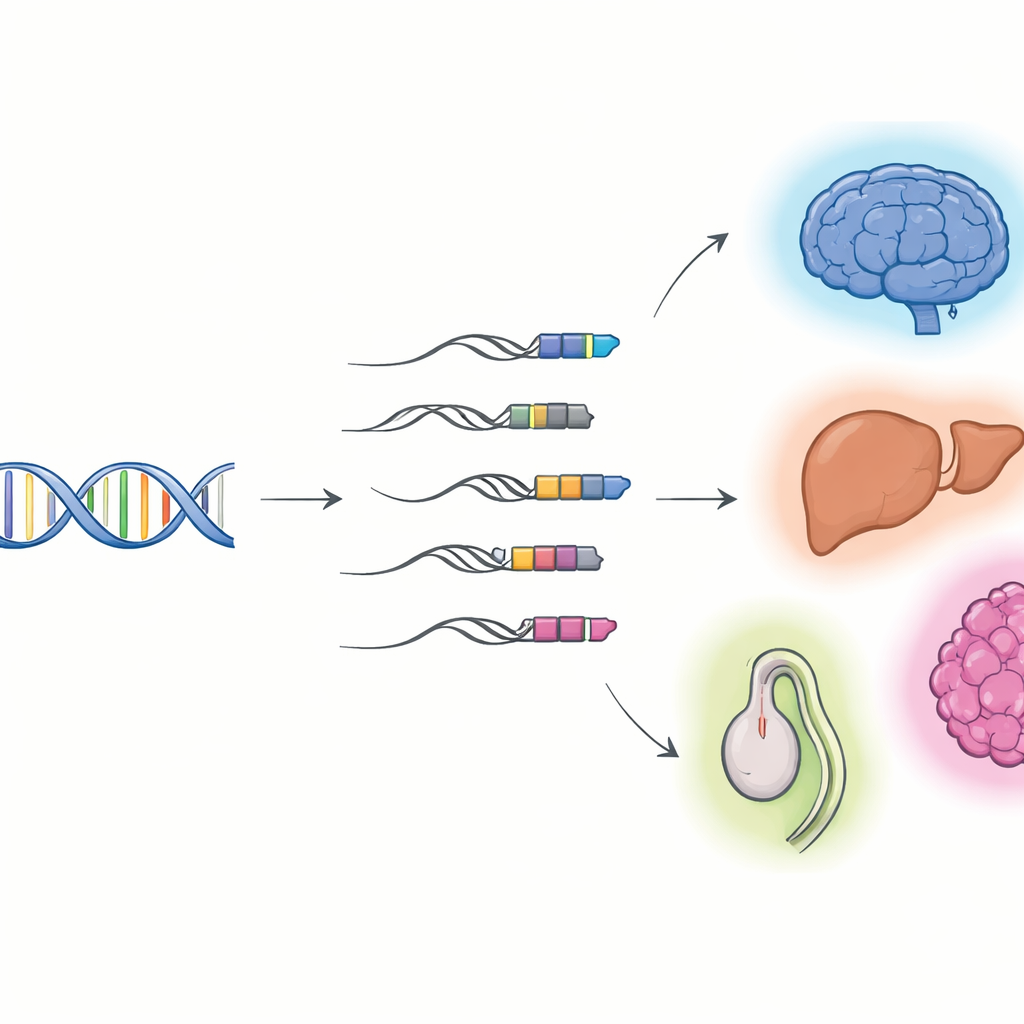
Quand l’ADN viral devient partie intégrante de nos gènes
Les chercheurs se sont concentrés sur les « chimères TE–gène » : des molécules d’ARN qui commencent dans un élément transposable puis se poursuivent dans un gène hôte. En combinant le séquençage long, capable de capturer des molécules d’ARN entières bout à bout, et le séquençage court standard, ils ont établi des catalogues détaillés de ces hybrides dans des cellules et organes de souris et d’humain. Ils ont découvert des milliers de transcrits chimériques jusque-là inconnus, la plupart étant des ARN non codants plutôt que des plans protéiques. Beaucoup commencent dans une classe de vestiges viraux appelés répétitions terminales longues (LTR), qui se situent souvent en amont des gènes et peuvent agir comme des interrupteurs alternatifs marche–arrêt. Différents tissus et organes utilisent des ensembles différents de ces chimères, avec une activité particulièrement riche dans le cerveau, le foie et les testicules, et leur utilisation change au fur et à mesure que les tissus passent des stades fœtal à adulte.
Chimères dans le vieillissement et le cancer
Pour étudier le comportement de ces hybrides viral–hôte dans des populations réelles, l’équipe a exploité de larges jeux de données humains couvrant des dizaines de tissus chez des centaines de personnes, ainsi que des échantillons tumoraux. Ils ont identifié plusieurs centaines de chimères à haute confiance qui réapparaissent chez différents individus. Leur expression varie non seulement entre organes mais aussi avec l’âge : dans des tissus comme le sang et le cerveau, certaines chimères pilotées par des LTR diminuent chez les adultes âgés, tandis que dans certains tissus périphériques elles augmentent. Dans de nombreux types de cancer, ces hybrides basés sur des LTR sont globalement surexprimés dans les tumeurs par rapport aux tissus normaux voisins, et les patients dont les tumeurs en expriment davantage ont tendance à avoir un pronostic plus mauvais. Dans des jeux de données de personnes résistantes à la chimiothérapie ou à l’immunothérapie, les gènes affectés par de nouveaux exons pilotés par des LTR se trouvent souvent dans des voies liées au mode d’action de ces médicaments, suggérant que les chimères TE peuvent aider les tumeurs à se réorganiser sous la pression du traitement.
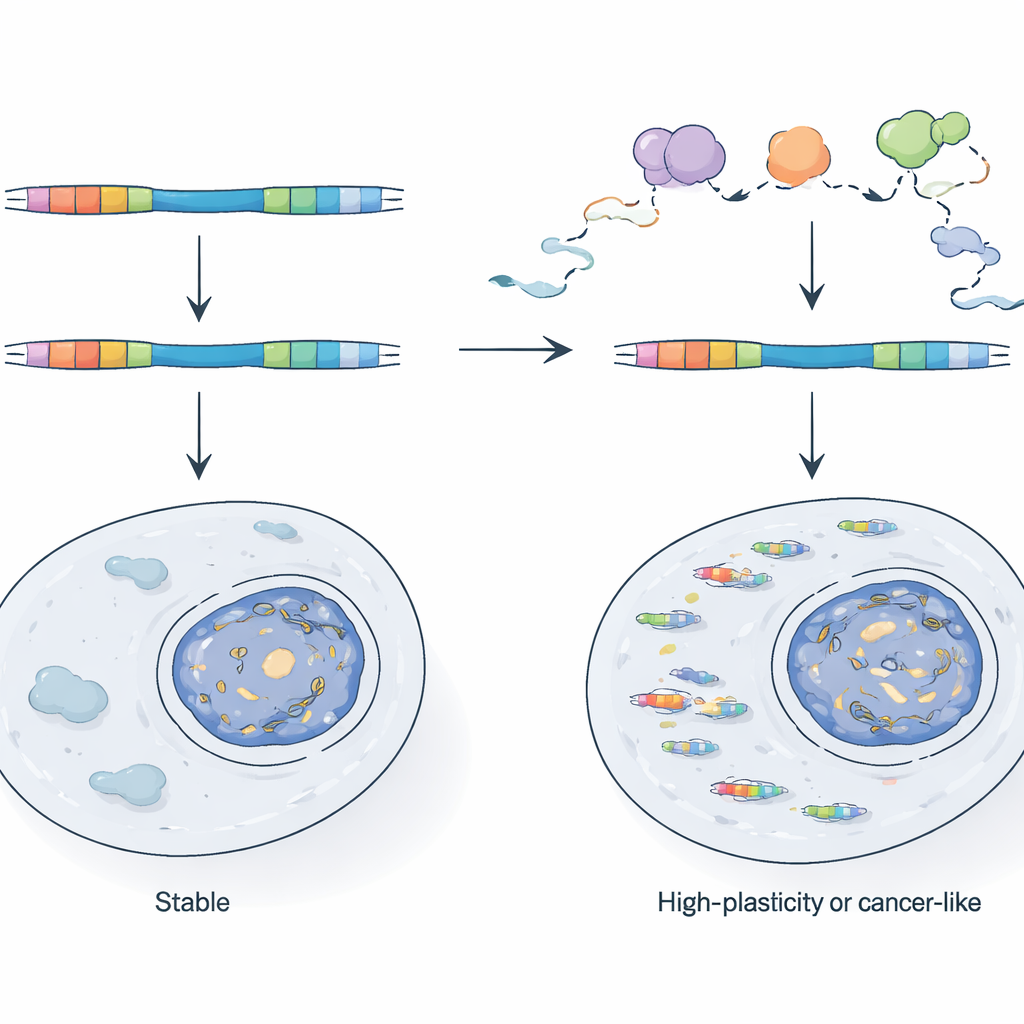
Comment les cellules contrôlent les hybrides viraux
Étant donné leur potentiel, pourquoi les chimères TE n’envahissent-elles pas les cellules normales ? Les auteurs montrent que les cellules s’appuient sur un système de contrôle qualité de l’ARN, centré sur le complexe exosome nucléaire, pour surveiller et détruire nombre de ces transcrits au moment même de leur synthèse. Lorsqu’ils inactivent génétiquement un composant clé de l’exosome dans des cellules souches de souris, les promoteurs pilotés par des LTR deviennent beaucoup plus actifs et les ARN chimériques explosent en nombre. En comparant l’ARN nouvellement synthétisé à l’ARN stable, ils montrent que certains LTR sont normalement contenus parce que leurs transcrits sont rapidement dégradés, tandis que d’autres sont contrôlés au niveau de la fréquence d’initiation de la transcription. Ces LTR actifs ont tendance à se situer dans des régions du génome déjà accessibles et fréquemment transcrites, indiquant que le simple fait d’être proche d’un gène actif ou d’un transcrit antisens peut aider un fragment viral à échapper au silencement épigénétique traditionnel.
Épissage, plasticité des cellules souches et un « interrupteur maître » viral
L’histoire se complique lorsque le dispositif d’épissage de la cellule est perturbé. Les auteurs diminuent l’expression de plusieurs facteurs essentiels de l’épissage ou inhibent chimiquement le spliceosome et observent un résultat commun à la perte de l’exosome : un net accroissement des chimères pilotées par des LTR et des gènes courts, pauvres en introns. Parmi les gagnants figure MERVL, un rétrovirus endogène actif chez les tout premiers embryons de souris. Lorsque la séquence interne de MERVL et ses facteurs de transcription en aval sont surexprimés, les cellules souches basculent vers un état plus proche de la « totipotence », ressemblant aux cellules embryonnaires précoces capables de former tous les tissus. À l’inverse, dégrader l’ARN de MERVL à l’aide d’oligonucléotides antisens réduit cette bascule et diminue l’activité des promoteurs LTR, ce qui indique que MERVL agit comme un interrupteur maître pouvant déclencher un réseau plus large de chimères TE et de plasticité des états cellulaires.
Innovation virale à travers l’évolution
En examinant de nombreux génomes de mammifères, l’équipe retrace quand différentes familles d’TE ont commencé à fournir des exons aux gènes hôtes. Chez l’humain comme chez la souris, des familles de LTR relativement jeunes sont particulièrement susceptibles de former des chimères dans l’orientation « sens » lisible comme partie des transcrits hôtes. Ce schéma suggère que de nouvelles vagues d’insertion de TE ont à plusieurs reprises alimenté les réseaux de régulation génique en matière première au cours de l’évolution. Plutôt que d’être purement nuisibles, ces insertions peuvent être testées par les machineries de transcription et de dégradation de la cellule : la plupart sont silencées ou dégradées, mais une minorité se retrouve au bon endroit et dans le bon contexte pour être réutilisée comme éléments régulateurs utiles ou nouveaux points de départ de gènes.
Pourquoi ces vestiges viraux importent
Pour un non-spécialiste, ce travail montre qu’une large portion de notre génome, autrefois dédaignée, façonne activement la manière dont les gènes sont lus, comment les cellules changent d’identité et comment les maladies évoluent. Des séquences virales anciennes peuvent être transformées en « portes d’entrée » alternatives de gènes, produisant des ARN hybrides normalement surveillés par les systèmes de nettoyage cellulaires. Lorsque cette surveillance ou l’épissage normal fait défaut, ces hybrides peuvent proliférer, poussant les cellules souches vers des états plus flexibles ou aidant les tumeurs à s’adapter et à résister aux traitements. Sur des millions d’années, l’évolution a à plusieurs reprises bricolé avec ces fragments viraux, convertissant bien des parasites génomiques en éléments constitutifs de la complexité régulatrice — et nous laissant un transcriptome bien plus plastique et dynamique qu’une simple liste de gènes ne le suggérerait.
Citation: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Mots-clés: éléments transposables, transcrits chimériques, surveillance de l’ARN, plasticité des cellules souches, évolution du cancer