Clear Sky Science · fr
Adaptation du transport des protéines mitochondriales au stress par dégradation de DNAJC15 médiée par OMA1
Comment nos cellules réagissent quand leurs centrales électriques sont en détresse
Chaque cellule de votre corps dépend de petites structures appelées mitochondries pour transformer les nutriments en énergie utilisable. À la manière de mini‑usines, les mitochondries importent en permanence de nouvelles pièces — des protéines synthétisées ailleurs dans la cellule — pour maintenir leur machinerie en marche. Cet article révèle comment, lorsque les mitochondries sont stressées ou endommagées, la cellule réduit délibérément ce flux d’importation de protéines. Ce freinage la protège d’une surcharge et coordonne une réponse au stress plus large qui implique non seulement les mitochondries, mais aussi un autre compartiment clé : le réticulum endoplasmique.
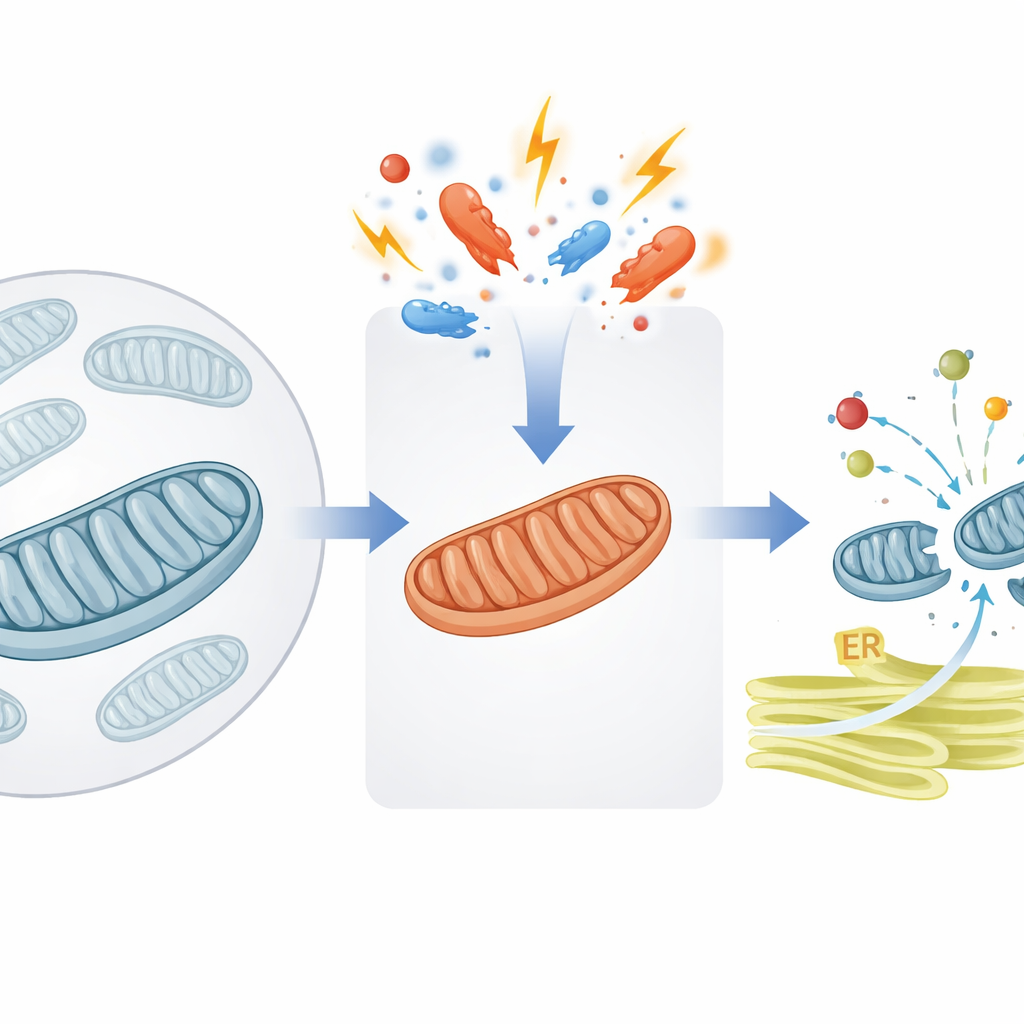
Une soupape de sécurité pour le trafic de protéines mitochondriales
Les mitochondries dépendent de milliers de protéines qui sont d’abord synthétisées dans le compartiment principal de la cellule puis envoyées à l’intérieur de l’organelle. Les auteurs se concentrent sur une porte d’entrée cruciale de la membrane interne mitochondriale, assistée par une protéine d’accompagnement appelée DNAJC15. En conditions normales, DNAJC15 aide à tirer ces « colis » protéiques à travers le canal d’importation et dans l’intérieur mitochondrial, où beaucoup d’entre eux s’intègrent à la machinerie productrice d’énergie connue sous le nom de phosphorylation oxydative (OXPHOS). L’étude montre que lorsque les mitochondries subissent un stress — par exemple une production d’énergie altérée ou des modifications des propriétés membranaires — la cellule active un commutateur moléculaire qui réduit la quantité de protéines que l’organite accepte d’importer.
OMA1 : le ciseau activé par le stress
Au cœur de ce commutateur se trouve une enzyme sensible au stress, OMA1, implantée dans la membrane interne mitochondriale. Lorsque les mitochondries rencontrent des problèmes, OMA1 s’active et clive DNAJC15 à une position spécifique près de son extrémité N‑terminale. Cette coupure produit une version raccourcie de DNAJC15 qui est rapidement dégradée par un autre complexe enzymatique mitochondrial, le protéase m‑AAA. En conséquence, la forme pleine longueur et compétente pour l’importation de DNAJC15 disparaît. Les auteurs montrent que les cellules dépourvues de DNAJC15, ou chez lesquelles DNAJC15 est rapidement détruite après l’activation d’OMA1, présentent une capacité réduite d’apporter de nouvelles protéines dans les mitochondries, en particulier celles nécessaires à la construction et au maintien des complexes OXPHOS.
Ralentir l’assemblage énergétique pour l’aligner sur l’état des mitochondries
Au moyen de mesures protéomiques à grande échelle et d’essais d’importation, l’équipe a constaté que DNAJC15 est particulièrement important pour fournir à l’intérieur mitochondrial des protéines impliquées dans l’expression génétique et l’assemblage de la chaîne respiratoire. En l’absence de DNAJC15, ces protéines s’accumulent plus lentement à l’intérieur des mitochondries, et la capacité des organites à consommer de l’oxygène et à alimenter la production d’énergie — telle que mesurée sur des mitochondries isolées — diminue, en particulier pour le complexe I de la chaîne respiratoire. Un autre composant du canal d’importation, TIMM17A, fonctionne de concert avec DNAJC15 : la perte des deux provoque des défauts particulièrement prononcés dans les niveaux des protéines ribosomales mitochondriales et des composantes de l’OXPHOS. Ensemble, ces résultats suggèrent que la destruction de DNAJC15 médiée par OMA1 constitue un moyen de freiner temporairement la construction de nouvelles machines énergétiques jusqu’à ce que l’organite se rétablisse.
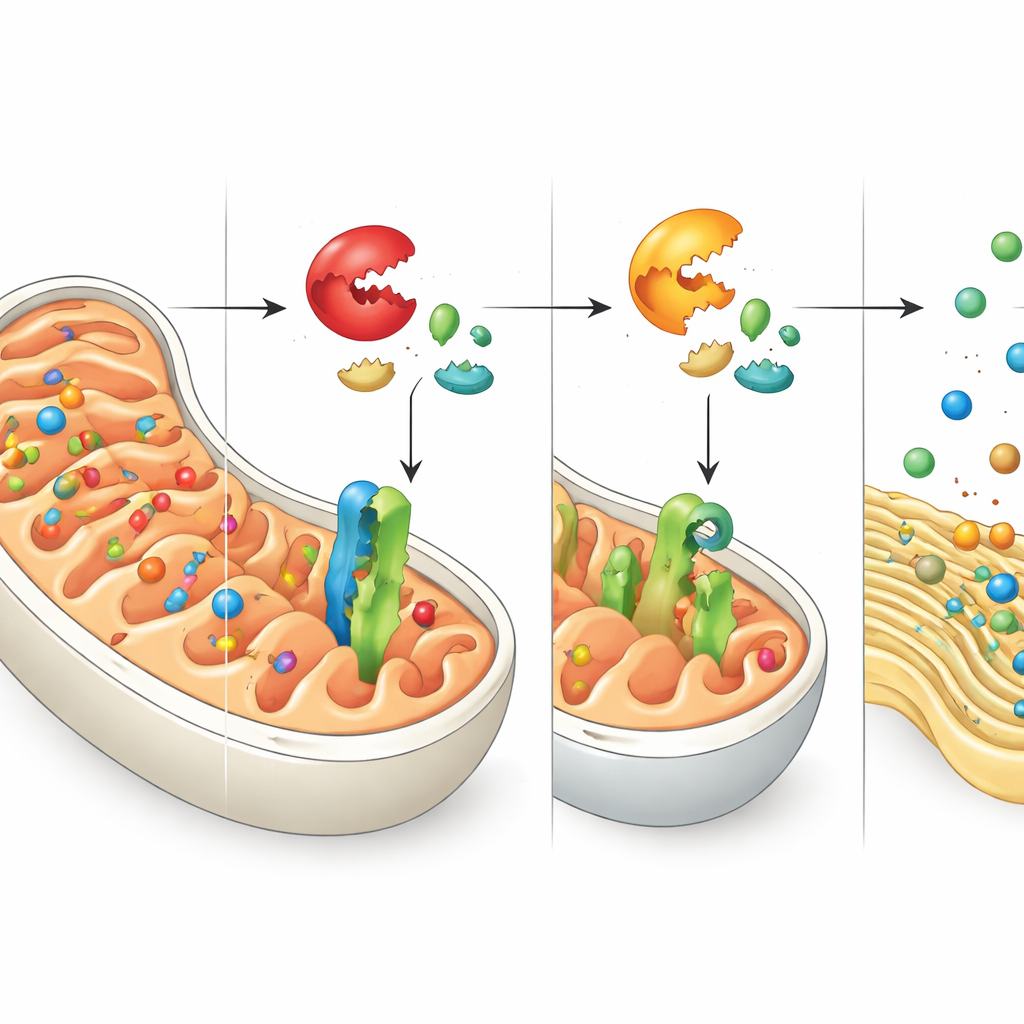
Colis égarés et appel à l’aide adressé au RE
La mise hors circuit de DNAJC15 n’arrête pas la synthèse des protéines mitochondriales par la cellule — elle empêche principalement ces protéines d’atteindre leur destination prévue. Les auteurs ont suivi le trajet de ces protéines abandonnées et ont constaté que beaucoup se retrouvent au niveau du réticulum endoplasmique (RE), un réseau membranaire qui aide normalement au repliement et au traitement d’autres ensembles de protéines. Ces protéines mitochondriales déviées s’intègrent dans les membranes du RE, perturbant l’équilibre du contrôle qualité de ce compartiment. En réponse, la cellule active un programme protecteur connu sous le nom de réponse aux protéines mal repliées, via une branche contrôlée par le senseur ATF6. Cette réponse augmente la capacité du RE à gérer les protéines mal repliées ou mal localisées, révélant une coordination étroite entre les systèmes de stress mitochondriaux et du RE.
Un ralentissement coordonné pour protéger la cellule
Dans l’ensemble, l’étude dresse le portrait d’un système de freinage intégré pour la biogenèse mitochondriale. Lorsque les mitochondries sont stressées, OMA1 rogne et détruit indirectement DNAJC15, réduisant le flux de nouvelles protéines liées à l’énergie vers des organites compromis. Certaines de ces protéines sont temporairement tamponnées au niveau du RE, qui déclenche sa propre réponse protectrice. En couplant la capacité d’importation mitochondriale à l’état de l’organite, et en engageant le RE comme site de secours pour les protéines en excès, les cellules peuvent éviter d’encombrer des mitochondries endommagées et gagner du temps pour les réparer ou les éliminer. Pour un lecteur non spécialiste, ce travail illustre à quel point nos systèmes cellulaires de contrôle qualité sont intégrés : la moindre défaillance dans un compartiment est détectée et compensée par d’autres pour maintenir la production d’énergie — et la vie elle‑même — sur la bonne voie.
Citation: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Mots-clés: stress mitochondrial, importation des protéines, contrôle qualité cellulaire, phosphorylation oxydative, réticulum endoplasmique