Clear Sky Science · fr
Structure et mécanisme de la retron antiphage Eco2
Comment les bactéries utilisent un « autodétruisant » intégré pour lutter contre les virus
Les virus qui infectent les bactéries, appelés phages, sont omniprésents — des océans à notre propre microbiote intestinal. Cette étude révèle comment un petit dispositif génétique présent dans certaines bactéries, nommé retron Eco2, les aide à survivre à une attaque phagique. En dévoilant la structure 3D d’Eco2 et son mode d’activation, le travail explique un nouveau type de défense d’urgence : lorsqu’une infection est détectée, la cellule coupe délibérément sa production protéique pour empêcher la propagation du virus.
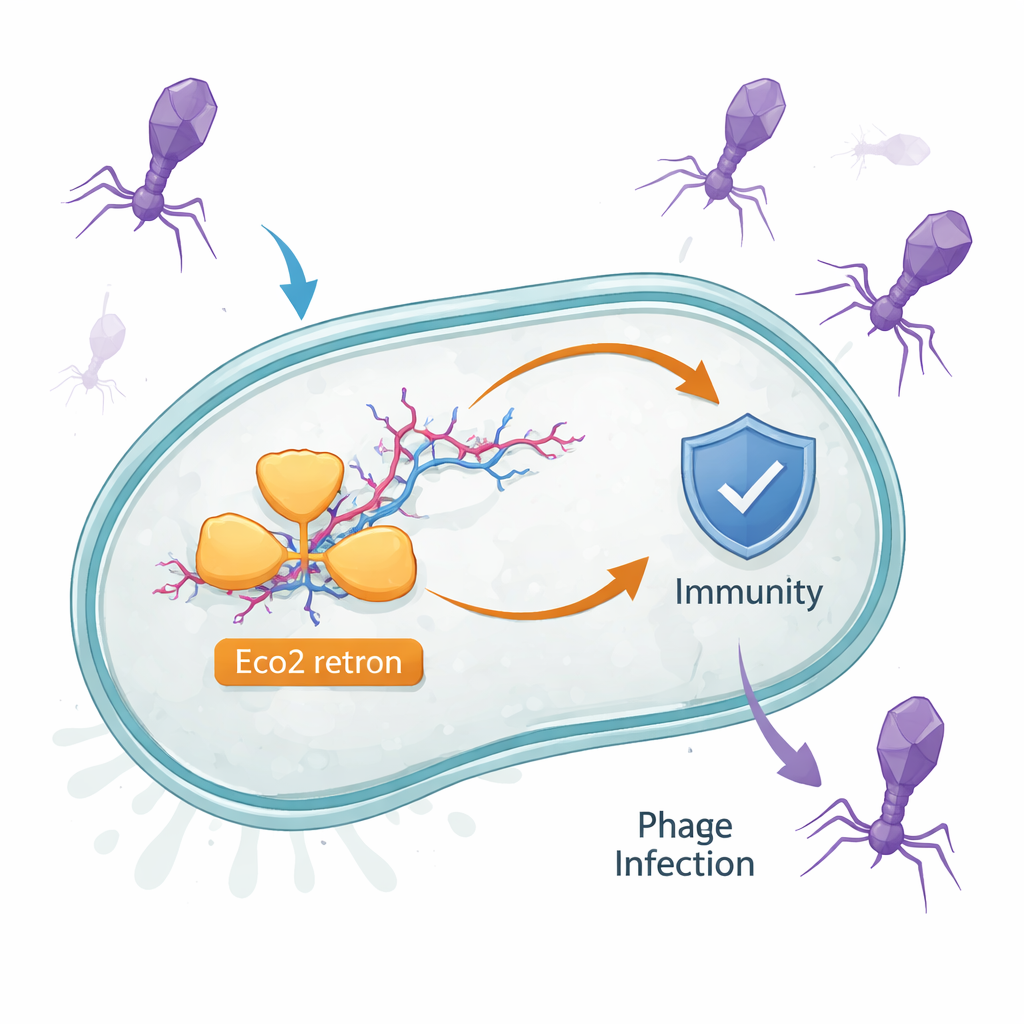
Un gadget ADN–ARN caché dans les cellules bactériennes
Les bactéries possèdent de nombreux petits systèmes de défense qui ne s’activent qu’en cas d’infection. Eco2 est l’un d’eux. Il se trouve chez Escherichia coli et se compose d’une seule protéine qui copie l’ARN en ADN et peut cliver des acides nucléiques. Cette protéine fonctionne avec une molécule étrange appelée msDNA, un hybride d’ARN et d’ADN simple brin qui se ramifie comme une petite brindille fourchue. Des indices antérieurs suggéraient que les retrons comme Eco2 défendent contre les phages, mais on ignorait comment une seule protéine et son partenaire msDNA détectent l’infection et y répondent.
Une protection large contre de nombreux virus
Les chercheurs ont d’abord évalué l’efficacité d’Eco2 face à un large éventail de phages. En exposant des cellules porteuses d’Eco2 à une collection diversifiée de virus, ils ont montré qu’Eco2 bloque de nombreuses familles de phages, mais pas toutes. Quand certains phages parvenaient à échapper à la défense, leurs génomes présentaient des mutations dans des gènes codant des nucléases virales, en particulier une appelée DenB. Ce schéma suggère qu’Eco2 est déclenchée par des nucléases virales spécifiques : quand ces enzymes sont inactivées par mutation, le virus peut contourner la défense.
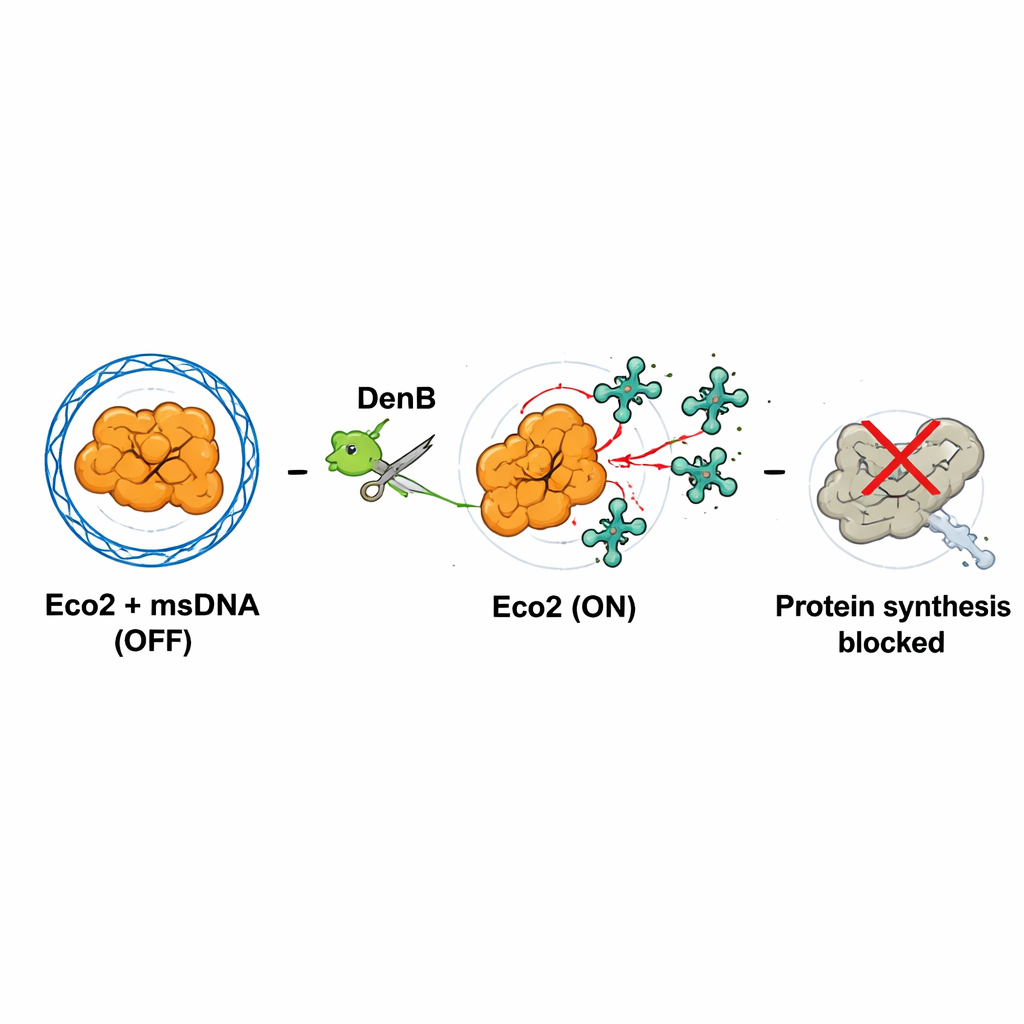
Un bouclier moléculaire à trois bras
Pour comprendre l’architecture d’Eco2, l’équipe a utilisé la cryo‑microscopie électronique pour visualiser le complexe à une résolution proche de l’atomique. Eco2 n’agit pas seul : trois copies de la protéine Eco2 s’assemblent en une structure tripode en forme de shuriken. Le msDNA ramifié s’enroule à travers et autour de ces trois protéines, les reliant entre elles. Ce faisant, le msDNA forme une jonction à trois voies au centre et « encage » physiquement la partie nucléase d’Eco2, obstruant son site de clivage. Des expériences d’échange hydrogène–déutérium, qui mesurent la flexibilité des régions, ont montré que la liaison du msDNA rigidifie et stabilise le complexe. Dans cet état de repos, Eco2 est effectivement verrouillé en position OFF.
L’attaque virale met le système en marche
La clé de l’activation est la destruction du msDNA. L’enzyme virale DenB, qui aide normalement le phage à traiter son ADN, coupe également le msDNA qui enferme Eco2. Les auteurs ont reproduit ce processus avec DenB purifié et une endonucléase standard et ont observé qu’une fois le msDNA sectionné, le site nucléase d’Eco2 devient exposé et se réorganise en une configuration active. Des structures haute résolution de cet « état ON » ont montré qu’un acide aminé critique dans la poche nucléase se déplace en position pour coordonner correctement un ion magnésium, essentiel au clivage de l’ARN. Ainsi, l’activité nucléasique virale, censée remodeler l’ADN de l’hôte, déclenche involontairement le mécanisme de sécurité d’Eco2.
Cliver les ARNt de la cellule pour stopper le virus
Qu’est‑ce qu’Eco2 clive une fois activé ? À l’aide de systèmes cellulaires sans cellules, du marquage radioactif et du séquençage d’ARN lors d’infections réelles, l’équipe a découvert qu’Eco2 nicke principalement les ARN de transfert (ARNt), ces molécules adaptatrices qui apportent les acides aminés au ribosome. Eco2 coupe ces ARNt près de leur extrémité 3’, en particulier à des sites riches en cytosine. Quand de nombreux ARNt sont endommagés, les ribosomes cellulaires ne peuvent plus synthétiser les protéines efficacement. En présence de DenB et d’Eco2 actif, la production de protéine fluorescente verte chute fortement et les ARN bactériens comme viraux sont dégradés. Cet arrêt représente probablement une « infection avortée » : la cellule bactérienne infectée sacrifie sa propre croissance pour empêcher le virus de se répliquer et de se propager.
Pourquoi cela importe au‑delà des bactéries
Ce travail montre comment une retron minimale peut détecter une enzyme virale, basculer d’une forme inactive à une forme active, puis paralyser la synthèse protéique en ciblant les ARNt. Pour le non‑spécialiste, l’idée clé est que les bactéries battent parfois les virus non pas par une précision chirurgicale, mais en coupant l’alimentation de leur propre machinerie cellulaire au bon moment. Outre l’élargissement de notre compréhension de l’immunité microbienne, les structures détaillées d’Eco2 et de son échafaudage msDNA fournissent une feuille de route pour les ingénieurs qui souhaitent réutiliser les retrons comme outils d’édition génomique et de biologie synthétique.
Citation: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Mots-clés: immunité contre les bactériophages, retron Eco2, défense antivirale bactérienne, clivage des ARNt, msDNA