Clear Sky Science · fr
Structure et fonction du supercomplexe détecteur d'acides aminés SEAC–EGOC chez la levure
Comment les cellules décident de croître
Chaque cellule doit en permanence décider si elle peut se permettre de croître ou si elle doit économiser ses ressources. Cette décision dépend fortement des acides aminés, éléments constitutifs des protéines et source importante d’azote. Cet article dévoile, avec un niveau de détail structurel remarquable, comment les cellules de levure détectent la disponibilité des acides aminés via une immense assemblée moléculaire et utilisent cette information pour activer ou désactiver un contrôleur majeur de la croissance, appelé TORC1. Comme la même architecture est conservée chez l’humain et liée au cancer et au métabolisme, les découvertes faites chez la levure offrent une fenêtre sur la manière dont nos propres cellules évaluent si les conditions sont favorables à la croissance.
Un hub complexe au centre de recyclage de la cellule
Chez la levure, un complexe décisionnel central nommé SEAC se situe sur la membrane de la vacuole, un organite qui joue le rôle de centre de recyclage de la cellule. Là, il rencontre un autre complexe, EGOC, qui relaie l’information sur le niveau des acides aminés. Ensemble, ils transmettent des signaux à TORC1, le principal interrupteur de croissance. SEAC comprend deux moitiés fonctionnelles : SEACIT, capable d’éteindre TORC1, et SEACAT, longtemps considérée comme un frein sur SEACIT. Les auteurs ont utilisé la cryo‑microscopie électronique à haute résolution pour visualiser le SEAC complet lié à EGOC, capturant un instantané de ce centre moléculaire précisément là où la signalisation se produit, à la surface de la vacuole. 
Voir l’architecture moléculaire de près
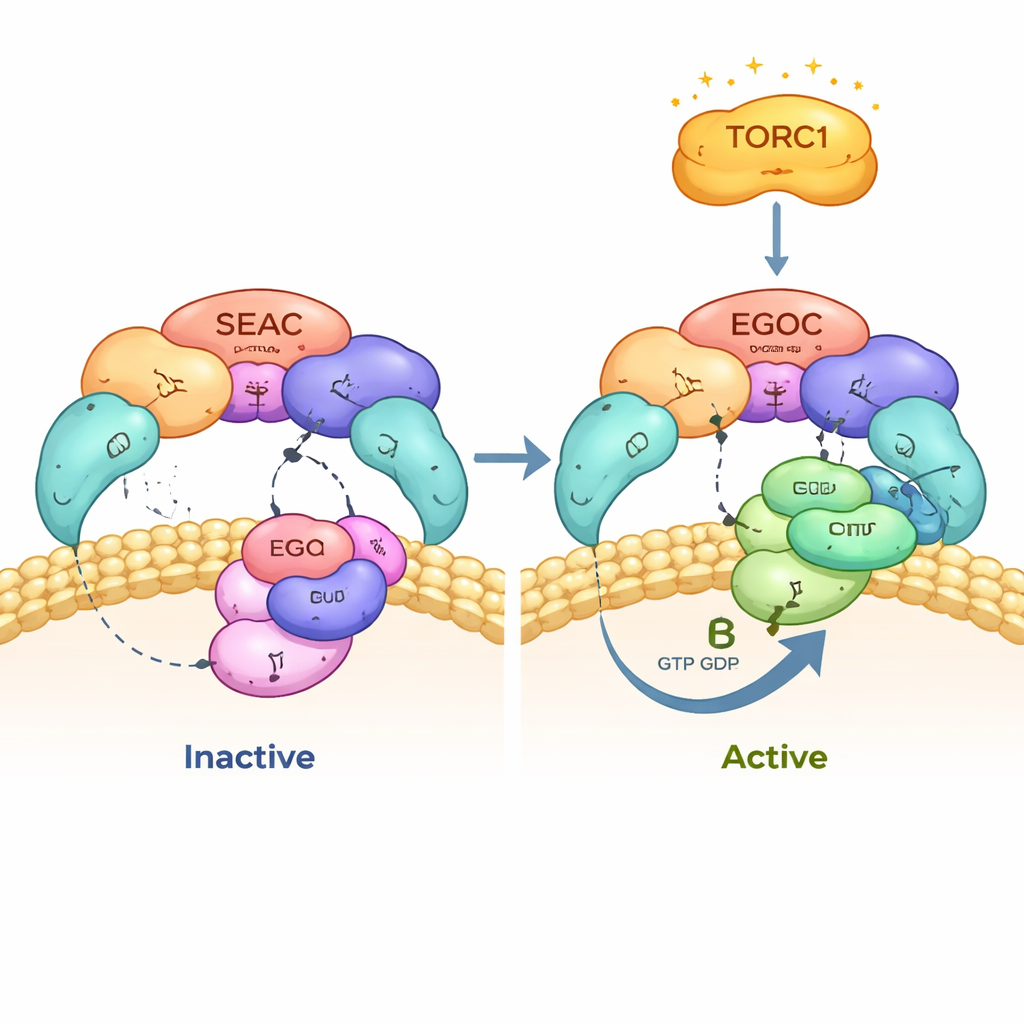
La structure révèle SEAC comme un large noyau composé de sous‑unités SEACAT, d’où s’étendent deux « ailes » flexibles de SEACIT. Chaque aile peut lier un complexe EGOC, ce qui signifie qu’un seul SEAC peut recevoir deux entrées de signalisation simultanément. Fait remarquable, EGOC s’attache uniquement aux ailes et non au noyau, et la forme globale de SEAC change à peine quand EGOC est présent. Cela montre que SEACAT n’obstrue pas physiquement le site actif de SEACIT et n’empêche pas la liaison d’EGOC. L’orientation du complexe sur la membrane de la vacuole place également le noyau de SEAC face au cytoplasme, où il peut interagir avec des régulateurs supplémentaires, tandis que les ailes se trouvent près de la membrane, idéalement situées pour contacter EGOC et d’autres partenaires ancrés à la membrane.
Comment SEAC choisit le bon signal
Les auteurs ont rapproché l’analyse des contacts entre SEAC et EGOC et ont constaté que SEAC reconnaît uniquement la version « active » d’EGOC, dans laquelle l’un de ses petits GTPases, Gtr1, porte un nucléotide de type GTP, tandis que son partenaire, Gtr2, tient du GDP. SEACIT fournit un « doigt » catalytique qui plonge dans la poche du nucléotide de Gtr1 et accélère l’hydrolyse du GTP, basculant EGOC de l’état actif à l’état inactif. Des cartes cryo‑EM détaillées et des expériences mutagènes montrent que ce doigt catalytique et un résidu voisin d’aide sont essentiels pour l’interaction et pour lire correctement l’état du nucléotide. Lorsque les auteurs ont altéré ces résidus clés, SEAC ne se localisait plus correctement à la vacuole et EGOC ne pouvait plus s’engager de façon productive.
Contrôle rapide versus contrôle lent de l’interrupteur de croissance
Pour comprendre ce que cela signifie pour la cellule vivante, les chercheurs ont suivi l’activité de TORC1 au fil du temps lorsque les acides aminés étaient retirés puis réintroduits. Dans des cellules normales, TORC1 s’éteint rapidement en quelques minutes après la privation d’azote, puis se réactive rapidement lorsque les acides aminés reviennent. Lorsque le doigt catalytique de SEACIT était désactivé, ou que des sous‑unités de SEACIT étaient supprimées, TORC1 répondait à peine dans cette fenêtre temporelle précoce. Il en allait de même lorsque Gtr1 et Gtr2 étaient tous deux supprimés, montrant que la paire SEAC–EGOC constitue la voie dominante et rapide pour le contrôle de TORC1 par les acides aminés. Cependant, à des temps plus tardifs—environ une demi‑heure—l’activité de TORC1 s’ajustait lentement même dans ces mutants, indiquant qu’une voie distincte et plus lente vers TORC1, indépendante de ce système de GTPase, opère également dans les cellules.
Un rôle surprenant pour une sous‑unité éloignée
Une découverte particulièrement intrigante concerne Sea2, une composante de SEACAT dotée d’un domaine « hélice » flexible qui dépasse du noyau. La suppression de Sea2, ou seulement de son hélice, produisait des défauts de signalisation presque identiques à ceux observés lorsque l’activité catalytique de SEAC était perdue : TORC1 répondait lentement à la fois au retrait et à la réintroduction des acides aminés. Pourtant Sea2 se trouve loin du site catalytique et ne touche pas directement l’aile SEACIT, rendant un simple mécanisme de blocage improbable. Des expériences génétiques combinant la perte de Sea2 et une variante de SEAC catalytiquement inactive suggèrent que le fait d’avoir l’activité GAP bloquée totalement activée ou totalement désactivée perturbe la réponse rapide, tandis qu’une régulation intermédiaire est nécessaire. Les auteurs proposent que l’hélice de Sea2 serve de plateforme d’ancrage pour un facteur inconnu qui module l’activité de SEACIT, permettant aux cellules d’ajuster finement TORC1 plutôt que de l’éteindre de façon binaire.
Ce que cela signifie pour les décisions de croissance cellulaire
Dans l’ensemble, l’étude reconsidère SEAC non pas comme deux assemblages opposés mais comme une machine unique et intégrée dont l’aile catalytique (SEACIT) et le noyau structural (SEACAT) travaillent de concert pour détecter les acides aminés et ajuster rapidement l’interrupteur de croissance TORC1. L’action enzymatique de SEACIT sur EGOC fournit le contrôle rapide et précis, tandis que l’hélice de Sea2 recrute probablement des régulateurs qui moduleraient cette activité. Parallèlement, des voies lentes et parallèles garantissent que TORC1 finit par refléter l’état nutritif même si le capteur principal est perturbé. Parce que des complexes étroitement apparentés accomplissent la même tâche dans les cellules humaines, ces aperçus obtenus chez la levure éclairent la manière dont nos propres cellules équilibrent la croissance et l’apport nutritif, avec des implications pour la compréhension de maladies où la signalisation TORC1 est déréglée.
Citation: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Mots-clés: détection des acides aminés, signalisation TORC1, complexe SEAC GATOR, contrôle de la croissance cellulaire, cryo-microscopie électronique