Clear Sky Science · fr
Mécanisme et reconstitution de la transcription circadienne chez les cyanobactéries
Pourquoi les horloges biologiques comptent, même chez les bactéries
Tous les êtres vivants, des humains aux micro-organismes, gardent le temps. Ces horloges internes aident les organismes à anticiper le lever et le coucher du soleil, en programmant des activités comme l’alimentation, la réparation et la croissance. Cet article examine comment une bactérie photosynthétique simple, Synechococcus elongatus, utilise une horloge fondée sur des protéines pour activer et désactiver des gènes avec une précision remarquable sur un cycle de 24 heures. En reconstruisant ce système temporel dans une boîte de Pétri, les chercheurs révèlent une version épurée d’une horloge biologique qui pourrait inspirer de nouveaux outils pour la biotechnologie et la biologie synthétique.
Une petite horloge qui fonctionne grâce à la chimie
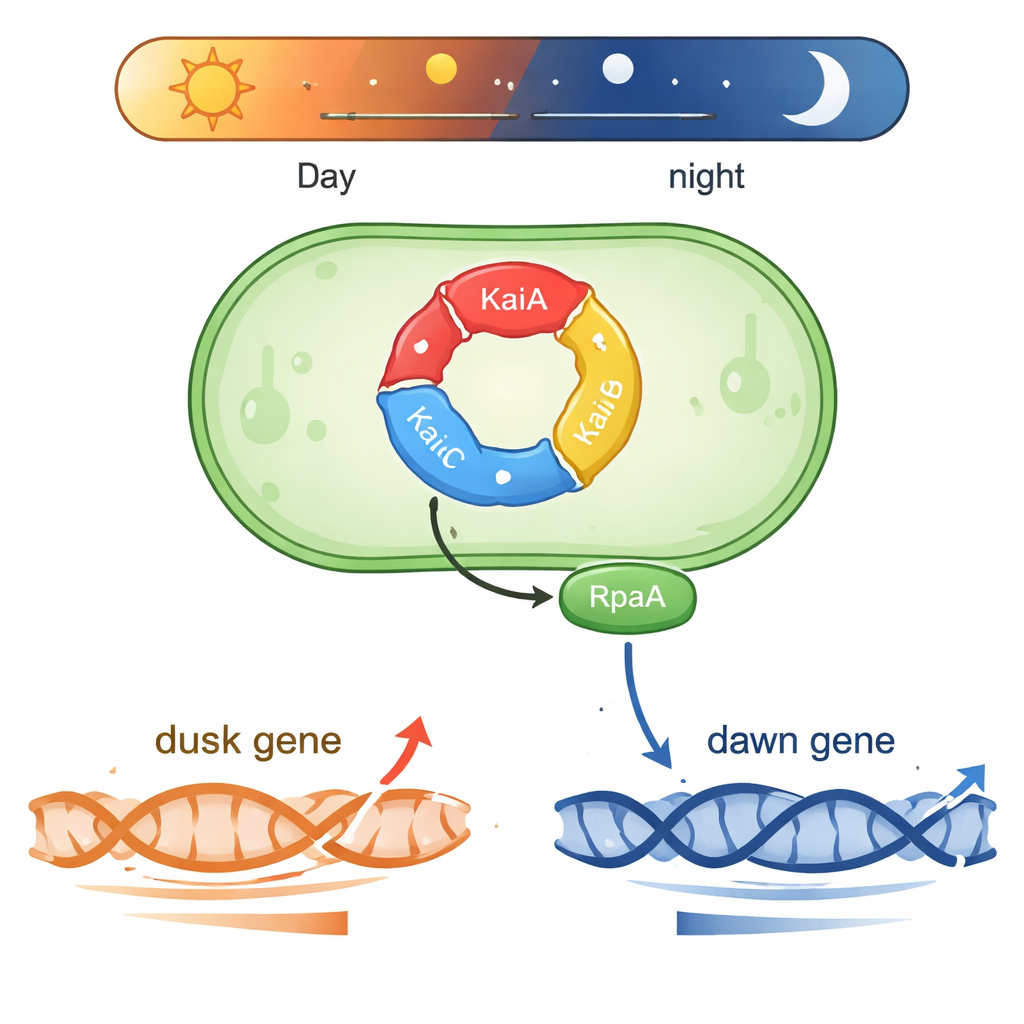
Synechococcus vit dans les eaux éclairées par le soleil et doit prédire les variations quotidiennes de lumière. Au cœur du système se trouve une machine protéique en trois parties composée de KaiA, KaiB et KaiC. Ces protéines échangent des groupes phosphate dans un cycle répétitif d’environ 24 heures, formant un « train d’engrenages » biochimique qui donne l’heure même hors de la cellule. Deux autres protéines, SasA et CikA, lisent l’état de phosphorylation de KaiC et l’utilisent pour contrôler une autre protéine, RpaA. Lorsque RpaA est phosphorylé, il se lie à l’ADN et agit comme un interrupteur maître pour des centaines de gènes qui montent et descendent soit autour du « lever » subjectif, soit autour du « coucher » subjectif en lumière constante.
Une protéine, deux calendriers génétiques opposés
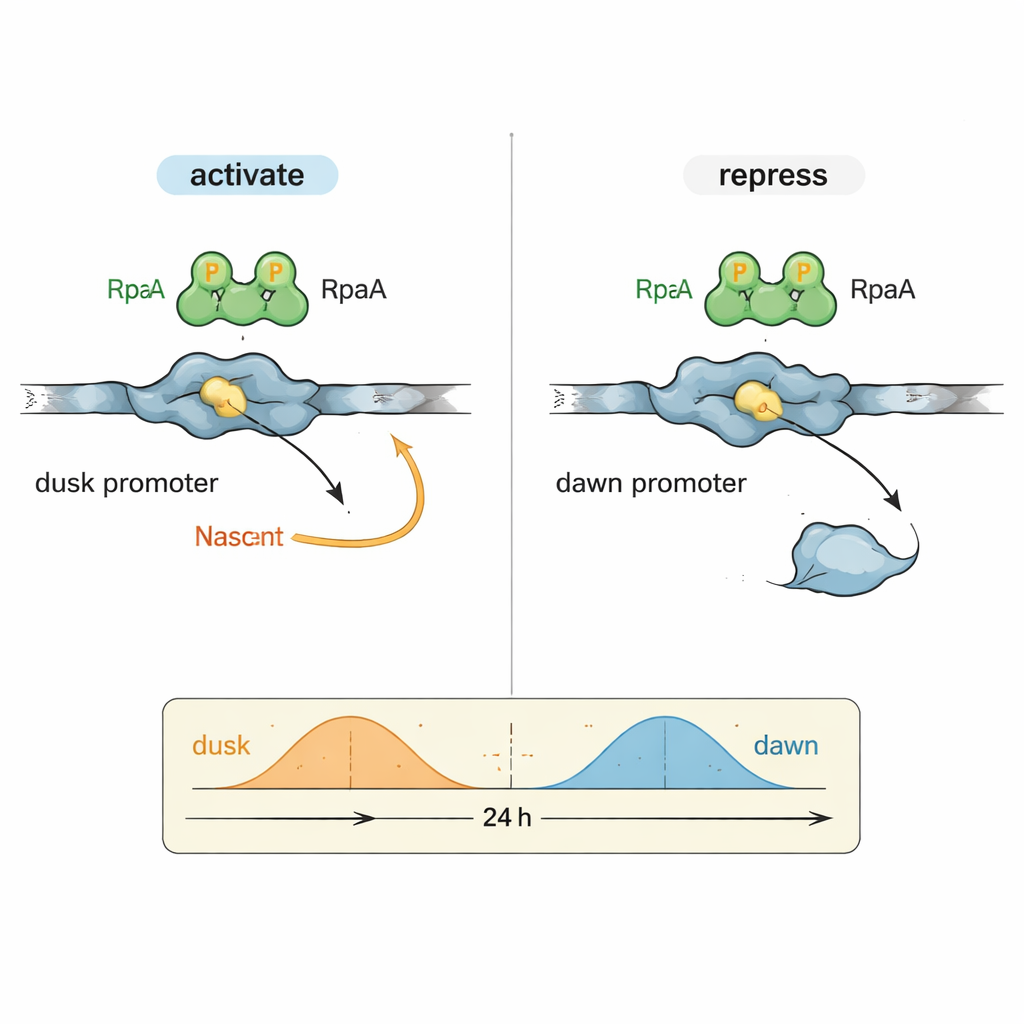
Un casse-tête en biologie circadienne est de savoir comment un seul facteur de sortie, RpaA, peut coordonner des gènes qui culminent à des moments très différents de la journée. Les auteurs se sont concentrés sur deux régions de contrôle de l’ADN représentatives (promoteurs) : kaiBC, qui est le plus actif au crépuscule, et purF, qui atteint son pic à l’aube. Dans des réactions contrôlées utilisant l’ARN polymérase cyanobactérienne purifiée et RpaA, ils ont montré que RpaA phosphorylé stimule la transcription à partir du promoteur kaiBC tout en réduisant simultanément la transcription à partir du promoteur purF. Des expériences de footprinting détaillées ont cartographié précisément où RpaA se lie sur chaque fragment d’ADN, révélant que sa position relative aux éléments promoteurs standards détermine s’il agit comme un accélérateur ou un frein.
Voir l’interrupteur de l’horloge en détail atomique
Pour comprendre ce comportement dual au niveau moléculaire, l’équipe a utilisé la cryo-microscopie électronique à haute résolution pour capturer la structure de RpaA lié au promoteur kaiBC en association avec l’ARN polymérase. Les images montrent RpaA agrippant l’ADN en paire asymétrique et contactant deux parties clés de l’enzyme : la queue de la sous-unité alpha et une région du facteur sigma qui reconnaît normalement les séquences promotrices. Ces contacts courbent l’ADN et aident à positionner l’ARN polymérase à un site de démarrage de la transcription légèrement redéfini. Des mutations soigneusement choisies qui affaiblissent l’un ou l’autre de ces points de contact réduisent ou abolissent l’activation de kaiBC, tant in vitro que dans des cellules vivantes, confirmant que le recrutement physique de l’ARN polymérase sous-tend l’activation des gènes en phase de crépuscule.
Construire un gène contrôlé par l’horloge à partir de rien
Parce que l’ARN polymérase cyanobactérienne native est complexe et difficile à maintenir active pendant des jours, les chercheurs se sont tournés vers l’ARN polymérase beaucoup plus simple du bactériophage T7, largement utilisée en laboratoire. RpaA ne peut pas recruter cette enzyme non apparentée, mais il peut encore la bloquer en restant posé sur l’ADN. L’équipe a conçu un modèle d’ADN synthétique où un promoteur T7 dirige un témoin ARN fluorescent « Broccoli », avec un site de liaison pour RpaA placé en aval. Lorsqu’ils ont combiné ce modèle avec l’horloge KaiA–KaiB–KaiC, la kinase/phosphatase CikA, RpaA et la polymérase T7 dans un tampon optimisé unique, ils ont observé des taux de transcription qui croissaient et décroissaient avec une période d’environ 24 heures. Le rythme pouvait être réinitialisé en changeant le rapport ATP/ADP et se maintenait avec quasiment la même période sur une plage de températures — des caractéristiques classiques d’une véritable horloge circadienne.
D’horloges simples à la chronométrie ingénierée
L’étude montre que seulement six protéines suffisent à relier un pacemaker chimique à une lecture génétique rythmique : les trois protéines Kai, CikA, RpaA et une ARN polymérase. En changeant l’emplacement où RpaA se place sur l’ADN, la même molécule peut faire culminer certains gènes au crépuscule et d’autres à l’aube, aidant à expliquer les vagues complexes d’activité génique observées chez les cyanobactéries. Parce que la conception basée sur la répression fonctionne même avec une polymérase étrangère comme T7, il devrait être possible de transplanter ce module d’horloge minimal dans d’autres microbes ou systèmes sans cellule, permettant aux scientifiques de programmer l’activation et la désactivation de gènes avec des rythmes quotidiens pour la recherche, la production industrielle ou de futures applications thérapeutiques.
Citation: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Mots-clés: horloge circadienne, cyanobactéries, régulation de la transcription, RpaA, biologie synthétique