Clear Sky Science · fr
La céréblon induit la dégradation du néosubstrat G3BP2 en utilisant l’imitation de surface moléculaire
Transformer le nettoyage cellulaire en un système de ciblage intelligent
Les médicaments modernes cherchent de plus en plus à traiter les maladies non seulement en bloquant des protéines problématiques, mais en les éliminant complètement. Cet article explore une manière ingénieuse de reprogrammer l’une des machines de « nettoyage » de la cellule pour qu’elle reconnaisse et détruise, en présence d’une petite molécule, une protéine liée au cancer et à d’autres troubles. Le travail révèle une astuce inattendue : la machine de nettoyage remodèle une partie de sa surface pour imiter un partenaire naturel de la protéine, ce qui lui permet de s’y accrocher et d’envoyer la protéine à la poubelle cellulaire.
Un collecteur de déchets cellulaire à flexibilité cachée
Nos cellules marquent en permanence les protéines usées ou indésirables pour destruction, en s’appuyant sur un système centré sur les ligases E3 — de grands complexes protéiques qui décident ce qui doit être éliminé. L’un de ces complexes repose sur un composant appelé céréblon, qui agit comme un détecteur reconnaissant des caractéristiques spécifiques (« degrons ») sur d’autres protéines. Certains médicaments approuvés exploitent déjà la céréblon en tant que « colles moléculaires » : ils se lient à la céréblon et créent une nouvelle surface d’ancrage qui attire des protéines impliquées dans la maladie, lesquelles sont ensuite marquées et dégradées. Jusqu’à présent, la plupart des cibles connues utilisaient un motif structurel particulier, ce qui laissait penser que la gamme de protéines pouvant être éliminées de cette façon était limitée.
Découvrir une nouvelle cible hors des règles connues
Dans la nouvelle étude, les auteurs ont testé une collection de colles moléculaires ciblant la céréblon dans des cellules humaines et identifié un composé appelé MRT-5702. Cette petite molécule provoque la disparition rapide d’une protéine nommée G3BP2, qui aide à gérer l’ARN et fait partie des granules de stress — assemblages associés au cancer, aux problèmes cardiaques et aux maladies neurodégénératives. Fait important, G3BP2 ne porte pas le motif de degron habituel reconnu par la céréblon. Des expériences cellulaires complémentaires, incluant des mesures sensibles basées sur la lumière de la proximité protéique, ont confirmé que MRT-5702 rapproche la céréblon et G3BP2 en un complexe tripartite conduisant à la dégradation de G3BP2, tout en épargnant sa protéine apparentée G3BP1 sauf si son domaine clé est échangé.
L’imitation comme stratégie de liaison
En creusant plus loin, les chercheurs se sont demandé comment G3BP2 pouvait se lier à la céréblon sans le motif de reconnaissance standard. Plutôt que de chercher des similarités entre G3BP2 et des cibles connues de la céréblon, ils ont inversé la question : la céréblon pourrait-elle ressembler à l’un des partenaires habituels de liaison de G3BP2 ? Les protéines G3BP interagissent souvent avec d’autres molécules via un point chaud situé sur une région appelée domaine de type NTF2, qui reconnaît normalement de courts motifs de séquence. En utilisant des modèles structurels du partenaire naturel de G3BP2, USP10, l’équipe a scanné informatiquement la surface de la céréblon et identifié une zone sur une région moins comprise, le domaine LON, qui imite étroitement la forme et la chimie du motif de liaison d’USP10. La mutation de quelques acides aminés clés sur cette zone, ou dans le point chaud de G3BP2, affaiblit le complexe tripartite, suggérant que la céréblon se fait effectivement passer pour USP10 afin de s’ancrer sur G3BP2.
Capturer la nouvelle interface en détail atomique
Pour visualiser cette interaction inhabituelle, l’équipe a utilisé la cryo‑microscopie électronique à haute résolution pour résoudre la structure d’un complexe contenant la céréblon, un autre composant central de la ligase, MRT-5702, et le domaine de type NTF2 de G3BP2. Les images ont révélé qu’une boucle flexible du domaine LON de la céréblon se replie et se remodela pour former près de la moitié de la surface de contact avec G3BP2. L’énantiomère actif de MRT-5702 s’installe dans la poche habituelle de liaison aux médicaments de la céréblon mais, conjointement avec la boucle, contribue à créer une large plateforme d’accueil qui berce une moitié du dimère G3BP2. De manière frappante, cette organisation n’utilise presque pas le site canonique de la céréblon impliqué pour les cibles des colles précédentes, montrant que la céréblon peut engager des régions très différentes de sa surface selon la colle et la protéine en cause. Parallèlement, l’autre moitié du dimère G3BP2 reste disponible pour lier d’autres partenaires, offrant une voie plausible pour une dégradation « collatérale » de protéines qui seraient attachées.
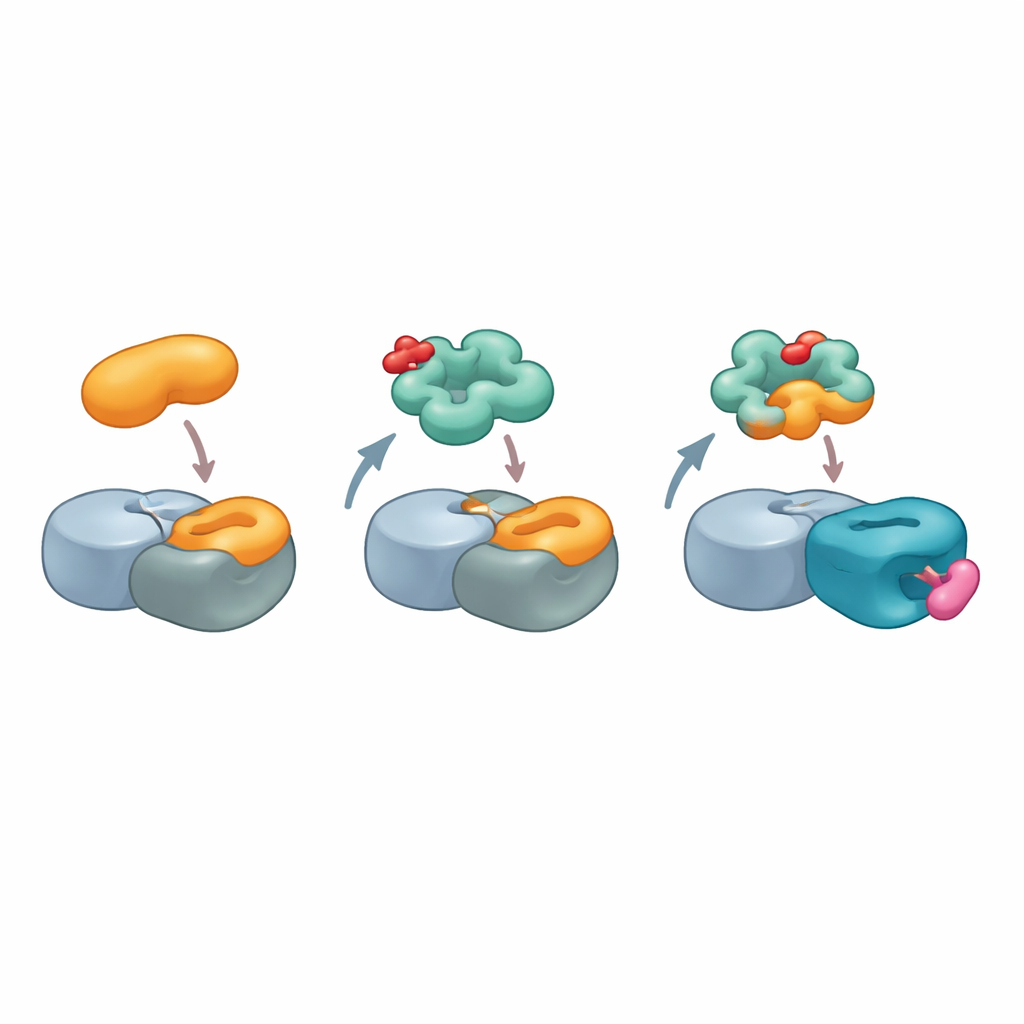
Des « empreintes-colle » pour la conception de médicaments futurs
Pris ensemble, les résultats dressent le portrait d’une céréblon bien plus polyvalente que ce qu’on pensait. Plutôt que d’exiger que les cibles portent un seul type de degron, la céréblon peut, lorsqu’elle est armée de la bonne colle moléculaire, façonner une surface composite qui imite des contacts protéine–protéine naturels ailleurs dans la cellule. Les auteurs proposent que de telles surfaces combinées protéine‑et‑colle, qu’ils appellent des « glueprints » (empreintes‑colle), puissent être cartographiées et conçues pour reproduire des points chauds d’interaction existants sur de nombreuses protéines liées aux maladies. Pour un lecteur non spécialiste, le message clé est que les développeurs de médicaments n’ont peut‑être pas besoin de découvrir de nouveaux sites de liaison sur les protéines problématiques ; ils peuvent plutôt apprendre à la machinerie de recyclage de la cellule à reconnaître ces protéines en copiant astucieusement les formes de leurs partenaires habituels, élargissant fortement le choix de cibles pouvant être éliminées de manière sûre et sélective.
Citation: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Mots-clés: dégradeurs colle moléculaire, céréblon, dégradation ciblée des protéines, G3BP2, interactions protéine–protéine