Clear Sky Science · fr
La signalisation TGFβ médiate la résilience microgliale face à une dégénérescence myélinique spatiale et temporellement restreinte
Pourquoi l’« électricité » du cerveau a besoin de gardiens
Avec l’âge, « l’isolation » autour de nos fibres nerveuses — appelée myéline — s’use naturellement. Cette isolation est essentielle pour une communication rapide et fiable entre le cerveau et le corps. La nouvelle étude examine pourquoi un axe précis de fibres nerveuses dans la moelle épinière, la colonne dorsale, est particulièrement vulnérable à cette usure, et comment un frein immunitaire intrinsèque, une voie de signalisation appelée TGFβ, empêche les lésions de se propager. Comprendre cette protection cachée est important car sa défaillance pourrait aider à expliquer certains troubles de la moelle épinière et influer sur la manière de traiter des maladies cérébrales et des cancers chez les personnes âgées.
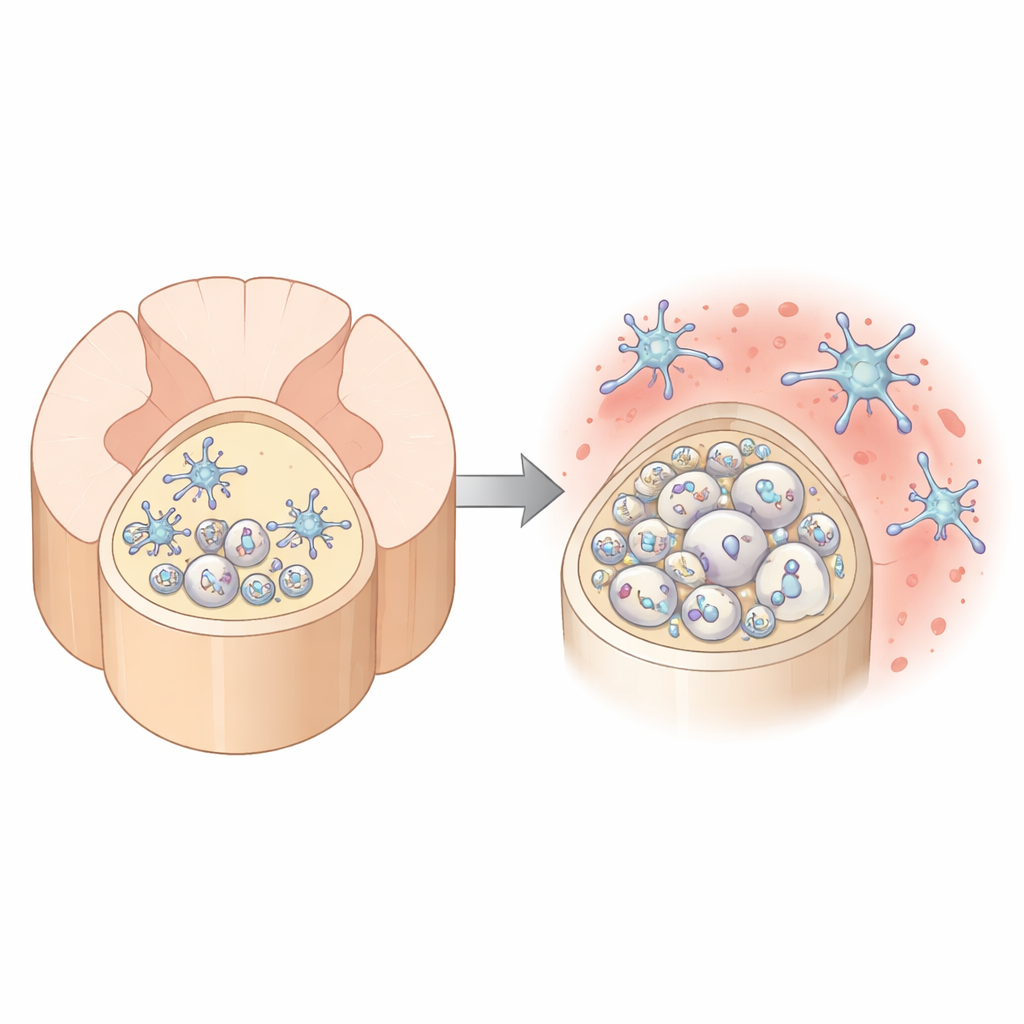
Où le vieillissement frappe le « superautoroute » spinale le plus fort
Les auteurs ont d’abord comparé deux voies majeures de substance blanche dans la moelle épinière de souris : la colonne dorsale à l’arrière et la colonne ventrale à l’avant. À l’aide d’une microscopie électronique haute résolution, ils ont constaté qu’avec l’âge, la myéline de la colonne dorsale devient de plus en plus déformée. Les gaines normalement serrées autour des fibres nerveuses se desserrent, forment des renflements ou se détachent, laissant de larges espaces entre l’axone et son isolation et entraînant une augmentation des ruptures de myéline. En revanche, la colonne ventrale reste relativement stable. La région dorsale contient également beaucoup plus d’axones, mais plus fins, ce qui en fait un environnement particulièrement exigeant pour les cellules qui construisent et entretiennent la myéline.
Des sentinelles immunitaires sous pression croissante
Autour de ces fibres se trouvent les microglies, les cellules immunitaires résidentes du cerveau et de la moelle épinière. Elles patrouillent en permanence les tissus, débarrassent les débris et ajustent finement les connexions. À mesure que la myéline de la colonne dorsale se dégrade avec l’âge, ces microglies commencent à changer d’aspect et de comportement : elles régulent à la hausse des gènes liés à l’activation immunitaire, accumulent des gouttelettes lipidiques à l’intérieur et montrent des signes d’avoir englouti davantage de myéline endommagée. Parallèlement, l’environnement tissulaire de la colonne dorsale se trouve fortement enrichi en TGFβ1, une molécule de signalisation connue pour maintenir les microglies dans un état restraint et protecteur de l’homéostasie. Les microglies elles‑mêmes sont la principale source de ce TGFβ1, ce qui suggère qu’elles tentent de se contenir alors même que les signaux de stress augmentent.
Que se passe‑t‑il quand le frein de sécurité lâche
Pour évaluer l’importance de ce frein, les chercheurs ont désactivé génétiquement la signalisation TGFβ spécifiquement dans les microglies de souris adultes, soit en supprimant le récepteur qu’elles utilisent pour détecter le TGFβ, soit en les empêchant de produire TGFβ1. Dans les deux cas, le résultat fut remarquablement similaire et très localisé : les microglies de la colonne dorsale sont devenues surabondantes, fortement activées et ont pris un aspect mousseux rempli de myéline ingérée. La myéline dans cette région a été arrachée, les axones présentaient des signes de dégénérescence et les souris ont développé des troubles moteurs et de coordination qui s’aggravaient, en particulier avec l’âge. D’autres régions de la moelle épinière ont été beaucoup moins affectées, révélant une dépendance région‑spécifique à cette voie.
Un sous‑type microglial particulier et des oligodendrocytes stressés
Le séquençage ARN nucléaire simple noyau a permis à l’équipe de dresser un catalogue des types cellulaires au fur et à mesure de la maladie. Ils ont découvert un sous‑ensemble distinct de microglies — appelées microglies sensibles au TGFβ — qui s’est développé de façon spectaculaire lorsque la signalisation TGFβ a été supprimée. Ces cellules exprimaient de hauts niveaux de gènes associés à de fortes réponses inflammatoires, à une intense phagocytose de myéline et à la gestion des lipides, et elles étaient concentrées dans la colonne dorsale. Parallèlement, la population de cellules formant la myéline mature, les oligodendrocytes, a changé. Les sous‑types sains ont décliné, tandis qu’un groupe d’oligodendrocytes « associés à la maladie » s’est étendu dans la colonne dorsale endommagée mais n’a pas réussi à reconstruire une myéline fonctionnelle, laissant les axones exposés malgré une tentative apparente de réparation.
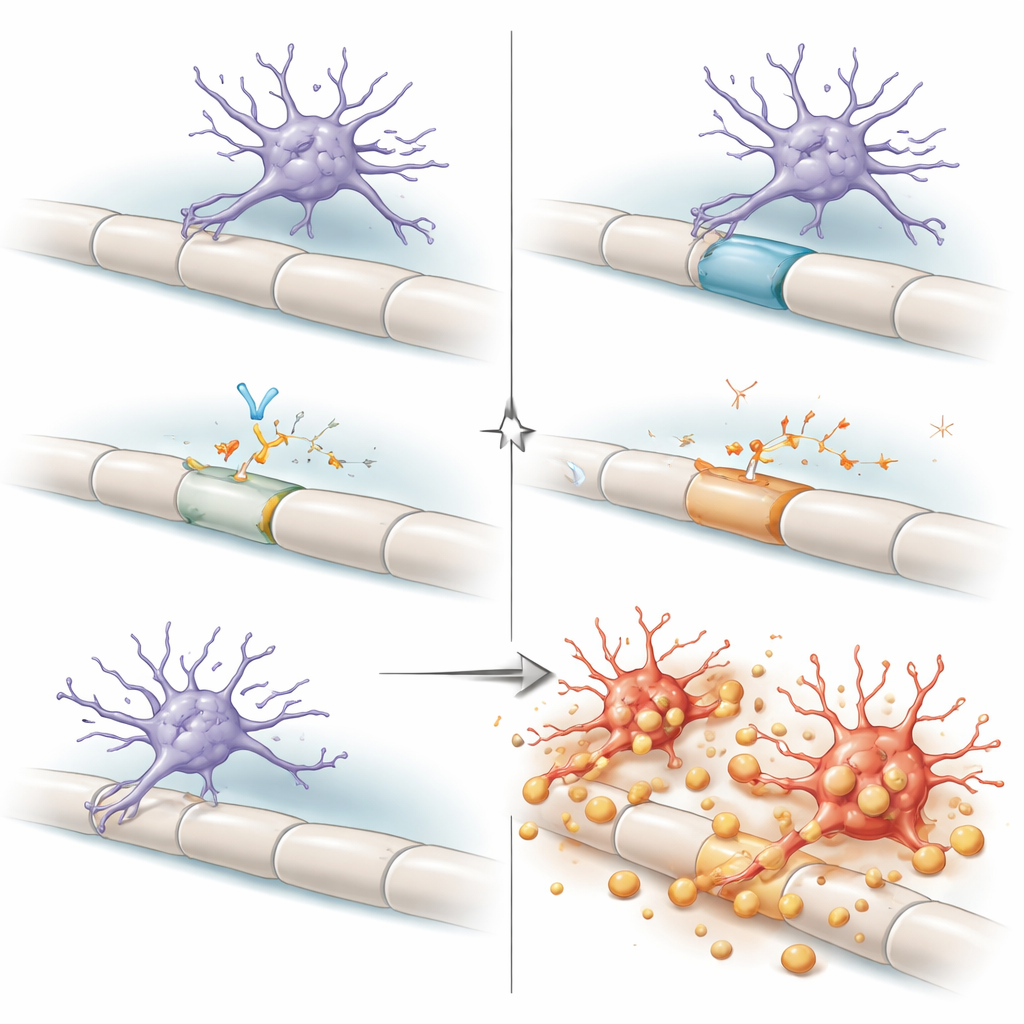
Conséquences pour le vieillissement et perspectives thérapeutiques
Dans l’ensemble, ces résultats décrivent la colonne dorsale comme un quartier à haute pression où la myéline vieillissante et des cellules de soutien surmenées poussent les microglies vers un point de basculement. Dans des conditions normales, une boucle autocrine — les microglies produisant et détectant leur propre TGFβ1 — les maintient dans un état « préparé mais résilient », capable de gérer les débris sans attaquer la myéline relativement intacte. Lorsque cette boucle est rompue, les microglies basculent en mode inadapté, arrachant agressivement la myéline et entraînant un déclin neurologique. Pour le grand public, le message clé est que les cellules immunitaires du cerveau ne sont pas simplement bonnes ou mauvaises ; leur comportement dépend fortement des exigences locales du réseau et de freins moléculaires comme le TGFβ. Étant donné que des médicaments bloquant le TGFβ sont en cours de développement pour le cancer et certaines maladies cérébrales, ce travail lance un avertissement important : perturber cette voie, surtout chez les personnes âgées, pourrait involontairement endommager des régions vulnérables de la moelle épinière en déchaînant les microglies contre l’isolation dont nos nerfs ont besoin pour fonctionner.
Citation: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Mots-clés: microglie, vieillissement de la myéline, colonnes dorsales de la moelle épinière, signalisation TGF bêta, neuroinflammation