Clear Sky Science · fr
Indicateurs multicolores de nouvelle génération pour l'imagerie in vivo de la noradrénaline
Voir un messager cérébral caché
La noradrénaline est une molécule du cerveau qui façonne discrètement notre éveil, notre attention, la formation des souvenirs et la réponse au stress. Jusqu'à récemment, les scientifiques ne pouvaient l'apercevoir qu'avec des outils lents ou imprécis. Cet article présente une nouvelle paire de marqueurs lumineux qui permet aux chercheurs d'observer la montée et la baisse de la noradrénaline dans le cerveau vivant, en temps réel et avec un grand niveau de détail. Ces avancées pourraient approfondir notre compréhension du sommeil, de l'anxiété, de l'apprentissage et des maladies neurodégénératives.
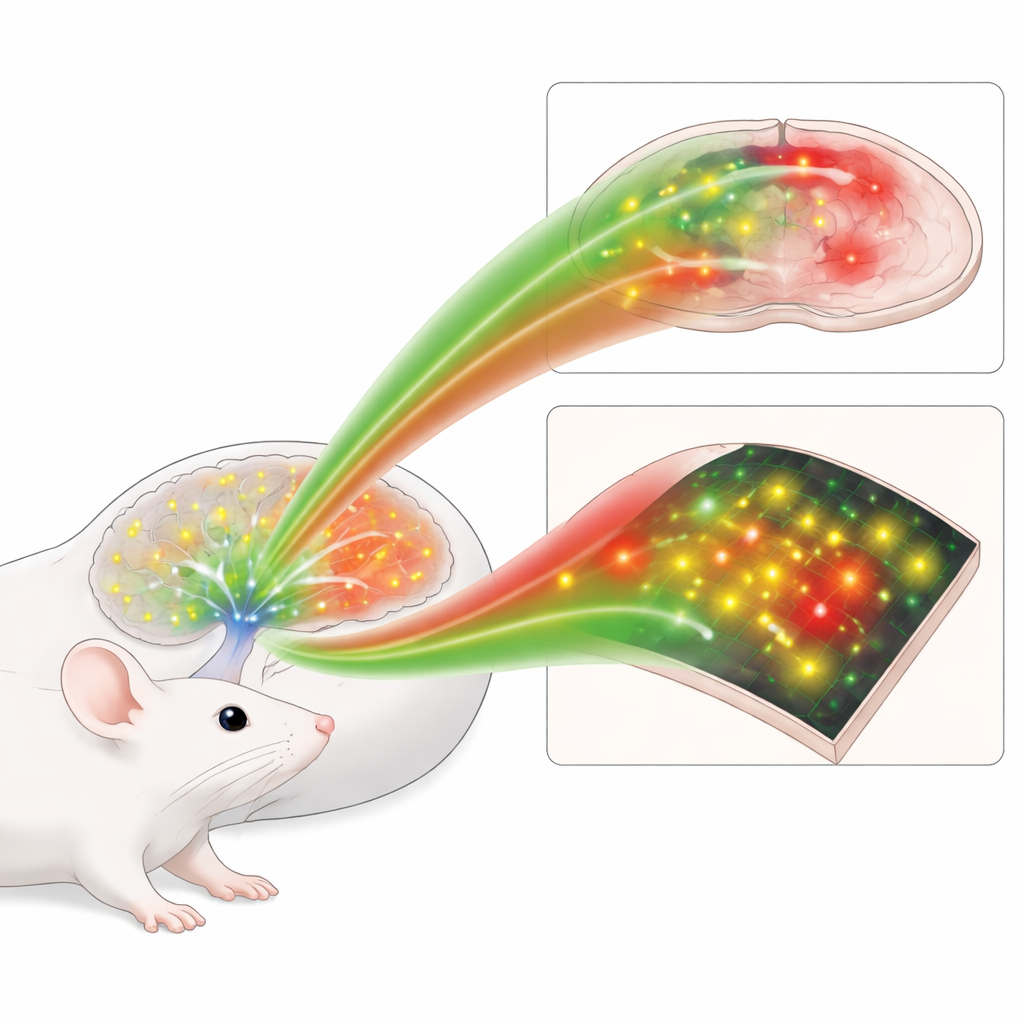
Pourquoi le suivi de ce signal a été si difficile
La noradrénaline est libérée par un petit groupe de cellules du tronc cérébral qui envoient des fibres dans tout le cerveau, modulant le comportement des circuits plutôt que de simplement les activer ou les désactiver. Les méthodes classiques de mesure, comme de minuscules sondes chimiques ou des cellules implantées qui répondent à la noradrénaline, estompent soit les événements sur plusieurs secondes, soit ne la distinguent pas clairement des molécules voisines. Une stratégie plus récente utilise des récepteurs modifiés à la surface cellulaire qui s'éclaircissent lorsqu'ils lient la noradrénaline, permettant une lecture optique. Mais les premières versions étaient relativement peu lumineuses, en particulier dans la partie rouge du spectre, et manquaient de flexibilité pour des expériences nécessitant la combinaison de plusieurs couleurs.
Construire des sentinelles vertes et rouges plus lumineuses
Les auteurs ont conçu des indicateurs verts et rouges améliorés, nommés nLightG2 et nLightR2, en combinant des éléments de capteurs de dopamine et de noradrénaline antérieurs et en testant systématiquement des dizaines de mutations. Ces modifications ont rendu les capteurs beaucoup plus lumineux en présence de noradrénaline, sans modifier fortement leur éclat de base. En culture cellulaire, les nouveaux outils ont montré des réponses plusieurs fois supérieures à la noradrénaline par rapport aux versions précédentes, ont réagi en quelques dizaines de millisecondes et se sont réinitialisés en moins d'une seconde. Ils ont également très peu réagi à d'autres neurotransmetteurs, comme la dopamine, et n'ont pas activé les voies de signalisation internes des cellules — un contrôle de sécurité important pour s'assurer qu'ils observent plutôt qu'ils n'interviennent.
Démontrer leur puissance dans le tissu cérébral
Ensuite, l'équipe a introduit les capteurs dans des coupes de cerveau de souris et a utilisé la microscopie deux-photons, qui peut pénétrer profondément dans le tissu, pour comparer les conceptions anciennes et nouvelles. Lorsque la noradrénaline était insufflée sur le tissu, ou lorsque des fibres locales étaient stimulées électriquement pour la libérer naturellement, nLightG2 et nLightR2 produisaient des éclairs beaucoup plus importants et plus facilement détectables que les capteurs antérieurs. Les outils vert et rouge ont eu des performances temporelles similaires, ce qui signifie que le choix de la couleur n'impose plus de compromis sur la vitesse. Cette sensibilité accrue a permis aux chercheurs de cartographier la diffusion spatiale de la noradrénaline, plutôt que de savoir simplement qu'elle avait été libérée quelque part dans le champ de vue.
Observer les états cérébraux, la peur et la navigation en action
La vraie promesse de ces outils réside dans les animaux vivants. À l'aide de fibres optiques d'un cheveu d'épaisseur, les auteurs ont combiné l'indicateur rouge de la noradrénaline avec un capteur vert du calcium qui rend compte de l'activité des neurones. Dans le centre du sommeil du cerveau, ils ont observé que des rafales d'activité des cellules productrices de noradrénaline pendant le sommeil profond étaient étroitement suivies par des augmentations locales de noradrénaline, événement par événement. Dans l'amygdale, une région impliquée dans les émotions, le capteur vert de la noradrénaline a révélé qu'un son inoffensif en venait à déclencher une augmentation soutenue de la noradrénaline une fois associé à un léger choc, reflétant le renforcement des souvenirs de peur. Dans l'hippocampe, qui aide à cartographier l'espace, le capteur rouge a été imagé en même temps qu'un capteur de calcium astrocytaire vert pendant que les souris couraient dans un couloir virtuel pour obtenir de l'eau. Là, l'activité des astrocytes près d'un site de récompense était étroitement liée aux surgissements locaux de noradrénaline, suggérant un dialogue entre ce neuromodulateur et les cellules de soutien lors d'expériences récompensantes.
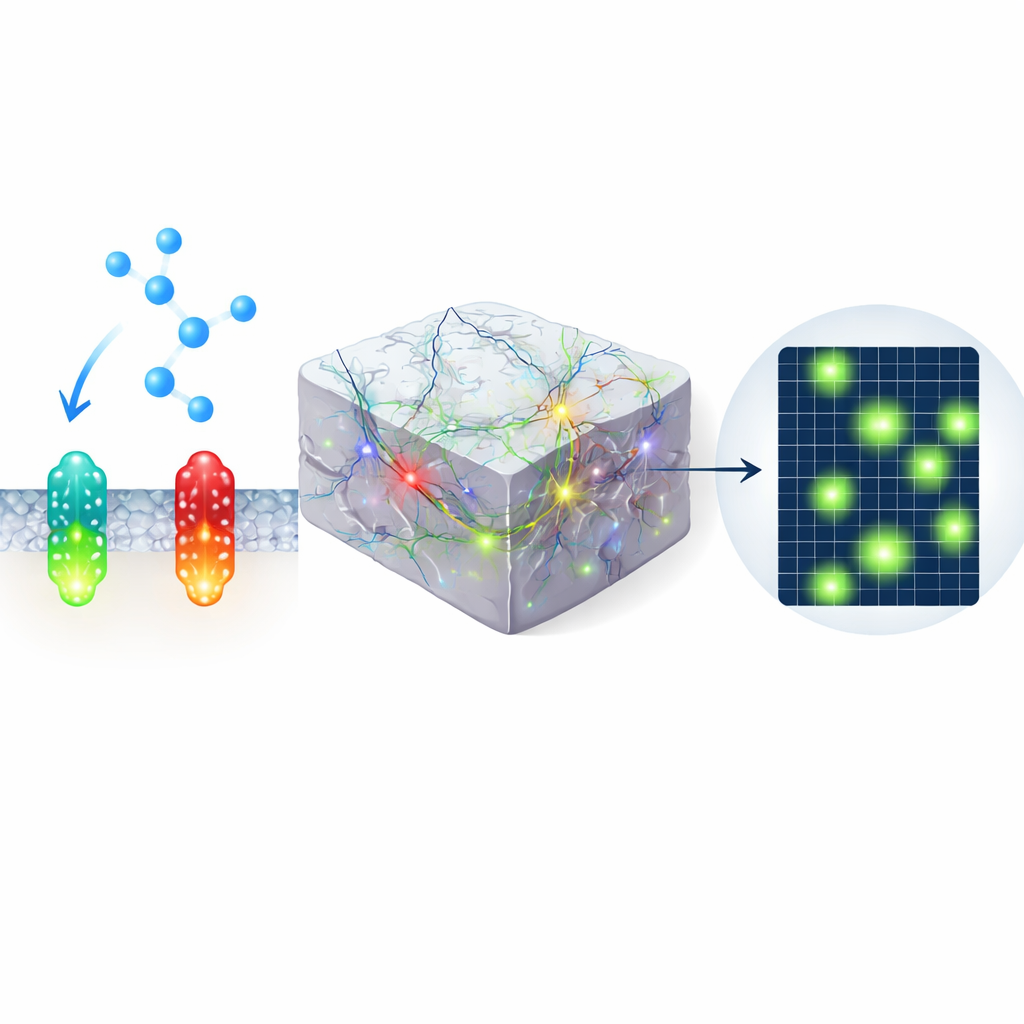
Révéler de minuscules poches d'activité dans le cortex visuel
Dans une autre série d'expériences, les auteurs ont exprimé le capteur vert dans le cortex visuel de souris éveillées et l'ont imagé avec la microscopie deux-photons pendant que les animaux regardaient des stimuli en approche et alternaient entre repos et course. Plutôt qu'un flux continu de signal, ils ont trouvé des patches brefs et très localisés d'augmentation de fluorescence — des microdomaines — disséminés dans le champ de vue. Certains microdomaines répondaient préférentiellement à la menace visuelle, d'autres au mouvement, et beaucoup s'activaient spontanément. Ces motifs étaient largement invisibles avec un ancien capteur vert ou un contrôle muté non liant, soulignant la sensibilité améliorée de nLightG2 et suggérant que la noradrénaline sculpte l'activité cérébrale de manière beaucoup plus fine qu'on ne le pensait auparavant.
Ce que cela signifie pour la recherche cérébrale
Ensemble, ces résultats montrent que nLightG2 et nLightR2 constituent une boîte à outils puissante pour observer la noradrénaline dans le cerveau vivant, à des échelles allant de microdomaines individuels à des états comportementaux entiers. Parce qu'ils existent en couleurs distinctes et peuvent être combinés à d'autres témoins fluorescents, les scientifiques peuvent désormais suivre la noradrénaline parallèlement aux signaux électriques ou calciques dans des types cellulaires spécifiques, pendant le sommeil, l'apprentissage ou le stress. Cette capacité à voir quand et où ce neuromodulateur clé agit pourrait à terme éclairer la façon dont il soutient l'attention et la mémoire en bonne santé, et comment sa perturbation contribue à des troubles tels que l'anxiété, la dépression et les maladies neurodégénératives.
Citation: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
Mots-clés: noradrénaline, neuromodulation, capteurs encodés génétiquement, imagerie deux-photons, sommeil et apprentissage