Clear Sky Science · fr
MaAsLin 3 : affiner et étendre les modèles linéaires multivariables généralisés pour la découverte d’associations en méta-omique
Pourquoi les petits voisins intestinaux comptent
Notre corps abrite des billions de microbes qui aident à digérer les aliments, entraînent le système immunitaire et peuvent même influencer notre humeur. Avec l’essor du séquençage de l’ADN, qui facilite l’inventaire de ces communautés microbiennes, une question cruciale est apparue : quels microbes spécifiques s’associent à des maladies comme les maladies inflammatoires de l’intestin, ou à des caractéristiques quotidiennes telles que l’âge et l’alimentation ? Y répondre s’avère étonnamment difficile. Les données sont bruitées, pleines de zéros et rapportées en pourcentages plutôt qu’en dénombrements réels. Cet article présente MaAsLin 3, un nouvel outil statistique conçu pour extraire des signaux plus nets de données microbiomes désordonnées afin que les chercheurs puissent relier plus fiablement les microbes à la santé humaine et à l’environnement.
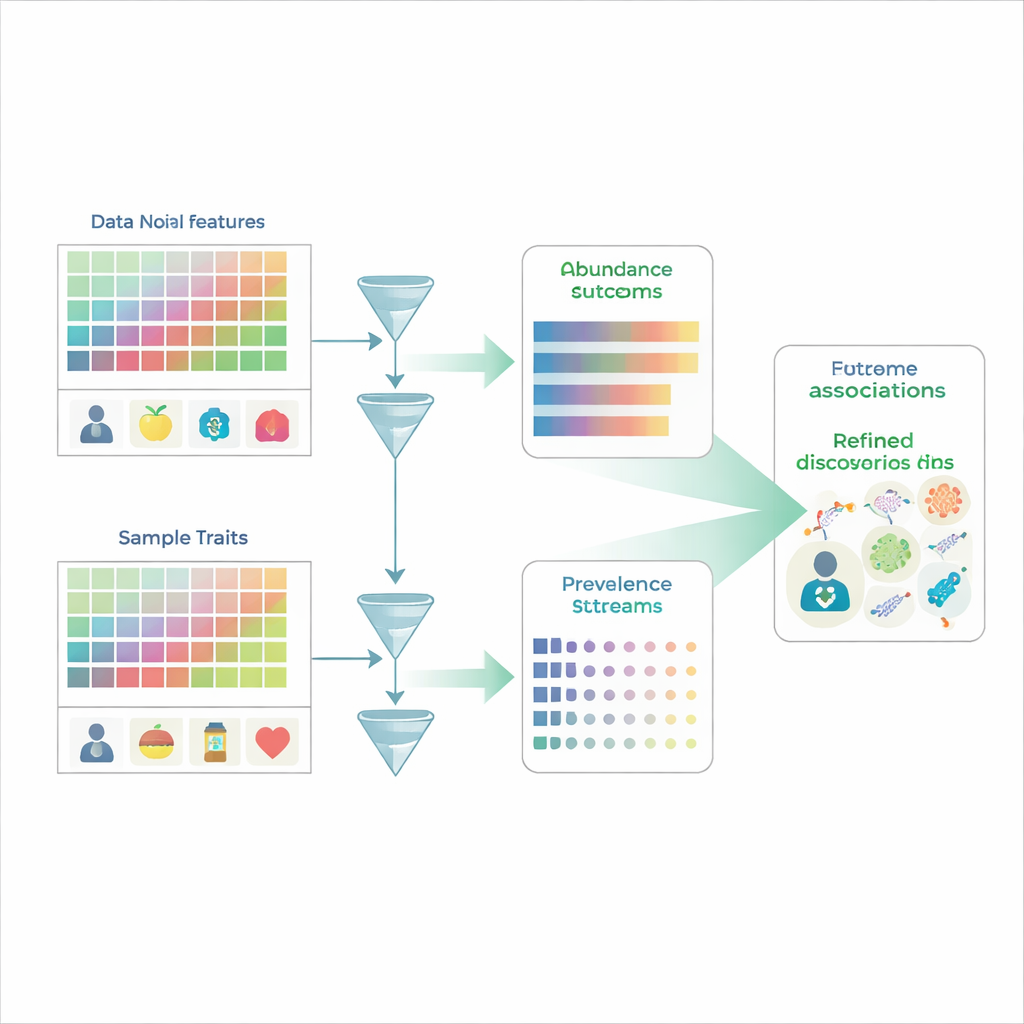
Rechercher des motifs dans une foule bruyante
Les études microbiomes traditionnelles ressemblent un peu à compter des visages dans une foule : les chercheurs mesurent l’abondance relative de centaines ou milliers d’espèces microbiennes chez de nombreuses personnes, puis demandent quelles espèces diffèrent entre, par exemple, des groupes malades et sains. Mais les données microbiomes sont contraintes à des pourcentages qui doivent totaliser 100 % ; ainsi, si une espèce augmente, au moins une autre semble diminuer même si sa quantité réelle n’a pas changé. De plus, de nombreuses espèces ne sont tout simplement pas détectées dans un échantillon donné, produisant beaucoup de zéros qui peuvent refléter soit une absence réelle, soit des limites de détection. Les méthodes d’analyse courantes brouillent généralement deux questions distinctes : un microbe est-il présent du tout, et quelle est sa quantité lorsqu’il est présent ? Ce mélange facilite la mauvaise lecture de la biologie sous-jacente.
Séparer présence et quantité
MaAsLin 3 aborde ces problèmes en traitant explicitement la présence et la quantité comme des phénomènes séparés mais liés. Pour chaque caractéristique microbienne — par exemple une espèce, un gène ou une voie métabolique — il construit deux modèles en parallèle. Un modèle examine la prévalence, c’est‑à‑dire la fréquence de détection de la caractéristique selon les échantillons et leurs traits. L’autre modèle se concentre sur l’abondance, en examinant comment le niveau de la caractéristique varie parmi seulement les échantillons où elle est détectée. En scindant ainsi les données, MaAsLin 3 évite le raccourci courant consistant à remplacer les zéros par de petits nombres arbitraires, ce qui peut fausser les résultats. Il combine ensuite les deux effets pour dresser un portrait global de la relation entre chaque caractéristique et chaque trait, tout en permettant aux chercheurs de voir si une association relève principalement de la présence, de la quantité, ou des deux.
Se rapprocher des quantités réelles
Une complication supplémentaire en science du microbiome est que la plupart des mesures sont relatives : elles indiquent quelle fraction de la communauté totale occupe une espèce, pas combien de cellules il y a réellement. Or, des questions biologiques dépendent souvent de l’abondance absolue — par exemple, si le nombre de cellules d’un pathogène dépasse un seuil susceptible de déclencher une maladie. MaAsLin 3 propose deux solutions complémentaires. Lorsque les expériences incluent des informations additionnelles, comme des quantités connues d’un organisme référent ou des estimations de la charge microbienne totale, la méthode peut transformer des pourcentages relatifs en estimations de comptes absolus et modéliser ceux‑ci directement. Lorsqu’un tel jeu de données n’est pas disponible, MaAsLin 3 compare à la place le comportement de chaque caractéristique au modèle typique observé sur l’ensemble des caractéristiques, ce qui, sous des hypothèses réalistes, approche ce que l’on verrait à l’échelle absolue. De nombreuses simulations informatiques et tests sur des jeux de données réels avec abondances absolues mesurées expérimentalement montrent que cette stratégie récupère fidèlement les tendances sous‑jacentes et surpasse plusieurs outils largement utilisés.
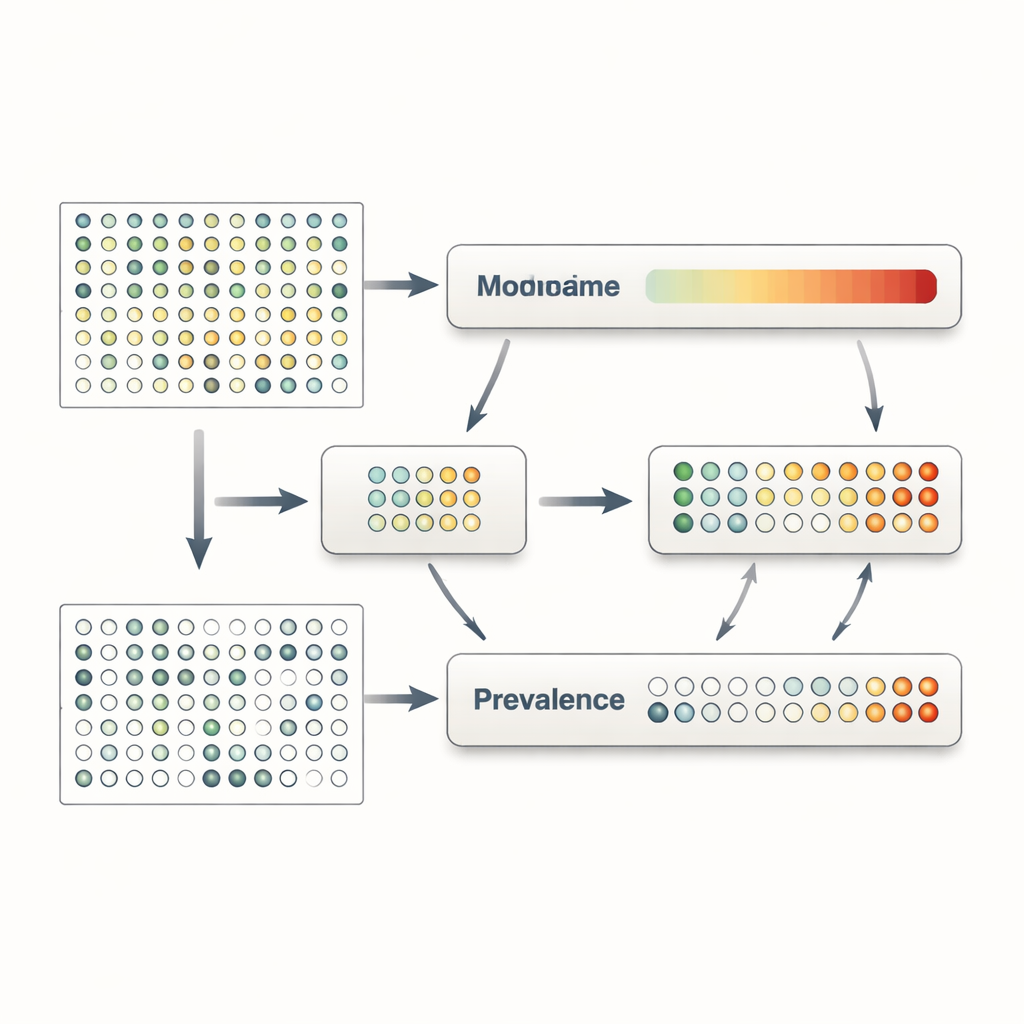
Révéler des signaux cachés dans les maladies intestinales
Pour illustrer l’intérêt pratique de ces avancées, les auteurs ont appliqué MaAsLin 3 à une large cohorte bien étudiée de personnes avec et sans maladies inflammatoires de l’intestin, comme la maladie de Crohn et la rectocolite hémorragique. Des travaux antérieurs avaient déjà identifié de nombreux changements microbiens dans ces affections, mais MaAsLin 3 a ajouté plusieurs niveaux de nuance. Il a confirmé la plupart des liens connus tout en précisant qu’environ les trois quarts des associations impliquaient des changements dans la présence même des microbes, plutôt que dans leur abondance quand ils sont présents. Autrement dit, l’inflammation intestinale coïncidait souvent avec la disparition complète de certains microbes utiles ou leur non‑détection, plutôt qu’avec une simple diminution de leurs niveaux. La méthode a également mis en évidence des microbes dont la seule présence — indépendamment de leur quantité — suivait fortement la perturbation liée à la maladie de la communauté intestinale.
Ce que cela signifie pour les études et les soins futurs
Pour les non‑spécialistes, le message clé est que la façon dont nous analysons les données microbiomes peut profondément influencer les microbes que nous estimons importants pour la santé. En mieux traitant les zéros, en séparant présence et quantité et en approchant les comptes cellulaires réels, MaAsLin 3 offre une lentille plus nette pour découvrir des marqueurs microbiens fiables de la maladie, de l’alimentation et de l’environnement. Ses résultats dans les maladies inflammatoires de l’intestin suggèrent que de nombreux changements cliniquement pertinents impliquent des microbes qui disparaissent ou apparaissent de novo, et non seulement ceux dont l’abondance varie progressivement. Cette distinction est importante pour concevoir des thérapies : si la maladie est liée à la perte complète d’espèces bénéfiques, des stratégies visant à réintroduire ou protéger ces microbes peuvent être plus efficaces que des approches qui cherchent seulement à ajuster l’équilibre global de la communauté. MaAsLin 3 fournit ainsi aux chercheurs une boîte à outils plus précise et flexible pour transformer des mesures microbiomes complexes en connaissances biologiques exploitables.
Citation: Nickols, W.A., Kuntz, T., Shen, J. et al. MaAsLin 3: refining and extending generalized multivariable linear models for meta-omic association discovery. Nat Methods 23, 554–564 (2026). https://doi.org/10.1038/s41592-025-02923-9
Mots-clés: microbiome, maladie inflammatoire chronique de l’intestin, modélisation statistique, abondance absolue, prévalence microbienne