Clear Sky Science · fr
Distribution massive d’azithromycine et résistance aux antibiotiques dans l’intestin et le nasopharynx : un essai randomisé par grappes
Pourquoi donner un comprimé à de nombreux enfants compte
Dans certaines régions d’Afrique de l’Ouest, un seul antibiotique, l’azithromycine, a été utilisé dans des campagnes de masse pour réduire le nombre d’enfants en bas âge qui meurent d’infections. La stratégie fonctionne — mais elle soulève une inquiétude sérieuse : ne favorisons‑nous pas discrètement l’émergence de microbes plus résistants aux médicaments dans l’organisme des enfants ? Cette étude, menée dans des centaines de villages au Niger, examine de près l’intérieur des intestins et des narines des enfants pour voir comment des traitements répétés à l’échelle communautaire remodèlent leur monde microbien caché et la résistance aux antibiotiques.
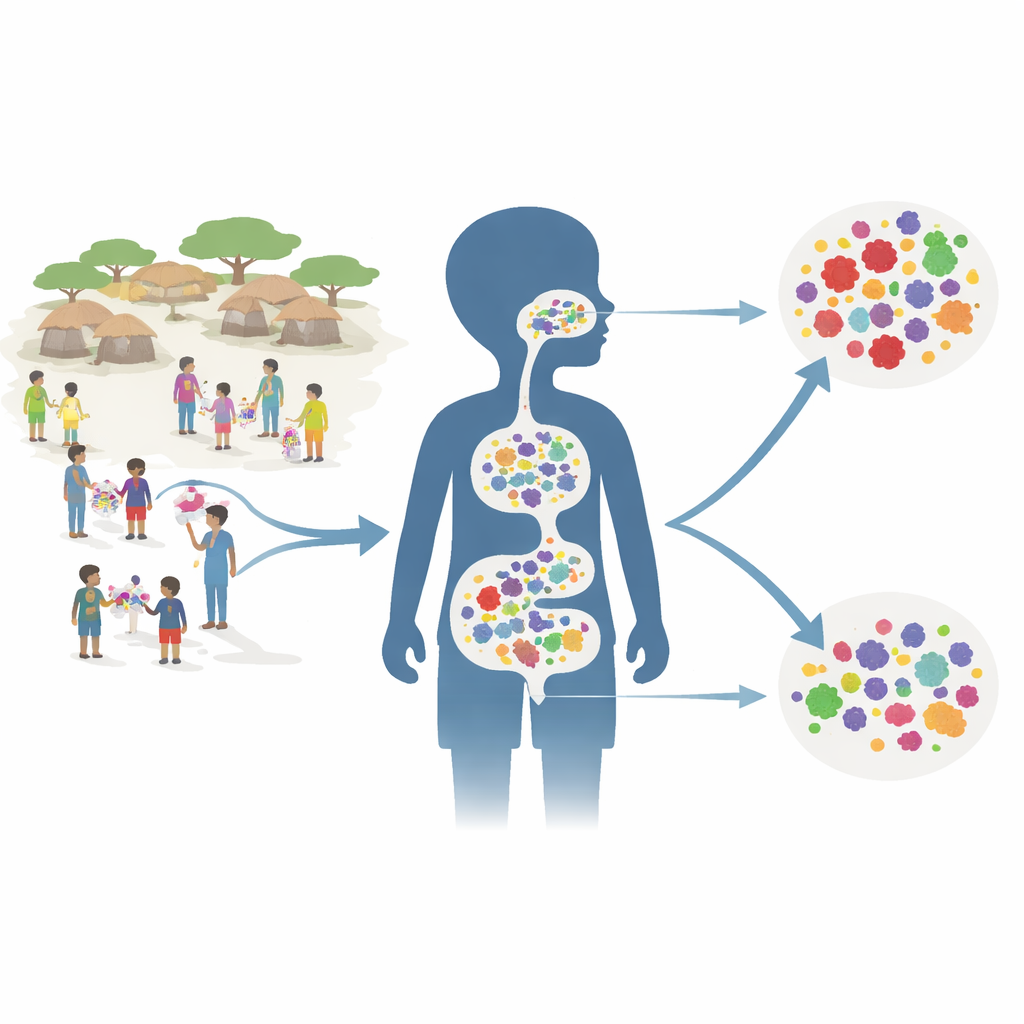
Tester un plan de médication à l’échelle communautaire
Les chercheurs ont intégré leur travail dans un vaste essai appelé AVENIR, qui avait déjà montré que donner de l’azithromycine tous les six mois à tous les enfants âgés de 1 à 59 mois pouvait réduire la mortalité dans cette tranche d’âge. Pour l’étude sur la résistance, ils se sont concentrés sur 150 villages choisis au hasard. Chaque village appartenait à l’un des trois groupes : tous les jeunes enfants recevaient de l’azithromycine ; seuls les nourrissons jusqu’à 11 mois recevaient de l’azithromycine tandis que les tout‑petits plus âgés et les enfants d’âge préscolaire recevaient un placebo ; ou tous les enfants recevaient un placebo. Deux ans après le début du programme — six mois après la quatrième série de traitements — l’équipe a prélevé des écouvillons rectaux et nasopharyngés profonds chez environ 30 enfants par village.
Plonger dans l’intestin et le nez
Plutôt que de cultiver les microbes en laboratoire, les scientifiques ont poolé les échantillons de chaque village et utilisé le séquençage d’ADN moderne. Cela leur a permis d’identifier les bactéries présentes et de compter les marqueurs génétiques qui signalent une résistance à différentes familles d’antibiotiques. Ils ont prêté une attention particulière aux macrolides — la famille de médicaments incluant l’azithromycine — tout en recherchant également la résistance à de nombreux autres types d’antibiotiques largement utilisés, comme les bêta‑lactamines apparentées à la pénicilline. L’intestin et le nasopharynx (la partie haute de la gorge derrière le nez) ont été examinés car ce sont des réservoirs majeurs où les gènes de résistance peuvent s’accumuler et potentiellement se propager.
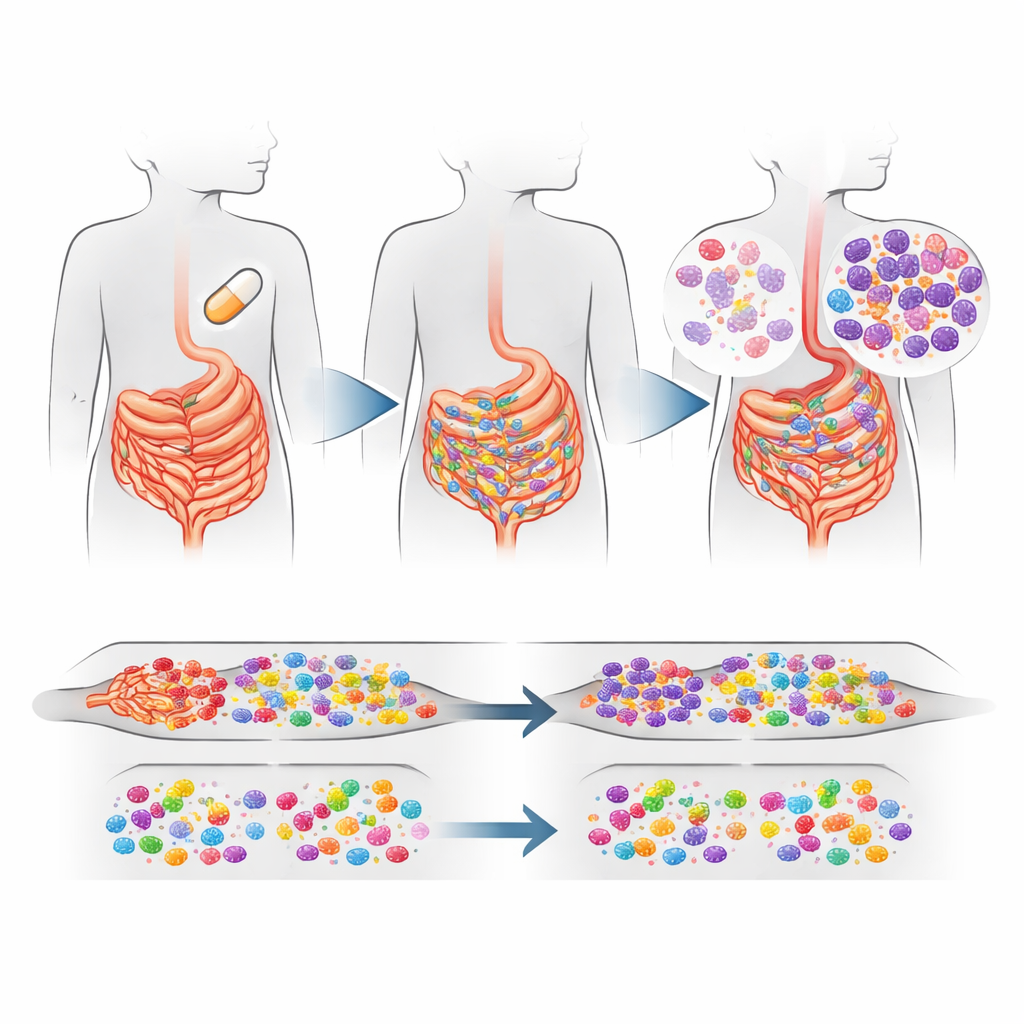
Ce qui a changé dans l’intestin des enfants
Le signal le plus net venait de l’intestin. Les villages où tous les enfants recevaient de l’azithromycine présentaient une augmentation modeste mais statistiquement significative — d’environ 16 % au total — des gènes de résistance aux macrolides dans les bactéries intestinales comparé aux villages sous placebo. Cette hausse était principalement portée par un gène de résistance, appelé ermF, qui aide à protéger les bactéries contre les macrolides. Ce gène est souvent porté par des bactéries intestinales courantes telles que Bacteroides et Prevotella, qui vivent habituellement sans causer de tort dans les intestins mais peuvent parfois provoquer des infections. Fait intéressant, les gènes de résistance contre d’autres grandes familles d’antibiotiques n’ont pas augmenté, et la composition et la diversité globales des bactéries intestinales semblaient globalement similaires entre les groupes de traitement, même si certaines espèces spécifiques sont devenues plus ou moins communes.
Ce qui est resté identique dans le nez
En revanche, les voies nasales racontent une histoire plus discrète. L’étude n’a pas trouvé de différences claires et statistiquement robustes des gènes de résistance aux macrolides entre les groupes de traitement dans le nasopharynx, ni de preuve que la résistance à d’autres classes d’antibiotiques était sélectionnée à cet endroit. Les résidents nasaux typiques — des genres tels que Moraxella, Haemophilus et Streptococcus — sont restés dominants. Quelques bactéries associées à la cavité buccale liées aux maladies des gencives sont devenues plus fréquentes dans les communautés traitées par l’azithromycine, et certaines de celles‑ci peuvent aussi porter des gènes de résistance, mais la charge globale de résistance dans le nez n’a pas évolué de la même manière que dans l’intestin.
Équilibrer les gains d’aujourd’hui et les risques de demain
Pris ensemble, les résultats montrent que donner de l’azithromycine à tous les jeunes enfants d’une communauté peut sauver des vies, mais pousse aussi les bactéries intestinales vers une plus grande résistance à cette famille de médicaments, principalement via l’expansion de gènes de résistance spécifiques comme ermF. L’étude n’a pas observé de propagation vers une résistance à d’autres types d’antibiotiques sur la période de deux ans, ni de changements marqués dans le réservoir nasal, mais les auteurs avertissent que les bactéries intestinales résistantes et leurs gènes peuvent se propager avec le temps et entre les personnes. Ils soutiennent que tout programme antibiotique large pour la survie infantile devrait inclure une surveillance attentive et à long terme de la résistance afin que les responsables de santé puissent continuer à peser le bénéfice immédiat de moins de décès infantiles contre le coût plus lent et moins visible de l’affermissement des microbes résistants aux médicaments.
Citation: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Mots-clés: azithromycine, mortalité infantile, résistance aux antibiotiques, microbiote intestinal, administration massive de médicaments