Clear Sky Science · fr
Atlas unicellulaire du cortex cérébral en développement dans la trisomie 21
Pourquoi cette recherche est importante
La trisomie 21 est la cause génétique la plus fréquente de déficience intellectuelle, et pourtant nous savons encore peu de choses sur la manière dont elle modifie le cerveau humain en développement avant la naissance. Cette étude examine le cortex fœtal — la région cérébrale cruciale pour la pensée et la mémoire — au niveau des cellules individuelles afin de cartographier ce qui déraille, quand cela commence et quels interrupteurs moléculaires pourraient être ciblés pour aider.
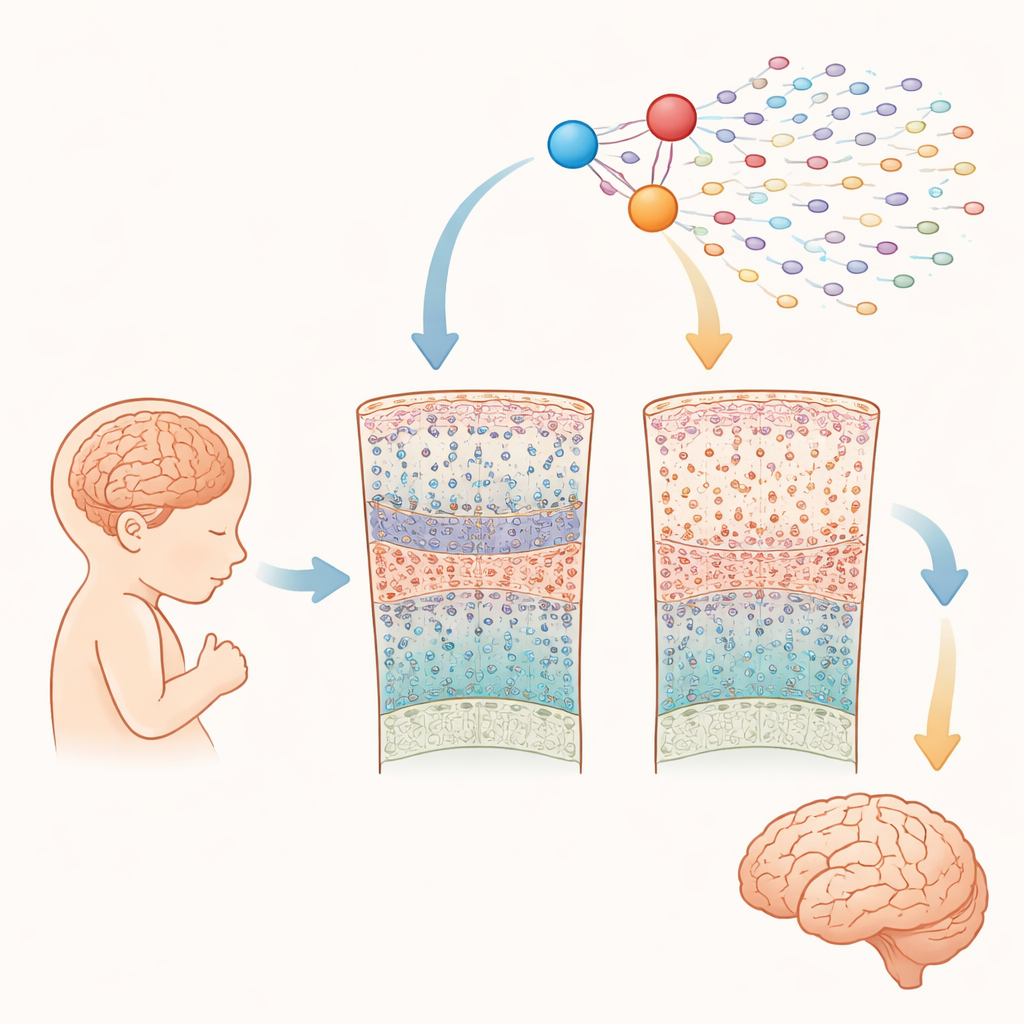
Observer de près le cerveau en croissance
Les chercheurs ont analysé près d’un quart de million de cellules prélevées dans le cortex cérébral de 15 fœtus porteurs de trisomie 21 et de 15 fœtus témoins, entre 10 et 20 semaines après la conception. À l’aide de méthodes monocellulaires avancées, ils ont mesuré à la fois les gènes activés et l’accessibilité de l’ADN dans chaque cellule. Cela leur a permis d’identifier tous les principaux types cellulaires présents à ce stade de mi-gestation — tels que les cellules progénitrices de type souche, différents types de neurones excitateurs et inhibiteurs, et les premiers oligodendrocytes/astrocytes — et de comparer leur abondance et leur activité génique entre les cerveaux trisomiques et typiques.
Modifications précoces dans des cellules-clés de la pensée
La plupart des grandes classes cellulaires étaient présentes en nombres similaires dans les deux groupes pendant cette fenêtre précoce. Cependant, l’équipe a observé un déficit marqué et sélectif d’un type particulier de neurone excitateur qui occupe normalement la couche 4 du cortex et joue un rôle important dans le traitement des informations entrantes. Ces neurones se définissent par les protéines RORB et FOXP1. Chez les fœtus porteurs de trisomie 21, les neurones RORB–FOXP1 étaient déjà diminués à la mi-gestation, en particulier entre 16 et 20 semaines, tandis que d’autres types neuronaux semblaient relativement épargnés. Cela suggère que des problèmes dans la génération ou la maturation de ce sous-ensemble de cellules débutent in utero et peuvent contribuer directement aux difficultés cognitives ultérieures.
Programmes génétiques perturbés et commutateurs maîtres
Au-delà des dénombrements cellulaires, l’étude a révélé que des centaines de gènes étaient subtilement déréglés, en particulier dans les neurones excitateurs et leurs progéniteurs. Beaucoup de ces gènes participent à la construction du cerveau antérieur, à la formation des ramifications neuronales, à l’établissement des connexions et au soutien des fonctions cérébrales supérieures. Plutôt que de n’agir que par l’excès des ~200 gènes présents sur le chromosome 21, les données pointent vers un réseau perturbé de régulation génique. En combinant activité génique et accessibilité de l’ADN, les auteurs ont cartographié des circuits régulateurs et mis en évidence trois facteurs de transcription — BACH1, PKNOX1 et GABPA — codés sur le chromosome 21 comme des « nœuds » sensibles au dosage. Ces molécules semblent influencer d’autres régulateurs critiques du développement cortical, y compris des facteurs déjà associés à la déficience intellectuelle, et aident à expliquer comment une augmentation modeste (~1,5×) du dosage génique peut se propager à travers des programmes développementaux entiers.
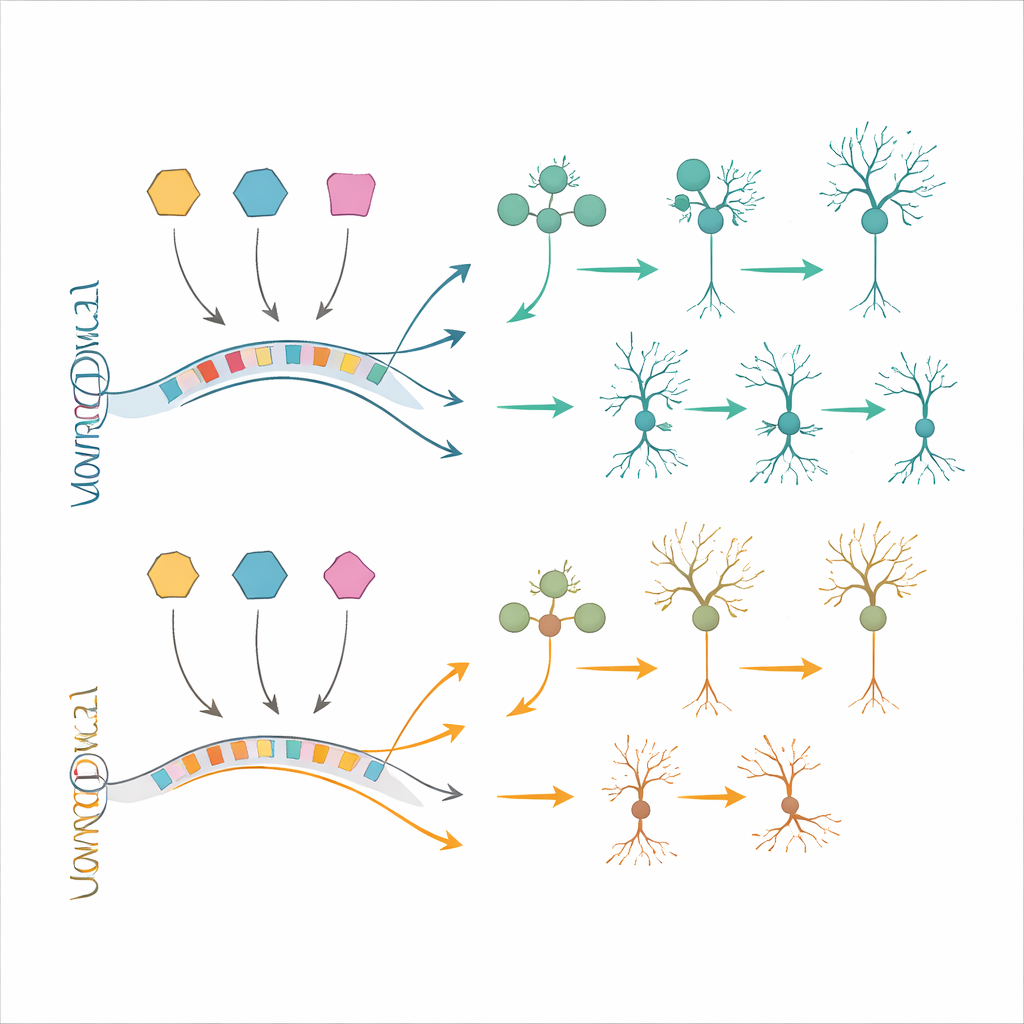
Tester des stratégies de restauration in vitro et in vivo
Pour déterminer si ces changements moléculaires pouvaient être corrigés, l’équipe a recours à des modèles de cellules souches. Ils ont généré des cellules progénitrices neurales et des neurones à partir de cellules souches pluripotentes induites porteuses de la trisomie 21 et de cellules témoins appariées. De nombreux changements d’expression génique observés dans les tissus fœtaux réapparaissaient dans ces cellules cultivées en laboratoire, confirmant la pertinence des modèles. Les chercheurs ont ensuite utilisé des oligonucléotides antisens — de courts brins d’un matériau analogue à l’ADN conçu — pour réduire l’expression de BACH1, PKNOX1 ou GABPA vers des niveaux plus normaux. Cette normalisation partielle des facteurs de transcription surexprimés a entraîné une récupération partielle de plusieurs gènes en aval, y compris certains connus pour intervenir dans la déficience intellectuelle et la différenciation neuronale. De manière complémentaire, ils ont transplanté des cellules neurales humaines trisomie 21 dans des cerveaux de souris et les ont laissées mûrir in vivo. Ces greffes ont reproduit des caractéristiques supplémentaires proches de la trisomie 21, telles qu’un déséquilibre neurone–glie altéré et des changements géniques non entièrement capturés en culture, offrant un terrain d’essai puissant pour de futures thérapies.
Ce que cela signifie pour l’avenir
Dans l’ensemble, ce travail fournit un atlas détaillé de la façon dont la trisomie 21 remodèle le paysage génétique du cortex en développement à résolution unicellulaire. Pour le lecteur général, le message clé est que le chromosome supplémentaire n’ajoute pas simplement quelques gènes perturbateurs ; il influe sur de nombreux commutateurs moléculaires interconnectés, conduisant à des pénuries précoces et sélectives de certains neurones liés à la pensée. En identifiant un petit groupe de facteurs de transcription du chromosome 21 comme acteurs centraux — et en montrant que leurs effets peuvent être partiellement inversés dans des cellules humaines — l’étude ouvre la voie à des stratégies plus ciblées visant à améliorer le développement et le fonctionnement cérébral dans la trisomie 21.
Citation: Lattke, M., Tan, W.L., Sukumaran, S.K. et al. Single-cell atlas of the developing Down syndrome brain cortex. Nat Med 32, 1061–1072 (2026). https://doi.org/10.1038/s41591-026-04211-1
Mots-clés: trisomie 21, d%C3%A9veloppement du cerveau f%C3%A9tal, g%C3%A9nomique monocellulaire, neurones corticaux, facteurs de transcription