Clear Sky Science · fr
Cellules CAR-T anti-CD19 pour des maladies auto-immunes réfractaires au traitement : essai panier de phase 1/2 CASTLE
Pourquoi un traitement unique compte
Beaucoup de personnes atteintes de maladies auto-immunes graves vivent sur un tapis roulant de médicaments permanents, enchaînant poussées après poussées et accumulant les effets secondaires. Cette étude explore une idée radicalement différente : utiliser une seule perfusion de cellules immunitaires reprogrammées pour « redémarrer » le système immunitaire afin qu’il cesse d’attaquer l’organisme. Pour des patients atteints de lupus sévère, de durcissement de la peau et des organes, ou d’inflammations musculaires qui n’ont plus d’options, un tel réinitialisation pourrait signifier un soulagement durable sans traitements quotidiens.
Trois maladies difficiles, un problème commun
Le lupus érythémateux systémique, la sclérodermie systémique et les myopathies inflammatoires idiopathiques peuvent paraître différentes en surface — touchant les articulations, la peau, les poumons, les reins ou les muscles — mais elles partagent un défaut central : certaines cellules immunitaires appelées cellules B dysfonctionnent et contribuent à l’inflammation chronique. Les traitements standards, des corticoïdes aux puissants immunosuppresseurs et perfusions d’anticorps, peuvent calmer les symptômes mais suppriment rarement la cause profonde. De nombreux patients enchaînent plusieurs thérapies qui ne fonctionnent que partiellement ou entraînent des effets secondaires intolérables, les laissant avec des lésions d’organes progressives et une qualité de vie réduite.
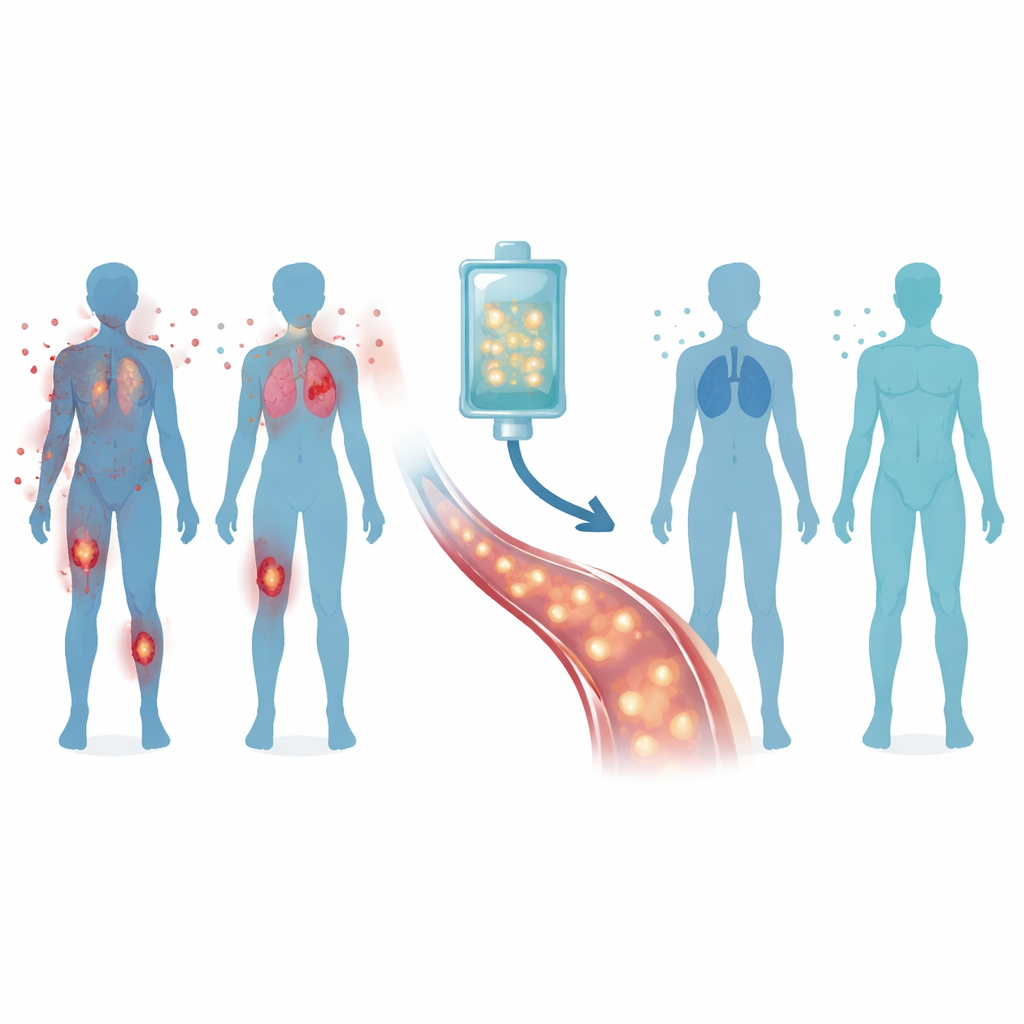
Reprogrammer les défenseurs du corps
L’essai CASTLE a testé une thérapie cellulaire personnalisée appelée Zorpo-cel chez 24 adultes atteints de formes sévères et résistantes au traitement de ces trois maladies. Les médecins ont d’abord prélevé les cellules T de chaque patient, les « soldats » du système immunitaire, puis les ont équipées en laboratoire d’un nouveau capteur — un récepteur chimérique d’antigène — qui reconnaît un marqueur appelé CD19 présent sur la plupart des cellules B. Après un court traitement chimiothérapeutique visant à libérer de l’espace dans le système immunitaire, les patients ont reçu une seule perfusion de ces cellules modifiées, appelées cellules CAR-T anti-CD19. L’espoir était qu’elles traquent et éliminent les cellules B défaillantes, permettant à un ensemble de cellules plus sain de repousser.
La sécurité d’abord, puis des signes d’amélioration
Parce que ce traitement peut être intense chez les patients atteints de cancer, l’objectif principal de cet essai précoce était la sécurité. Les chercheurs ont surveillé de près une réaction inflammatoire dangereuse appelée syndrome de libération des cytokines et les effets secondaires neurologiques. Dans CASTLE, près des trois quarts des patients n’ont présenté que des fièvres et une inflammation légères et transitoires ; aucune tempête cytokinique grave, aucune toxicité cérébrale ni problème sanguin persistant n’a été observé. Les problèmes les plus fréquents étaient des baisses temporaires des globules blancs et des infections bénignes, gérées par les soins standards. Un patient a développé une insuffisance rénale liée à une réactivation virale et à une poussée de sa maladie sous-jacente, ce qui a entraîné un renforcement des règles visant à mieux contrôler l’activité de la maladie avant la perfusion.
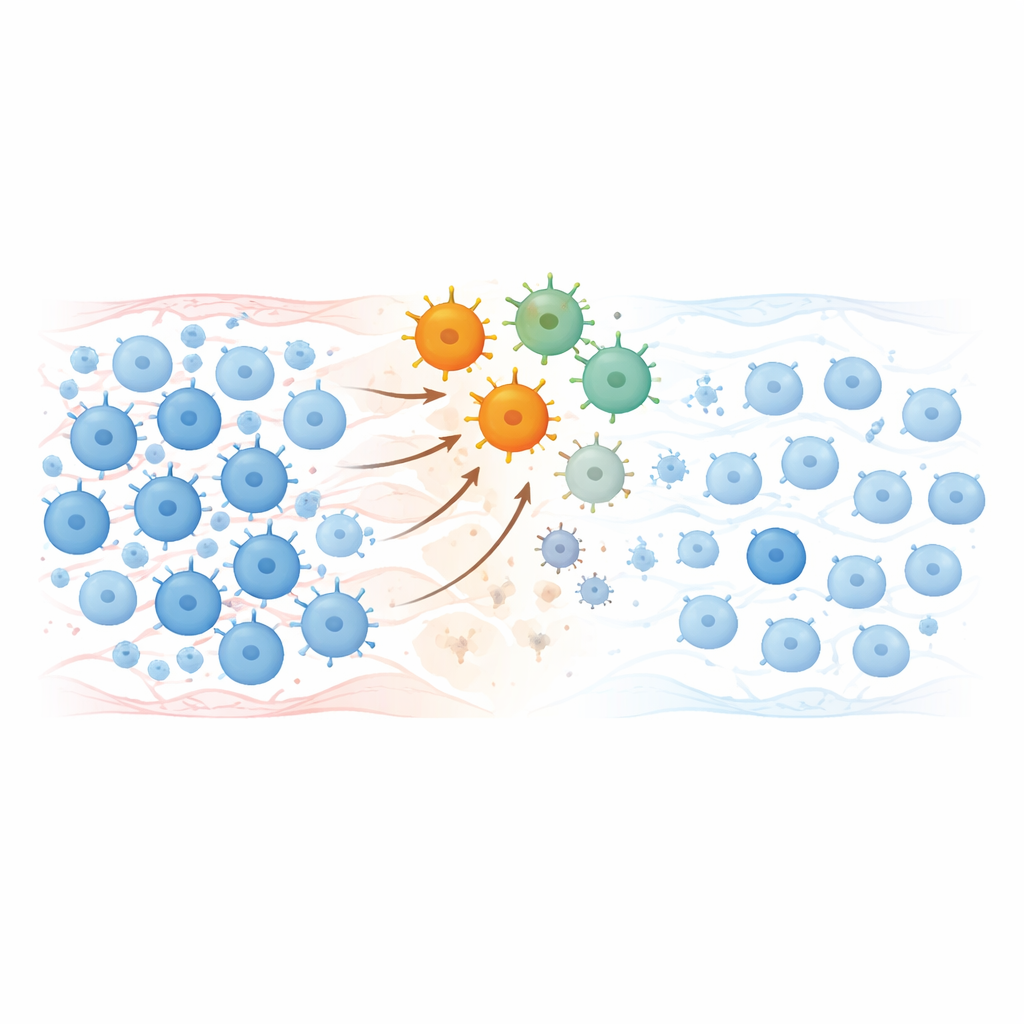
Réinitialiser le système immunitaire
Bien que la sécurité ait été la priorité, les améliorations cliniques ont été marquantes. Après six mois, 22 des 24 patients remplissaient des critères de succès prédéfinis adaptés à leur maladie : la plupart des patients lupiques ont atteint une définition stricte de rémission, tous les patients atteints de sclérodermie systémique n’ont pas présenté d’aggravation de la maladie pulmonaire et ont montré une meilleure fonction respiratoire et un assouplissement de la peau, et la plupart des patients atteints d’inflammation musculaire ont gagné en force et ont vu leurs enzymes musculaires diminuer. Fait important, tous les participants ont pu arrêter les corticoïdes et autres immunosuppresseurs et sont restés sans ces traitements pendant l’étude de six mois et au-delà, sans rechute observée sur un suivi médian d’environ un an.
Ce qui se passe dans le sang
Les analyses en laboratoire ont montré que les cellules CAR-T perfusées se sont multipliées pendant quelques jours, ont éliminé les cellules B circulantes puis ont progressivement disparu sur quelques mois. Lorsque les cellules B sont revenues, leur population avait changé : les cellules naïves, « fraîches », dominaient, tandis que les cellules mémoire et les précurseurs producteurs d’anticorps, qui abritent souvent la mémoire auto-immune, ont été fortement réduits. De nombreux auto-anticorps nuisibles sont tombés à des niveaux très faibles ou indétectables, tandis que les anticorps protecteurs issus de vaccinations antérieures contre des infections comme la rougeole ou le tétanos sont restés en grande partie présents, ce qui suggère une réinitialisation ciblée plutôt qu’un effacement complet de la mémoire immunitaire.
Un aperçu d’une nouvelle ère thérapeutique
Pour les personnes vivant avec une maladie auto-immune sévère, l’idée d’un traitement unique apportant une rémission durable sans médicaments semblait longtemps hors de portée. Cet essai suggère que des cellules T modifiées peuvent en toute sécurité réduire au silence des cellules B dévoyées dans trois maladies différentes et permettre au système immunitaire de se reconstruire d’une façon plus calme et moins auto-destructrice. CASTLE est une étude précoce et relativement petite ; des essais pivots plus larges sont nécessaires pour confirmer la durée du bénéfice et identifier les patients les plus susceptibles d’en tirer parti. Néanmoins, elle ouvre la voie à un avenir où réinitialiser le système immunitaire — plutôt que de le supprimer sans fin — pourrait devenir un objectif réaliste.
Citation: Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
Mots-clés: thérapie par cellules CAR-T, maladie auto-immune, lupus érythémateux systémique, sclérodermie systémique, cellules B