Clear Sky Science · fr
Les réponses humorales IgG1 aux antigènes tumoraux sous-tendent les résultats cliniques lors du blocage des points de contrôle immunitaires
Pourquoi cela compte pour les patients atteints de cancer
L’immunothérapie a transformé la prise en charge du cancer en aidant les défenses de l’organisme à attaquer les tumeurs, mais seuls certains patients en tirent bénéfice. L’attention s’est principalement portée sur un type de combattants immunitaires — les lymphocytes T —, mais cette étude montre qu’un autre groupe, les cellules B productrices d’anticorps, peut faire la différence entre succès et échec. En révélant comment une réponse anticorps spécifique, appelée IgG1, s’associe à de meilleurs résultats, ce travail ouvre la voie à de nouvelles méthodes pour prédire qui bénéficiera de l’immunothérapie et pour étendre l’efficacité de ces traitements à davantage de patients.
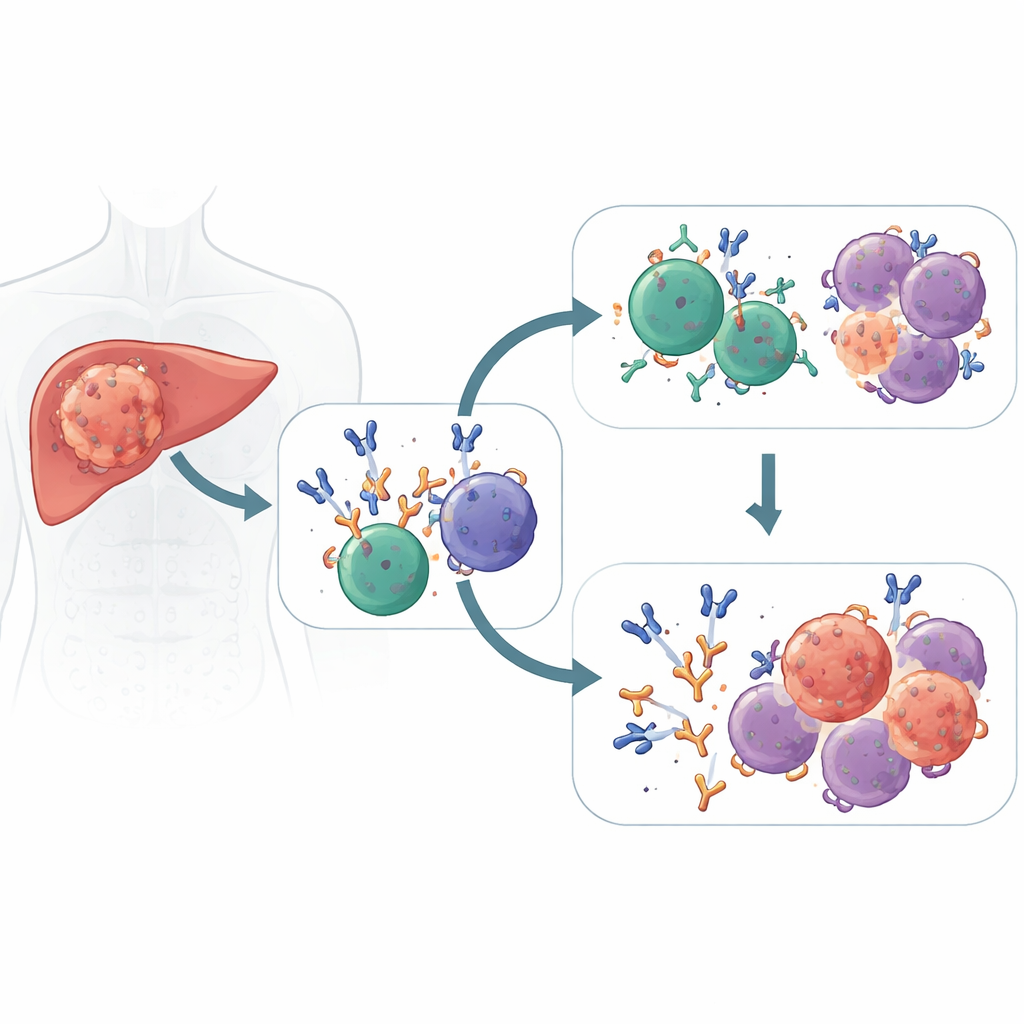
Deux lignes de défense qui coopèrent
Les médicaments modernes connus sous le nom d’inhibiteurs des points de contrôle immunitaires relâchent les « freins » sur les lymphocytes T pour qu’ils reconnaissent et tuent les cellules cancéreuses. Les chercheurs ont étudié des personnes atteintes de cancer du foie recevant ces médicaments avant chirurgie et ont découvert que les bons répondeurs ne comptaient pas uniquement sur les T. Leurs tumeurs étaient également envahies de plasmocytes — cellules B matures qui fonctionnent comme de petites usines à anticorps — produisant une vague dominante d’anticorps IgG1 dirigés contre des cibles tumorales. En revanche, les patients dont les tumeurs ne régresseraient pas présentaient davantage de cellules B inactives ou dysfonctionnelles et moins de ces plasmocytes spécialisés au sein de leurs cancers.
Suivre la piste des anticorps dans l’organisme
Pour comprendre l’origine de ces plasmocytes utiles, l’équipe a combiné le séquençage unicellulaire avec le suivi détaillé des « codes-barres » anticorps uniques portés par chaque cellule B. Ils ont constaté que les patients avec une bonne réponse avaient des familles de cellules productrices d’IgG1 étroitement apparentées qui s’expandaient à la fois dans la tumeur et dans les ganglions lymphatiques voisins — les centres de commandement du système immunitaire. Les mêmes signatures clonales étaient présentes avant le traitement puis augmentaient après la thérapie, indiquant que le blocage des points de contrôle amplifie des clones B préexistants, sensibilisés à la tumeur, plutôt que d’en générer entièrement de nouveaux. Cela suggère une circulation coordonnée de ces producteurs d’anticorps entraînés entre ganglions et sites tumoraux.
Comment les anticorps reconfigurent le voisinage tumoral
Des images microscopiques et une cartographie spatiale des gènes ont montré que, chez les répondeurs, les plasmocytes n’étaient pas cantonnés aux marges de la tumeur — ils infiltraient en profondeur le cancer aux côtés des lymphocytes T cytotoxiques et des macrophages utiles. Ces zones étaient riches en signaux favorisant l’activation des cellules B et la production d’anticorps, formant des « quartiers » immunitaires optimisés pour l’attaque. Les non-répondeurs, en revanche, accumulaient des cellules B de type mémoire et des cellules immunitaires régulatrices dans des poches stromales fibreuses qui freinaient les réponses efficaces. Dans plusieurs cohortes indépendantes de patients et avec différentes combinaisons d’immunothérapies, une prédominance de plasmocytes producteurs d’IgG1 marquait systématiquement un meilleur contrôle tumoral et une progression de la maladie plus lente.
Des anticorps qui reconnaissent des marqueurs spécifiques du cancer
Comme les plasmocytes sécrètent des anticorps dans le sang, les investigateurs se sont demandé si ces molécules pouvaient être détectées dans des échantillons sanguins. Chez de nombreux répondeurs, ils ont trouvé des niveaux élevés d’anticorps IgG1 ciblant les soi‑disant antigènes cancer/testicule — des protéines comme NY-ESO-1 qui sont normalement absentes des tissus sains mais réapparaissent dans les tumeurs. Les patients porteurs de ces anticorps présentaient aussi plus souvent une forte activité des lymphocytes T dirigée contre les mêmes cibles, ce qui suggère que les anticorps facilitent la présentation de fragments tumoraux au bras cellulaire de l’immunité. De larges jeux de données de survie en mélanome et en cancer du poumon ont confirmé que les tumeurs avec de fortes signatures IgG1 ont tendance à mieux répondre aux inhibiteurs de points de contrôle, alors que les cancers traités principalement par chimiothérapie standard ne montrent pas ce lien.
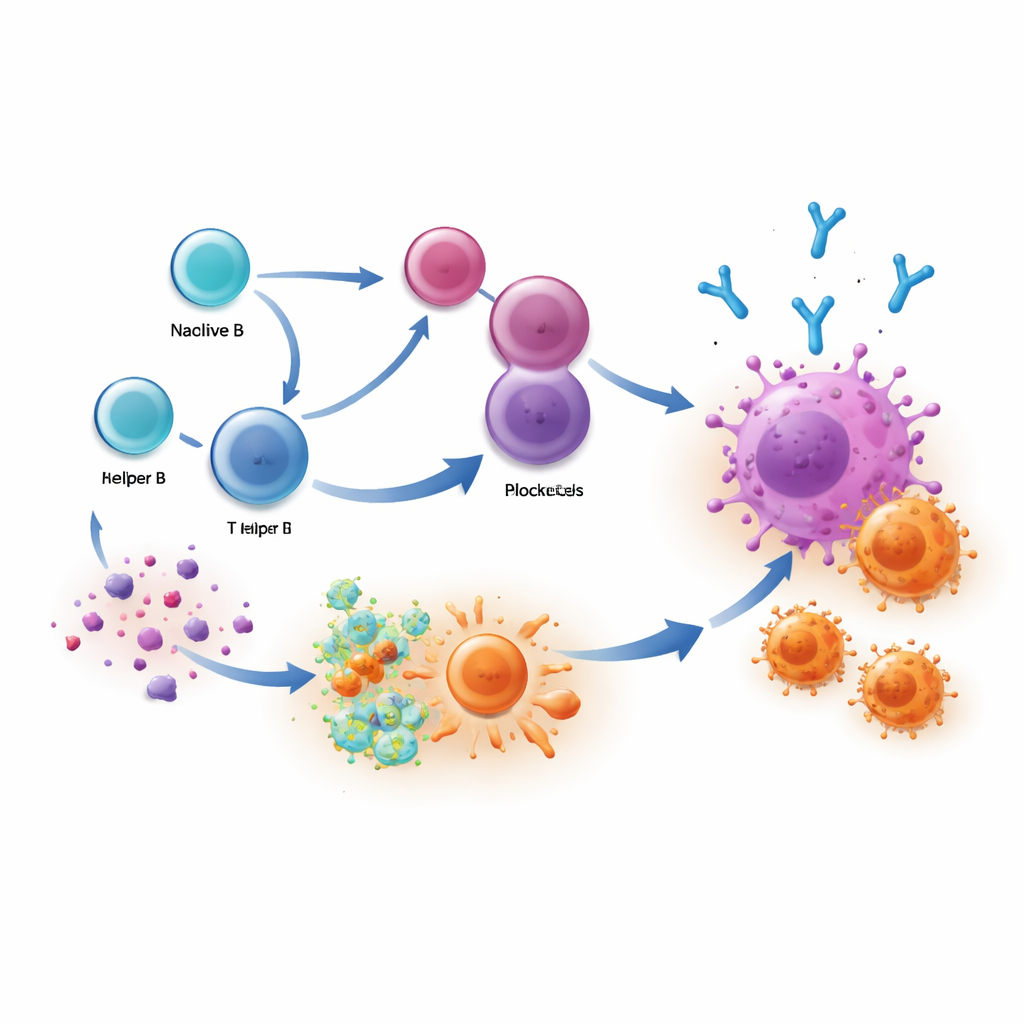
Ce que cela signifie pour les traitements futurs
En résumé, les patients obtiennent les meilleurs résultats lorsque leur système immunitaire mène une attaque à deux volets : des anticorps IgG1 produits par des plasmocytes balisent les cellules cancéreuses, et les lymphocytes T interviennent pour les éliminer. Cette étude montre que les thérapies par blocage des points de contrôle peuvent renforcer ces réponses anticorps, surtout lorsque des clones B utiles sont déjà présents avant le traitement. Mesurer les plasmocytes riches en IgG1 ou leurs anticorps dans le sang et les échantillons tumoraux pourrait aider les médecins à identifier les patients susceptibles de répondre et à suivre l’efficacité du traitement. À terme, des vaccins ou des médicaments orientant les cellules B vers la production de ces anticorps IgG1 précis et ciblant la tumeur pourraient amplifier les bénéfices de l’immunothérapie et offrir des réponses durables à un plus grand nombre de personnes vivant avec un cancer.
Citation: Gonzalez-Kozlova, E., Sweeney, R., Figueiredo, I. et al. Humoral IgG1 responses to tumor antigens underpin clinical outcomes in immune checkpoint blockade. Nat Med 32, 978–991 (2026). https://doi.org/10.1038/s41591-025-04177-6
Mots-clés: immunothérapie du cancer, cellules B, anticorps IgG1, blocage des points de contrôle immunitaire, carcinome hépatocellulaire