Clear Sky Science · fr
Échappement antigénique multimodal aux engageurs de cellules T ciblant GPRC5D dans le myélome multiple
Quand le cancer déjoue l’immunothérapie de précision
De nouveaux médicaments immunitaires puissants transforment le traitement du myélome multiple, un cancer du sang qui reste incurable pour la plupart des patients. Ces thérapies agissent en redirigeant les propres cellules T de l’organisme pour chercher et détruire les cellules tumorales marquées par des « drapeaux » spécifiques à leur surface. Un drapeau prometteur est une molécule appelée GPRC5D. Pourtant, comme pour de nombreuses thérapies ciblées, les tumeurs peuvent évoluer et échapper au traitement. Cette étude révèle, avec un détail inhabituel, comment les cellules de myélome modifient ou masquent le drapeau GPRC5D afin d’échapper à des médicaments engageant les cellules T hautement efficaces.
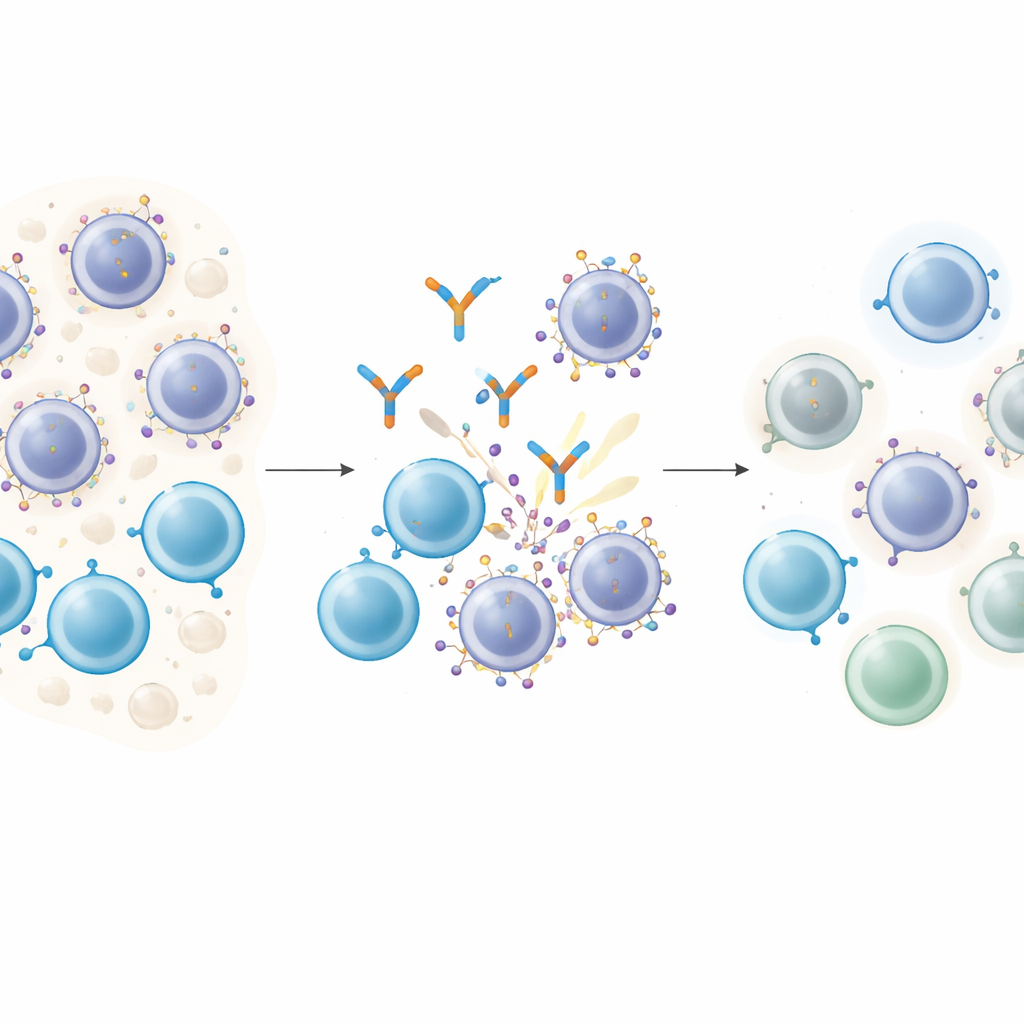
Comment les médicaments intelligents s’accrochent aux cellules cancéreuses
Les anticorps engageant les cellules T fonctionnent comme des entremetteurs moléculaires : une extrémité saisit une cellule T, l’autre s’attache à une molécule cible sur la cellule cancéreuse, rapprochant les deux pour que la cellule T puisse tuer sa proie. Dans le myélome multiple, GPRC5D est une cible attrayante parce qu’elle est abondante sur les cellules plasmatiques malignes mais rare sur la plupart des tissus normaux. Les patients traités par un médicament dirigé contre GPRC5D appelé talquetamab connaissent souvent des rémissions profondes. Cependant, presque tous rechutent finalement, ce qui soulève une question cruciale : les cellules cancéreuses modifient‑elles la cible même dont dépendent ces médicaments ?
Suivre l’évolution tumorale en temps réel
Les chercheurs ont suivi 21 personnes atteintes d’un myélome difficile à traiter qui ont reçu du talquetamab. Ils ont prélevé des échantillons de moelle osseuse avant le traitement chez certains patients puis à la rechute, puis ont utilisé plusieurs couches d’analyse de l’ADN, de l’ARN et de la chromatine pour examiner les cellules tumorales. Cette vue ultra‑détaillée a révélé que, chez environ les deux tiers des patients rechutés, le cancer avait altéré GPRC5D de façons susceptibles d’affaiblir ou de bloquer l’effet du médicament. Fait frappant, plusieurs sous‑clones résistants différents — branches génétiquement distinctes de la tumeur — coexistaient souvent chez une même personne, montrant que l’évolution vers l’échappement peut suivre plusieurs voies à la fois.
Trois principales façons dont les tumeurs dissimulent la cible
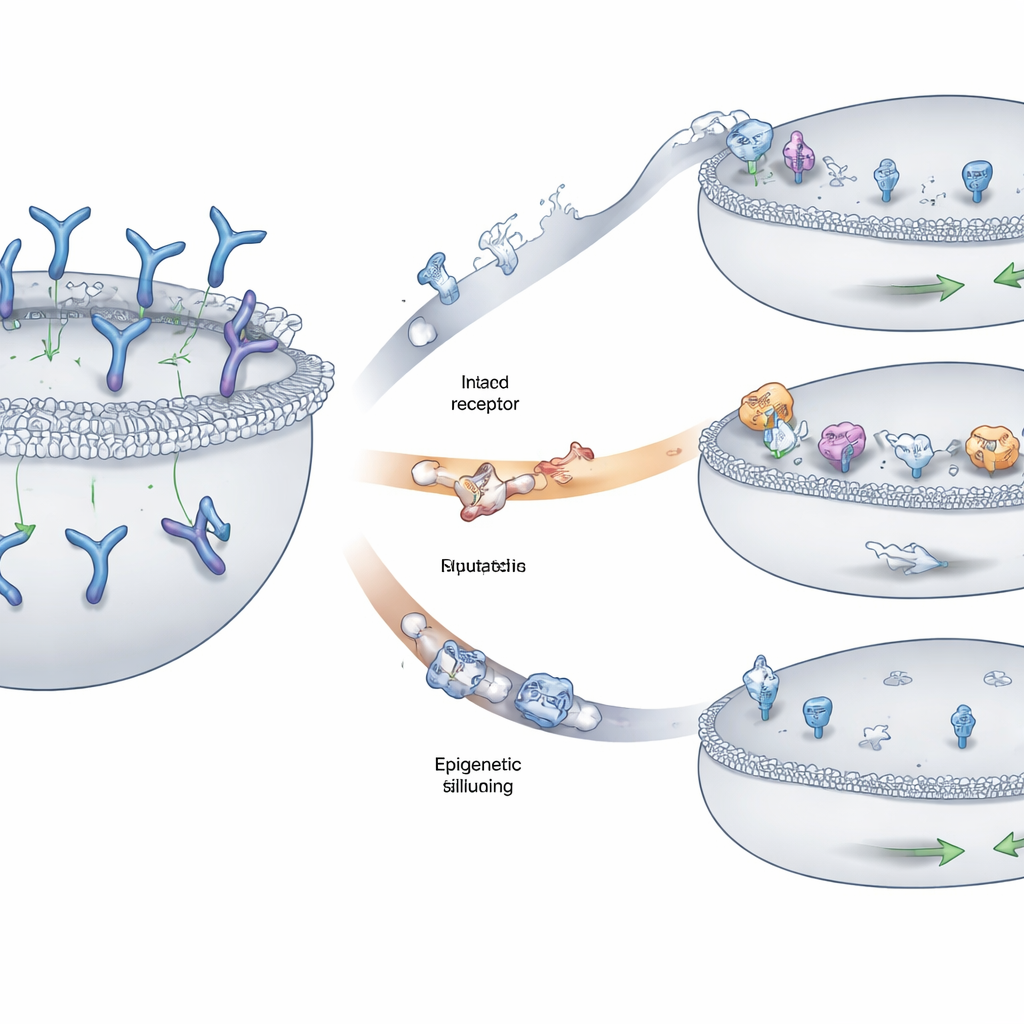
L’équipe a identifié trois schémas récurrents par lesquels les cellules de myélome échappaient à la reconnaissance. Chez certains patients, des fragments du chromosome porteuse du gène GPRC5D ont été supprimés sur les deux copies, effaçant complètement le drapeau de la surface cellulaire. Chez d’autres, des modifications plus petites — substitutions d’une seule lettre d’ADN ou petites insertions et délétions — ont déformé des régions clés de la protéine GPRC5D. Beaucoup de ces altérations perturbaient des parties de la protéine nécessaires à son acheminement correct de l’intérieur de la cellule jusqu’à la membrane externe, provoquant le piégeage de GPRC5D dans un compartiment interne au lieu d’être exposée là où le médicament peut la détecter. Une troisième voie impliquait un silence épigénétique : l’ADN entourant GPRC5D devenait étroitement compacté et chimiquement marqué de sorte que le gène était à peine lu, même si la séquence sous‑jacente restait largement intacte. Les cellules tumorales utilisant cette stratégie produisaient peu ou pas de GPRC5D.
Quand le drapeau est présent mais que la serrure ne correspond plus
Toutes les voies d’échappement n’éliminaient pas GPRC5D de la surface cellulaire. Dans certains cas, la protéine avait l’air normale aux tests de laboratoire standard mais ne convenait plus au médicament comme une clé dans une serrure. L’équipe a recréé des mutations spécifiques dérivées de patients dans des lignées cellulaires en laboratoire et a testé la capacité de différents anticorps ciblant GPRC5D à se lier et à tuer ces cellules. Une mutation a subtilement modifié l’endroit précis où talquetamab saisit le récepteur, réduisant fortement la capacité du médicament à se lier et à déclencher la mort cellulaire, même si le récepteur restait visible par coloration de routine. De façon intrigante, un autre médicament dirigé contre GPRC5D qui s’accroche au récepteur en deux sites restait efficace contre plusieurs de ces mutants, soulignant comment la conception du médicament — par exemple l’utilisation d’unions multivalentes ou ciblant plusieurs épitopes — peut influencer la survie des clones résistants.
Au‑delà de la cible : autres limites à l’attaque immunitaire
Alors que la plupart des rechutes présentaient une forme de perte ou d’altération de GPRC5D, une minorité de patients rechutaient sans changements évidents de la cible elle‑même. Dans ces cas, le problème semblait se situer au niveau des cellules T : elles étaient moins aptes et moins capables de tuer les cellules cancéreuses lors d’essais en laboratoire, ce qui suggère qu’une exposition continue à long terme à la thérapie engageante peut épuiser le système immunitaire. L’étude a aussi révélé qu’un sous‑type génétique particulier de myélome (impliquant un échange chromosomique appelé t(11;14)) maintient naturellement le gène GPRC5D dans un état de chromatine plus « fermé », avec une expression de base plus faible. Cela laisse supposer que certains patients peuvent être prédisposés à de mauvaises réponses parce que leurs tumeurs commencent avec des niveaux atténués du drapeau cible.
Ce que cela signifie pour les patients et les traitements futurs
Pour les patients et les cliniciens, ce travail explique pourquoi même des thérapies ciblant GPRC5D très puissantes ne sont pas encore des cures : les cellules de myélome peuvent supprimer, remanier, mal acheminer ou éteindre le drapeau même dont dépendent ces médicaments, et elles le font souvent de plusieurs manières à la fois. Les résultats suggèrent que surveiller l’ADN tumoral, plutôt que de se contenter de mesurer les niveaux de protéine, sera important pour détecter les mutations d’échappement émergentes que les tests de routine peuvent manquer. Ils orientent également vers des stratégies de prochaine génération — telles que des médicaments se liant à GPRC5D avec plus d’affinité à plusieurs sites, des associations ciblant plusieurs antigènes simultanément, ou des agents rouvrant des gènes silencés — pour devancer l’évolution tumorale. En substance, cette étude cartographie les voies d’échappement utilisées par le myélome afin que les thérapies futures puissent être conçues pour les bloquer, prolongeant l’efficacité des traitements basés sur les cellules T.
Citation: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Mots-clés: myélome multiple, engageurs de cellules T, GPRC5D, échappement antigénique, immunothérapie contre le cancer