Clear Sky Science · fr
Thérapie CAR-T à ARN messager dirigée contre BCMA pour la myasthénie grave : essai de phase 2b randomisé, en double aveugle et contrôlé par placebo
Pourquoi cette étude importe dans la vie quotidienne
La myasthénie grave est une maladie chronique qui rend des gestes simples — comme monter des escaliers, mâcher un repas ou garder les paupières ouvertes — soudainement difficiles. De nombreuses personnes ont besoin d’années de traitements immunosuppresseurs puissants qui peuvent entraîner des effets indésirables sérieux. Cette étude a testé un nouveau type de traitement cellulaire unique visant à calmer la maladie pendant au moins un an avec seulement six perfusions hebdomadaires, réduisant potentiellement le besoin de médicaments permanents.
Une maladie des muscles fatigués
Dans la myasthénie grave, les défenses de l’organisme attaquent par erreur la « poignée de main » entre les nerfs et les muscles. Des anticorps produits par certains cellules immunitaires bloquent et endommagent les sites d’ancrage qui permettent normalement aux signaux nerveux de déclencher le mouvement musculaire. Avec le temps, les personnes développent des paupières tombantes, une parole pâteuse, des difficultés à avaler et une faiblesse des bras, des jambes et des muscles respiratoires. Les traitements standards atténuent le système immunitaire de manière globale, ce qui peut aider, mais laissent souvent des symptômes persistants et augmentent le risque d’infections, de prise de poids, de troubles de l’humeur et d’autres problèmes liés aux médicaments.
Un nouveau type de thérapie cellulaire sur mesure
La thérapie testée ici, appelée Descartes-08, adopte une approche plus ciblée. Les médecins prélèvent d’abord les propres cellules T d’un patient — des cellules immunitaires pouvant être entraînées à reconnaître des cibles spécifiques — à partir du sang. En laboratoire, ces cellules sont temporairement équipées d’instructions génétiques, transportées sous forme d’ARNm, qui leur apprennent à reconnaître une protéine appelée BCMA à la surface des cellules productrices d’anticorps responsables de la maladie. Contrairement aux thérapies cellulaires anticancéreuses classiques qui utilisent des modifications virales permanentes et nécessitent une chimiothérapie préalable, ce dispositif est de courte durée et ne requiert pas de traitement visant à anéantir le système immunitaire. Les patients reçoivent Descartes-08 sous forme de six brèves perfusions hebdomadaires en consultation ambulatoire. 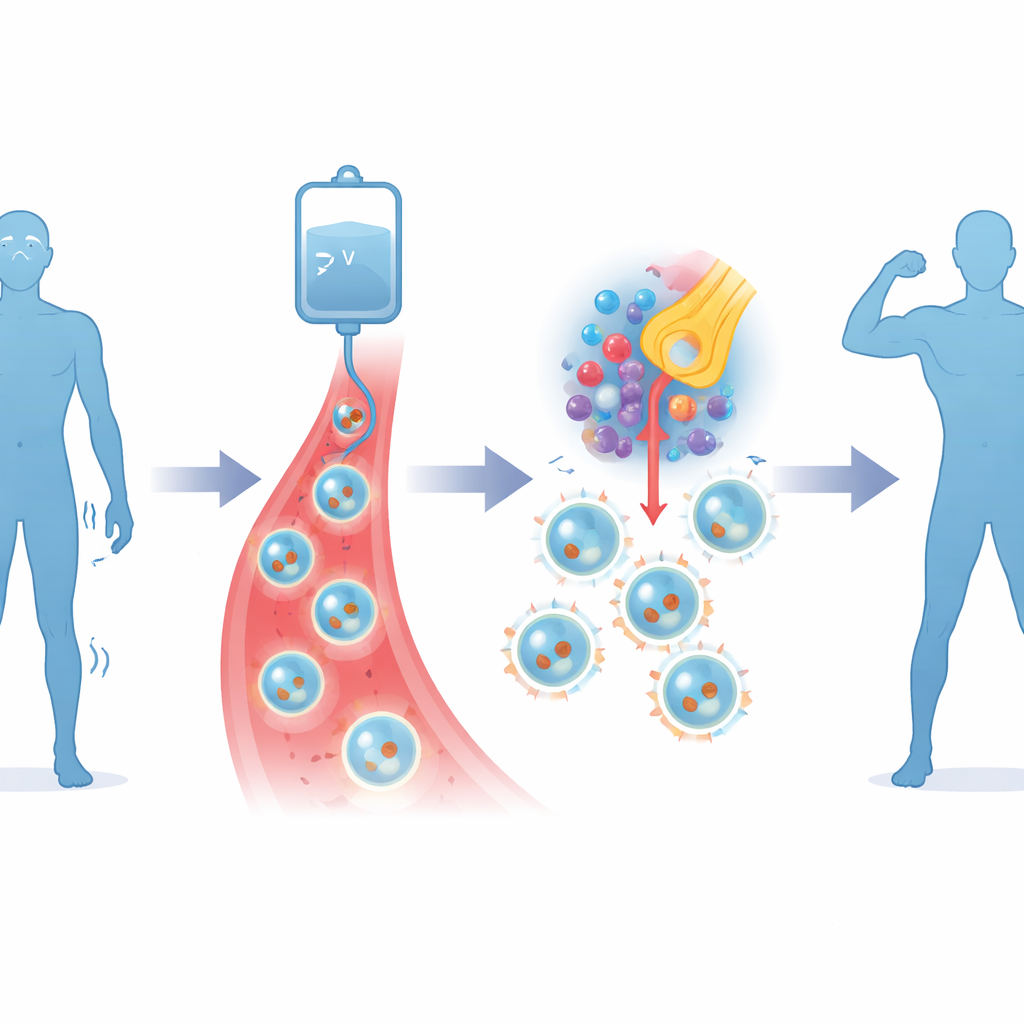
Mettre l’idée à l’épreuve de manière équitable
Cet essai de phase 2b a inclus des adultes atteints de myasthénie grave généralisée dont la maladie touchait plus que les muscles oculaires et qui étaient déjà sous traitements standards. Les participants ont été répartis au hasard pour recevoir soit Descartes-08, soit une perfusion placebo identique, et ni eux ni leurs médecins ne savaient quel traitement ils recevaient. Le critère principal était un score largement utilisé qui combine le ressenti fonctionnel quotidien des patients et les tests de force réalisés par les médecins. Les chercheurs ont demandé : trois mois après le traitement, combien de personnes s’étaient améliorées d’au moins cinq points — plus que ce que les experts considèrent comme un changement significatif ? Ils ont aussi suivi la durée des améliorations, la possibilité pour les patients de réduire leur dose de stéroïdes, et les effets secondaires sur une année complète.
Des muscles plus forts, moins de symptômes
Parmi les 26 participants inclus dans l’analyse principale, ceux ayant reçu Descartes-08 avaient plus de deux fois plus de chances d’atteindre l’amélioration ciblée à trois mois que ceux sous placebo (environ deux tiers contre un quart). En moyenne, les patients traités ont montré des baisses plus importantes des scores de gravité des symptômes et de meilleurs résultats aux tests de force que le groupe placebo, et ces gains se sont généralement renforcés au cours des quatre premiers mois et étaient encore présents à un an. Environ un patient sur trois a atteint une « expression symptomatique minimale », c’est-à-dire que son score quotidien de symptômes était proche de zéro, et cela était encore plus fréquent — chez plus de la moitié — chez les personnes n’ayant jamais reçu auparavant des médicaments biologiques récents. De nombreux patients sous Descartes-08 ont également pu réduire leur dose de stéroïdes d’environ moitié après six mois, tandis que les doses du groupe placebo sont restées à peu près inchangées. 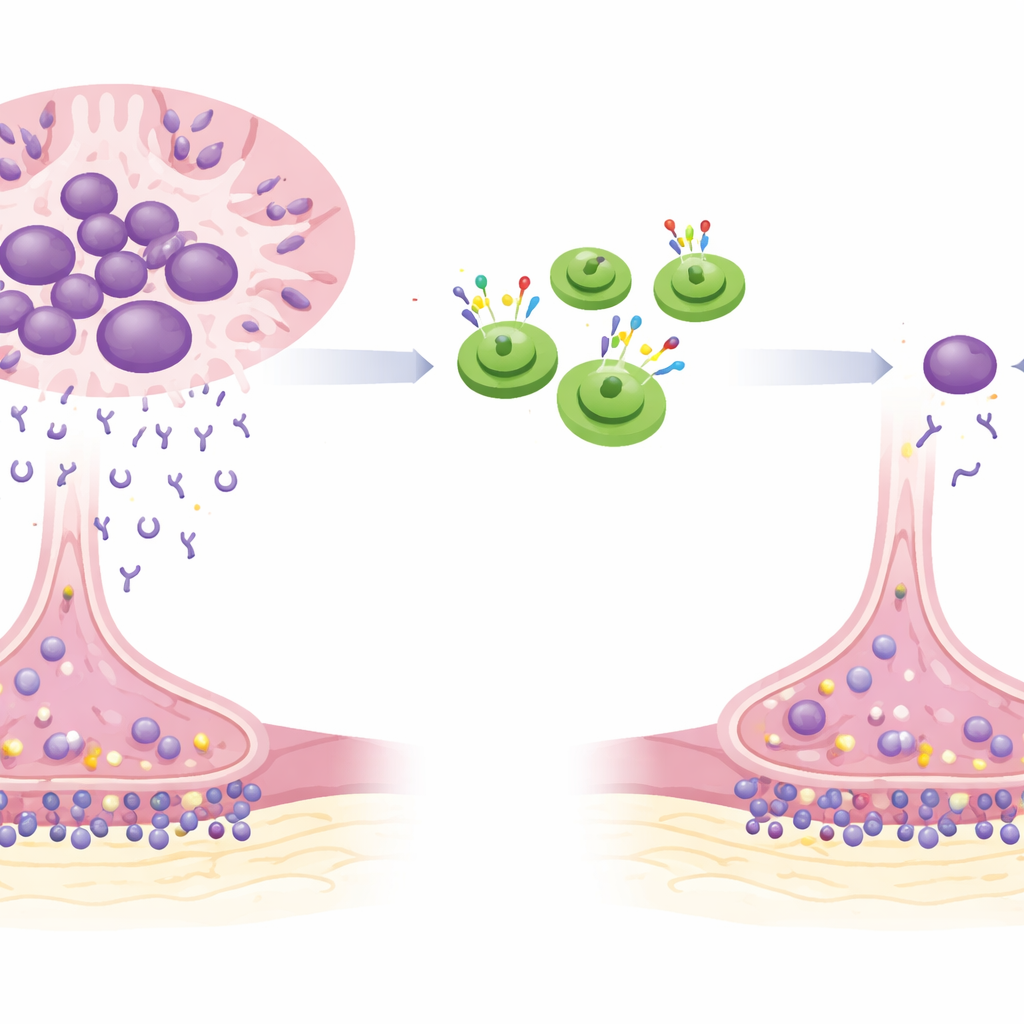
Sécurité et effets sur le système immunitaire
Les effets secondaires étaient fréquents mais pour la plupart légers à modérés dans les deux groupes. Les problèmes les plus fréquents avec Descartes-08 étaient des réactions transitoires à la perfusion — fièvre, frissons, maux de tête et courbatures — qui se résorbaient généralement en moins d’un jour sans traitement particulier. Des complications graves comme des orages immunitaires menaçant la vie ou des effets cérébraux majeurs, qui peuvent survenir avec certaines thérapies cellulaires anticancéreuses, n’ont pas été observées. Fait important, les analyses sanguines ont montré que les taux globaux d’anticorps et les réponses de protection aux vaccins étaient conservés, ce qui suggère que la thérapie a principalement réduit les cellules responsables de la maladie au lieu d’anéantir largement le système immunitaire. Des mesures exploratoires ont laissé entendre que certains signaux inflammatoires liés à l’auto-immunité diminuaient après le traitement, cohérent avec un « réajustement » plus précis de la réponse immunitaire mal dirigée.
Ce que cela pourrait signifier pour les patients
Pour les personnes vivant avec la myasthénie grave, ces résultats suggèrent qu’une courte série de perfusions cellulaires personnalisées pourrait offrir un soulagement significatif et durable tout en permettant de réduire les médicaments immunosuppresseurs du quotidien. L’étude était relativement petite, et certaines différences au-delà du critère principal nécessitent confirmation dans des essais plus larges, mais le schéma cohérent d’amélioration et les effets secondaires généralement maîtrisables sont encourageants. Si des études ultérieures confirment ces résultats, la thérapie cellulaire à base d’ARNm pourrait devenir une nouvelle option permettant de contrôler la maladie de façon plus précise et pratique, rapprochant de nombreux patients d’une vie avec des symptômes minimaux plutôt que d’une fatigue constante et d’un fardeau médical permanent.
Citation: Vu, T., Durmus, H., Rivner, M. et al. BCMA-directed mRNA CAR T cell therapy for myasthenia gravis: a randomized, double-blind, placebo-controlled phase 2b trial. Nat Med 32, 1131–1141 (2026). https://doi.org/10.1038/s41591-025-04171-y
Mots-clés: myasthénie grave, thérapie cellulaire, cellules CAR T, maladie auto-immune, thérapeutiques à ARNm