Clear Sky Science · fr
Linavonkibart et pembrolizumab dans les tumeurs solides avancées résistantes au blocage des points de contrôle immunitaire : un essai de phase 1
Pourquoi les cancers récalcitrants nous concernent tous
Les médicaments d’immunothérapie qui « retirent les freins » du système immunitaire ont transformé la prise en charge de nombreux cancers, mais la plupart des patients n’en tirent jamais avantage ou voient leurs tumeurs réapparaître avec le temps. Cette étude évalue un nouvel anticorps, linavonkibart, conçu pour neutraliser un puissant bouclier que les tumeurs utilisent pour se dissimuler des attaques immunitaires, en l’associant à une immunothérapie existante, le pembrolizumab. Les résultats offrent un premier aperçu selon lequel, même chez des patients dont les cancers ne répondaient plus aux inhibiteurs de points de contrôle, il pourrait être possible de restaurer le contrôle immunitaire tout en maintenant des effets indésirables acceptables.
Un bouclier caché autour des tumeurs
Beaucoup d’immunothérapies modernes agissent en bloquant les molécules dites de point de contrôle, comme PD‑1, qui limitent normalement l’activité des lymphocytes T. Quand ces freins sont levés, les cellules immunitaires peuvent attaquer le cancer plus vigoureusement. Mais les tumeurs s’adaptent souvent en construisant un environnement hostile qui empêche les lymphocytes T tueurs d’accéder à la tumeur ou les affaiblit une fois sur place. Un acteur central de cette bulle protectrice est une protéine de signalisation appelée TGFβ1, produite à la fois par les cellules cancéreuses et par les cellules de soutien avoisinantes. Les tentatives antérieures visant à bloquer l’ensemble de la famille TGFβ ont montré un certain potentiel mais ont entraîné de graves problèmes cardiaques et hémorragiques, car d’autres membres de cette famille sont importants pour les tissus sains. Linavonkibart a été conçu pour contourner cette difficulté en neutralisant sélectivement uniquement la forme latente, inactive, de la TGFβ1 avant son activation, tout en épargnant les molécules apparentées dont l’organisme a besoin.
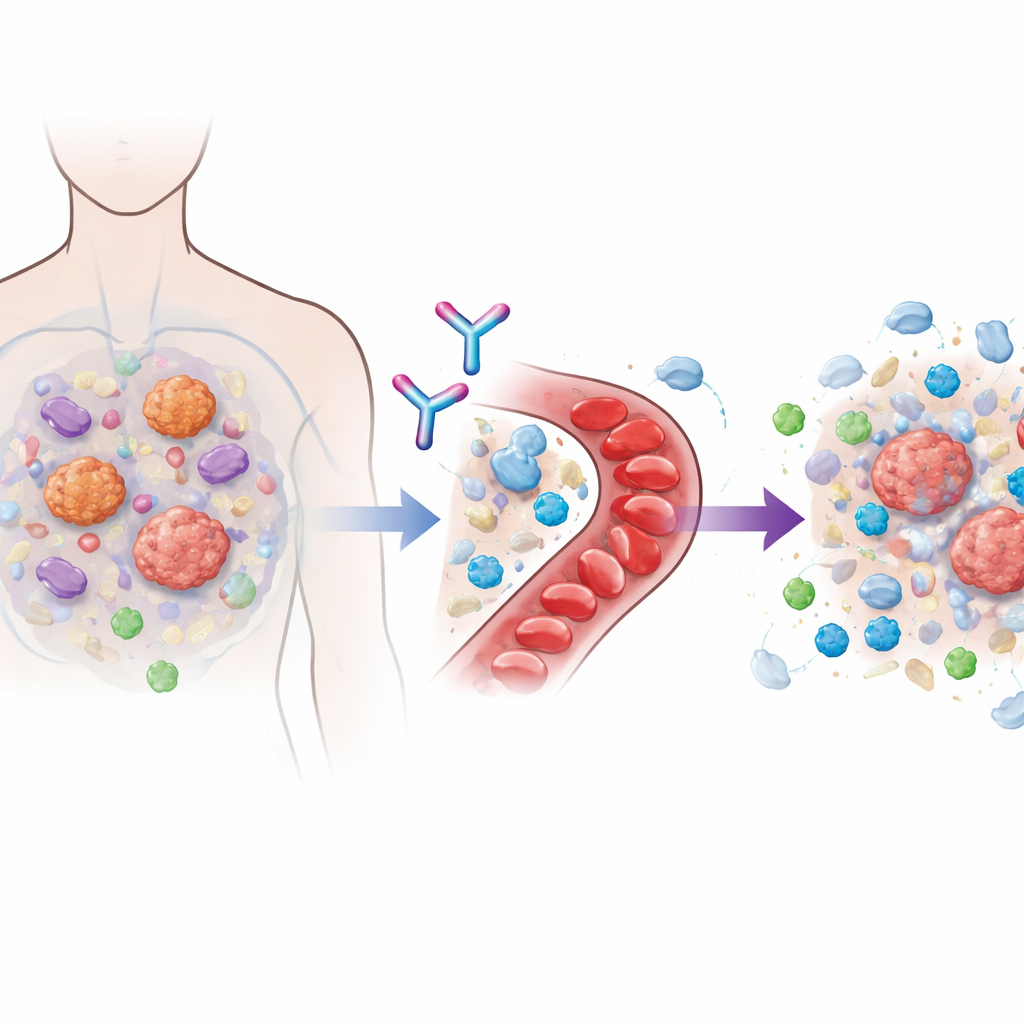
Concevoir un premier essai humain prudent
L’essai DRAGON était une étude de phase 1 multicentrique menée dans 22 hôpitaux aux États‑Unis et en Corée du Sud. Il a inclus 112 adultes atteints de tumeurs solides avancées, tous ayant des options thérapeutiques limitées. Dans la première partie de l’étude, le linavonkibart était administré seul à des doses croissantes à de petits groupes de patients, ou en association avec leur traitement antérieur à base d’inhibiteur de PD‑1. Cette approche progressive visait à dresser la carte de la sécurité, de la pharmacocinétique et de la pharmacodynamie, et à choisir une dose pour des tests plus larges. Dans la deuxième partie, 78 patients dont les cancers avaient déjà résisté à au moins un traitement par PD‑1 ont reçu une dose fixe de linavonkibart associée au pembrolizumab. Ces patients souffraient de cancers difficiles à traiter, notamment un cancer du rein à cellules claires, un mélanome, des cancers de la tête et du cou, un cancer urothélial (de la vessie) et un cancer du poumon, et la plupart avaient suivi plusieurs lignes de traitement précédentes.
La sécurité d’abord : ce qui est arrivé aux patients
L’objectif principal de cette étude en phase précoce était la sécurité, et linavonkibart s’est montré encourageant à cet égard. À tous les niveaux de dose, aucune dose maximale tolérable n’a été atteinte, et aucun effet indésirable limitant la dose ni décès liés au médicament n’ont été observés. Lorsqu’il a été associé au pembrolizumab à la dose choisie pour la phase 2, environ trois quarts des patients ont présenté un effet indésirable lié au traitement, ce qui est comparable à ce que l’on observe souvent avec l’immunothérapie seule. Des éruptions cutanées et des démangeaisons étaient les problèmes additionnels les plus fréquents, et un petit nombre de patients a développé des inflammations cutanées ou pulmonaires plus sévères. Fait important, le syndrome d’activation des cytokines, réaction immunitaire excessive dangereuse pouvant survenir avec certains anticorps, n’a pas été observé, et le profil global de sécurité ressemblait en grande partie à celui du pembrolizumab administré seul.
Des indices que le système immunitaire peut être réveillé
Bien qu’il ne s’agisse pas d’un vaste essai d’efficacité définitif, plusieurs signes ont suggéré que l’inhibition de la TGFβ1 pouvait aider à raviver les réponses au blocage de PD‑1. Lors de la phase d’expansion, la combinaison linavonkibart–pembrolizumab a réduit des tumeurs mesurables chez une fraction notable de patients qui avaient auparavant cessé de bénéficier des inhibiteurs de PD‑1. Les taux de réponse confirmés étaient de 20 % pour le cancer du rein à cellules claires, 18,2 % pour le mélanome, et juste au‑dessus de 9 % pour les cancers de la tête et du cou et urothéliaux, un patient atteint d’un cancer du rein obtenant une disparition complète des lésions visibles. Beaucoup de ces réponses ont duré plusieurs mois, et les patients répondeurs sont restés sous la combinaison plus longtemps que sous leur traitement PD‑1 antérieur. Des biopsies prélevées avant et après le traitement apportent une explication biologique : les tumeurs présentaient une infiltration accrue de lymphocytes T CD8 « tueurs », des niveaux plus élevés de lymphocytes T activés, moins de cellules T régulatrices suppressives et moins de cellules myéloïdes suppressives, ainsi qu’un glissement global vers un microenvironnement plus inflammatoire et prêt à l’attaque.
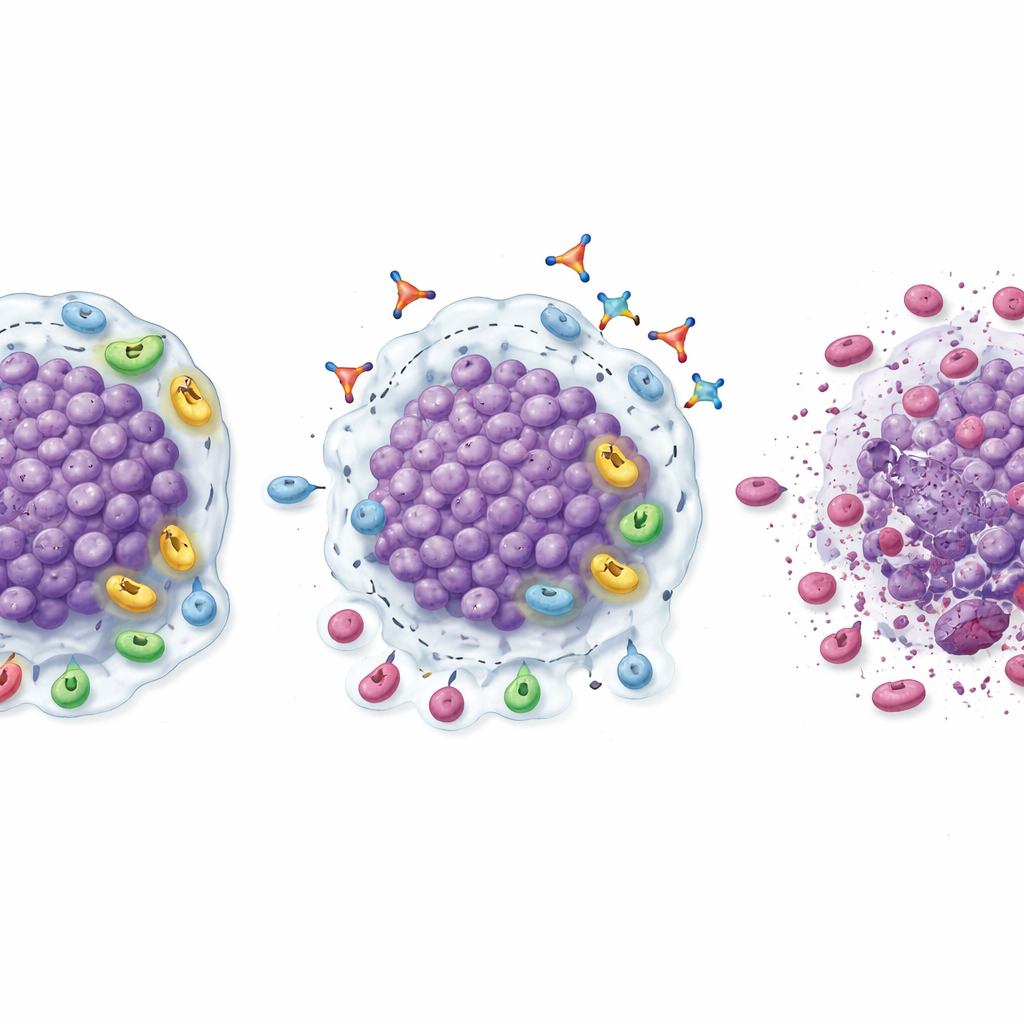
Identifier ceux qui pourraient le plus bénéficier
Les chercheurs ont également exploré quels patients étaient particulièrement susceptibles de répondre. Dans le cancer du rein à cellules claires, les tumeurs contenant déjà un grand nombre de lymphocytes T CD8 au départ — mais riches également en cellules T régulatrices et exprimant des niveaux élevés de TGFβ1 — étaient plus susceptibles de diminuer sous la thérapie combinée. Chez ces patients, les taux de réponse et la survie sans progression étaient sensiblement plus élevés que dans le groupe rénal plus large. Ce schéma suggère un « point idéal » : les tumeurs qui disposent d’un grand nombre de soldats immunitaires mais qui sont retenues par une suppression dirigée par la TGFβ1 pourraient être des candidates idéales pour linavonkibart associé au blocage PD‑1. Si cela est confirmé dans des études plus larges, des tests tissulaires simples pour ces marqueurs pourraient aider les médecins à sélectionner les patients les plus susceptibles de bénéficier du traitement.
Ce que signifie ce travail pour l’avenir
Pour les personnes confrontées à des cancers avancés qui ont déjà résisté à l’immunothérapie, la perspective de réactiver leur propre système immunitaire sans ajouter une toxicité sévère est séduisante. Ce premier essai chez l’humain fournit des preuves initiales que neutraliser sélectivement le bouclier TGFβ1 avec linavonkibart peut se faire en sécurité et peut restaurer un contrôle tumoral significatif lorsqu’on l’associe à un inhibiteur de PD‑1, en particulier dans certains cancers rénaux. Bien que l’étude soit de petite taille et non randomisée, son bilan de sécurité, ses lectures biologiques et ses réponses durables constituent un argument solide en faveur d’essais de phase 2 plus importants. Si des études ultérieures confirment ces résultats, cette approche pourrait élargir le cercle des patients pouvant bénéficier de l’immunothérapie, transformant certains cancers actuellement récalcitrants en tumeurs à nouveau vulnérables aux défenses de l’organisme.
Citation: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Mots-clés: immunothérapie du cancer, inhibition de la TGFβ1, résistance aux points de contrôle immunitaire, carcinome rénal à cellules claires, microenvironnement tumoral