Clear Sky Science · fr
Paysage interpretable de l'inflammation des cellules immunitaires circulantes
Pourquoi l'inflammation dans le sang vous concerne
L'inflammation est au cœur de nombreuses maladies, de l'arthrite et de l'asthme au COVID-19 et au cancer. Pourtant, les médecins ont encore du mal à lire les signaux inflammatoires du corps de manière à expliquer clairement ce qui dysfonctionne et quel traitement sera le plus efficace. Cette étude construit une immense « carte » des cellules immunitaires circulant dans le sang et montre comment ces cellules pourraient servir de biomarqueurs vivants, faciles à échantillonner, pour classer un large éventail de maladies inflammatoires.
Construire une carte géante des cellules immunitaires
Pour cartographier ce paysage, les chercheurs ont analysé plus de 6,5 millions de cellules immunitaires prélevées dans le sang de 1 047 personnes. Ces volontaires couvraient 19 affections, notamment des maladies auto-immunes comme le lupus et la polyarthrite rhumatoïde, des maladies pulmonaires chroniques comme l'asthme et la BPCO, des infections telles que le COVID-19 et le VIH, et plusieurs cancers, ainsi que des donneurs sains. Grâce au séquençage ARN unicellulaire, ils ont mesuré quels gènes étaient activés dans chaque cellule, puis utilisé des méthodes statistiques avancées pour corriger les différences techniques entre les études et regrouper les cellules en 64 états cellulaires immunitaires distincts. Cet « Atlas de l'inflammation » capture à la fois des acteurs connus — comme les cellules T, les cellules B et les monocytes — et des sous‑types plus spécialisés qui évoluent avec la maladie.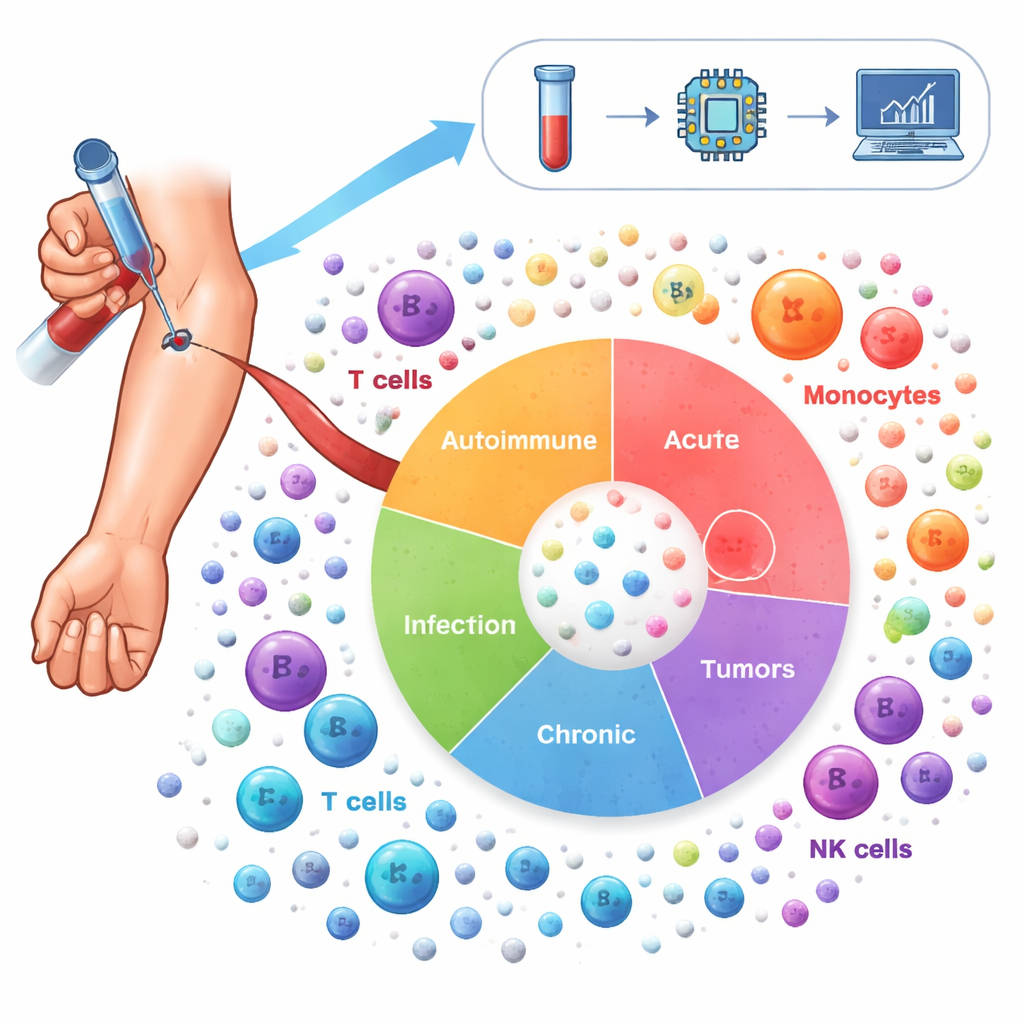
Lire les signatures inflammatoires du corps
L'équipe s'est ensuite concentrée sur les gènes qui contrôlent l'activation des cellules immunitaires, leur déplacement dans l'organisme, la présentation d'antigènes et la réponse à des molécules de signalisation comme les interférons et le facteur de nécrose tumorale. Ils ont regroupé ces gènes en 21 « signatures » biologiques et les ont affinées pour chaque type cellulaire majeur. En comparant les patients aux donneurs sains, ils ont pu voir quelles signatures étaient amplifiées ou diminuées selon les maladies. Par exemple, de nombreuses maladies inflammatoires à médiation immune présentaient une activité accrue des molécules d'adhésion et du mécanisme de présentation d'antigène, tandis que les réponses aux interférons étaient abaissées dans la plupart des types cellulaires mais augmentées dans certains lymphocytes T CD8. Les infections virales comme la grippe et le COVID-19 stimulaient les programmes induits par les interférons, alors que des infections chroniques comme le VIH et l'hépatite B les affaiblissaient.
Approfondir les gènes-clés et les interrupteurs de contrôle
Parce que les signatures larges masquent encore des détails importants, les chercheurs sont descendus au niveau des gènes individuels et de leurs régulateurs. Dans les lymphocytes T CD8 non naïfs, ils ont trouvé que deux gènes, FGFBP2 et GZMB, étaient particulièrement actifs dans certains sous-types de mémoire effectrice, en particulier dans la rectocolite hémorragique. Ces gènes ont été associés à des dommages aux surfaces épithéliales, et leur signal fort dans le sang suggère que ces cellules agressives sont déjà prêtes avant d'entrer dans les tissus. Une analyse distincte des réseaux de régulation génique a mis en évidence deux facteurs de transcription, STAT1 et SP1, comme contrôleurs centraux des programmes induits par les interférons. Leurs profils d'activité différaient selon les maladies et les types cellulaires — par exemple un comportement opposé dans les monocytes par rapport aux lymphocytes T CD8 dans le lupus, et des variations entre phases de poussée et phases non‑poussée — laissant entrevoir comment les mêmes voies peuvent être protectrices dans un contexte et nocives dans un autre.
Entraîner des machines à repérer la maladie à partir des cellules sanguines
Pour transformer cet atlas en outil pratique, l'équipe a appliqué de l'apprentissage automatique interprétable. Ils ont entraîné des modèles d'arbres de décision à gradient boosté séparément pour chaque type cellulaire majeur, demandant aux algorithmes d'étiqueter les cellules individuelles selon la maladie d'après leur expression génique. Ces modèles ont atteint une grande précision lorsqu'ils ont été testés sur des échantillons mis de côté, surtout après correction des différences techniques. En utilisant SHAP, une méthode qui explique quels gènes motivent chaque décision, les chercheurs ont pu identifier des biomarqueurs candidats. Un exemple est CYBA dans les monocytes, dont les niveaux ont aidé à distinguer des maladies cutanées comme le psoriasis des inflammations intestinales comme la maladie de Crohn et la rectocolite hémorragique. Un autre est IFITM1 dans certains lymphocytes T et cellules lymphoïdes innées, séparant l'asthme de la BPCO et suggérant différents schémas de défense antivirale chronique.
Vers une boussole diagnostique basée sur le sang
Enfin, les auteurs se sont demandé si des patients entiers — pas seulement des cellules individuelles — pouvaient être classés à partir de leurs profils immunitaires circulants. Ils ont projeté les données de chaque cellule dans un espace d'« embedding » compressé, moyenné ces embeddings par type cellulaire pour chaque patient, puis entraîné des classificateurs pour prédire la maladie. Lorsque de nouveaux patients ressemblaient à ceux des données d'entraînement, les performances étaient excellentes. Mais lorsque les échantillons provenaient d'études complètement indépendantes utilisant des méthodes de laboratoire différentes, la précision chutait fortement, révélant la sensibilité de tels outils à la variabilité technique. Un jeu de données « centralisé » plus contrôlé, généré dans un seul centre avec une chimie de séquençage unique, a permis de restaurer une grande partie des performances, soulignant le besoin de protocoles standardisés ou d'ensembles d'entraînement très larges et diversifiés.
Ce que cela signifie pour le diagnostic et le traitement futurs
Pour le grand public, le message clé est que vos cellules immunitaires circulantes portent une empreinte riche de l'état inflammatoire de votre corps. En lisant ces empreintes cellule par cellule, ce travail montre qu'il est possible de distinguer de nombreuses maladies, de découvrir des gènes susceptibles de provoquer des symptômes spécifiques et de commencer à construire des tests sanguins universels qui classent les maladies inflammatoires. L'étude n'est pas encore un test clinique prêt à l'emploi — les différences techniques entre les études limitent encore la fiabilité — mais elle jette les bases d'outils futurs de « biopsie liquide » qui pourraient aider les médecins à identifier plus tôt le bon diagnostic et le bon traitement, à partir d'une simple prise de sang.
Citation: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Mots-clés: inflammation, cellules immunitaires, séquençage ARN unicellulaire, biomarqueurs, apprentissage automatique