Clear Sky Science · fr
Thérapie anti‑inflammatoire par IL‑2 à faible dose dans les syndromes coronariens aigus : un essai randomisé de phase 2
Pourquoi calmer l’inflammation artérielle est important
Beaucoup de personnes qui survivent à un infarctus ou à une douleur thoracique grave restent à haut risque d’un nouvel épisode, même lorsqu’elles prennent des traitements standard comme les statines et les anticoagulants. Une des raisons majeures est une inflammation persistante à l’intérieur des artères, qui maintient les parois vasculaires irritées et instables. Cette étude pose une question simple mais importante : peut‑on, en toute sécurité, inciter le système immunitaire à apaiser cette inflammation en utilisant de très faibles doses d’une protéine de signalisation naturelle appelée interleukine‑2 (IL‑2) ? Si tel est le cas, cela pourrait ouvrir une nouvelle voie pour protéger le cœur au‑delà des médicaments traditionnels abaissant le cholestérol.
Une nouvelle manière d’orienter le système immunitaire
Les chercheurs se sont concentrés sur un groupe particulier de globules blancs appelés cellules T régulatrices, ou Tregs. Ces cellules jouent le rôle de « pacificateurs » immunitaires, aidant à éteindre une inflammation excessive et à favoriser la réparation. Des études antérieures ont montré que les personnes atteintes de syndromes coronariens aigus — infarctus et affections apparentées — ont moins de Tregs et des Tregs moins efficaces. À fortes doses, l’IL‑2 peut stimuler des cellules immunitaires agressives et est utilisée en cancérologie, mais à très faibles doses elle favorise principalement les Tregs. L’équipe a conçu l’essai IVORY pour tester si l’IL‑2 à faible dose, administrée après un événement cardiaque en complément des soins habituels, pouvait augmenter en toute sécurité les Tregs et réduire l’inflammation artérielle.
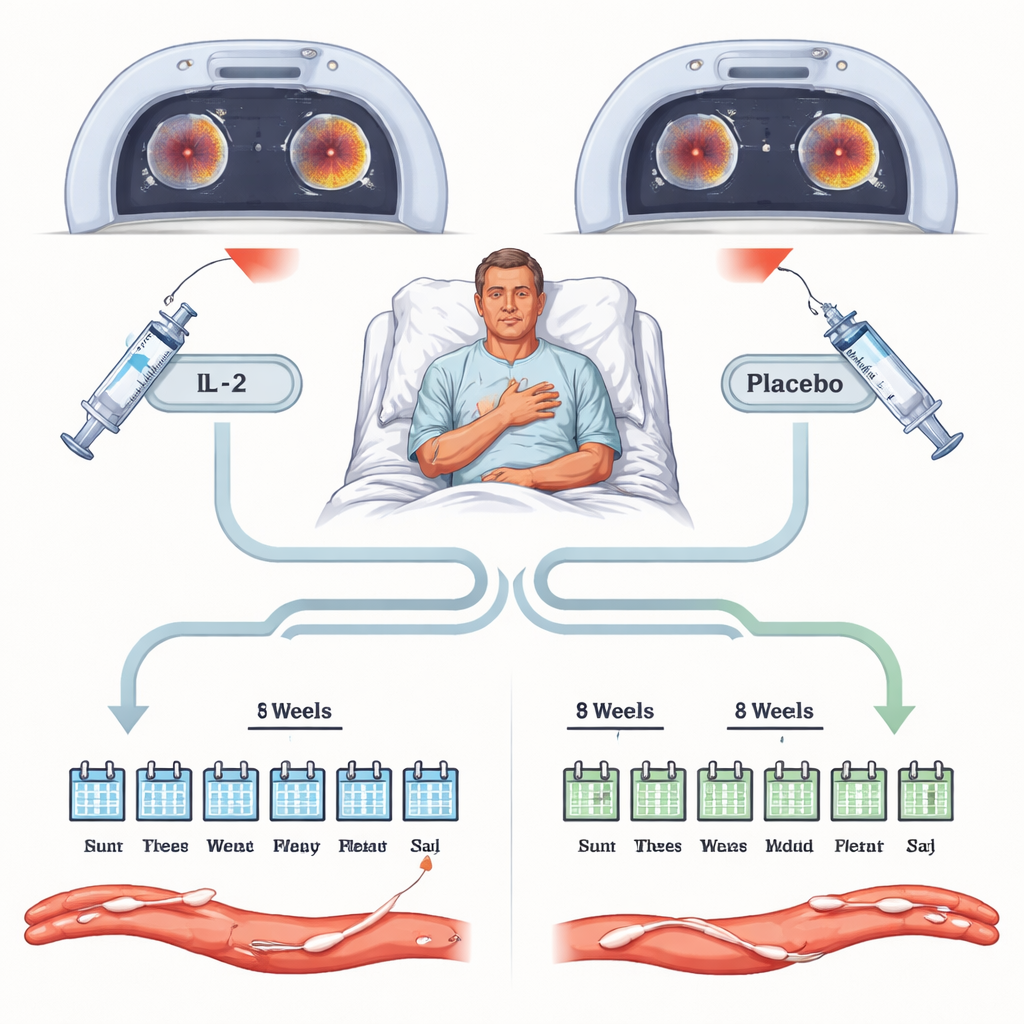
Déroulement de l’essai
L’étude a recruté des adultes récemment hospitalisés pour un syndrome coronarien aigu et présentant encore des signes d’inflammation systémique, mesurés par un test sanguin appelé protéine C‑réactive ultra‑sensible. Soixante‑trois patients ont été assignés aléatoirement, en double aveugle, pour recevoir soit l’IL‑2 à faible dose soit une injection placebo pendant huit semaines, en plus des traitements standard tels que statines et antiagrégants. Tous ont bénéficié d’examens PET–TDM spécialisés de l’aorte thoracique principale et des artères du cou avant le traitement puis à la fin des huit semaines. Ces examens mesurent la captation d’un sucre radioactif par la paroi artérielle, fournissant un indicateur sensible de l’inflammation. Le critère principal était la différence d’inflammation artérielle entre les groupes IL‑2 et placebo à la fin du traitement.
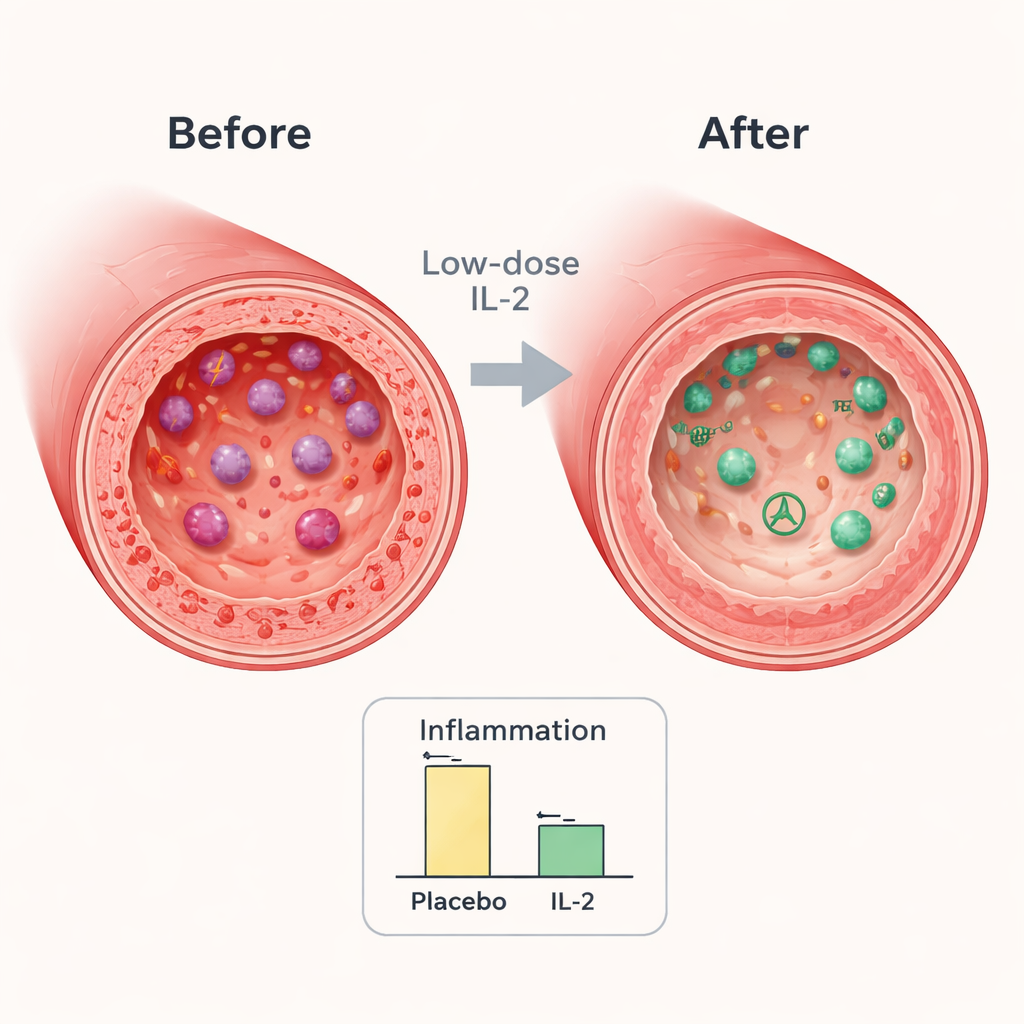
Ce qui a changé à l’intérieur des artères
À la fin de l’essai, les deux groupes ont montré une certaine réduction de l’inflammation artérielle, ce qui est attendu tandis que les patients se rétablissent et reçoivent un traitement standard intensif. Cependant, la baisse était significativement plus marquée chez ceux qui avaient reçu l’IL‑2 à faible dose. Dans l’artère clé choisie pour chaque patient, l’inflammation était environ 7–8 % plus faible dans le groupe IL‑2 que dans le groupe placebo. Lorsque les chercheurs se sont concentrés sur les portions les plus enflammées des vaisseaux, la différence est passée à environ 9 %. Ces réductions sont de l’ordre de grandeur de celles observées dans des études où des médicaments plus puissants abaissant le cholestérol ont conduit à moins d’événements cardiaques futurs, ce qui suggère que ce changement est cliniquement significatif.
Réponse du système immunitaire
Les analyses sanguines réalisées pendant l’essai ont montré que l’IL‑2 produisait exactement l’effet escompté. Les niveaux de cellules T régulatrices ont augmenté rapidement et sont restés de 30 à 50 % supérieurs à ceux du groupe placebo pendant toute la durée du traitement. Parallèlement, certains types cellulaires associés à des réponses immunitaires plus agressives, incluant certaines cellules T auxiliaires et tueuses, ont tendance à diminuer ou à augmenter moins. Dans l’ensemble, le profil immunitaire a basculé vers un état plus apaisé et régulateur. Fait intéressant, un marqueur général d’inflammation sanguine, la protéine C‑réactive, n’a pas diminué sous IL‑2, ce qui suggère que le médicament agit via une voie plus ciblée qui peut ne pas se refléter dans des tests sanguins globaux mais qui est visible au sein de la paroi artérielle.
Sécurité et premiers indices sur les résultats cliniques
La sécurité était une préoccupation centrale, car atténuer des composantes du système immunitaire peut parfois augmenter les infections ou d’autres complications. Dans cet essai, l’IL‑2 à faible dose a été bien tolérée. L’effet indésirable le plus fréquent était une légère rougeur et des démangeaisons au site d’injection, qui disparaissaient en environ deux jours. Les taux d’infections et d’autres effets indésirables étaient similaires entre les groupes IL‑2 et placebo, et aucun problème grave lié au traitement n’a été signalé. Dans un suivi des patients sur deux ans, trois personnes du groupe placebo ont présenté des événements cardiovasculaires majeurs tels qu’infarctus, AVC ou décès cardiovasculaire, tandis qu’aucune n’a été constatée dans le groupe IL‑2, bien que ces chiffres soient trop faibles pour tirer des conclusions définitives.
Ce que cela pourrait signifier pour les patients
Pour le grand public, le message principal est que cette étude fournit une preuve de concept précoce mais encourageante : en renforçant doucement les « freins » du système immunitaire de l’organisme grâce à de très faibles doses d’IL‑2, il pourrait être possible de réduire l’inflammation nuisible des artères après un infarctus, sans ajouter d’effets secondaires majeurs. L’essai est trop petit pour prouver que cette approche prévient les futurs infarctus ou AVC, mais l’ampleur de l’effet anti‑inflammatoire et le bon profil de sécurité justifient des essais plus vastes axés sur les événements cliniques. Si cela se confirme, l’IL‑2 à faible dose ou des stratégies similaires d’ajustement immunitaire pourraient devenir un nouvel outil, aux côtés des statines et des anticoagulants, pour mieux protéger le cœur après un incident cardiaque grave.
Citation: Sriranjan-Rothwell, R.S., Zhao, T.X., Hoole, S.P. et al. Anti-inflammatory therapy with low-dose IL-2 in acute coronary syndromes: a randomized phase 2 trial. Nat Med 32, 624–632 (2026). https://doi.org/10.1038/s41591-025-04090-y
Mots-clés: syndrome coronarien aigu, inflammation artérielle, cellules T régulatrices, thérapie par interleukine‑2, immunologie cardiovasculaire