Clear Sky Science · fr
CD38 confère aux Treg antigène-spécifiques locaux une résilience au stress pour contrôler l’inflammation compartimentalisée du SNC
Pourquoi les cellules immunitaires qui protègent le cerveau sont importantes
De nombreuses maladies auto-immunes du cerveau, comme la sclérose en plaques, se comportent comme des foyers couvants : une flambée initiale d’inflammation s’apaise, mais des lésions peuvent réapparaître des années plus tard. Cette étude pose une question apparemment simple mais aux grandes implications : après une attaque dans le système nerveux central (SNC), qu’est-ce qui maintient la paix — et qu’est-ce qui fait basculer l’équilibre vers la maladie ? Les auteurs se concentrent sur une petite population de cellules immunitaires appelées cellules T régulatrices qui s’installent dans le cerveau et la moelle épinière après l’inflammation, et révèlent comment une seule molécule de surface leur permet de survivre dans un environnement hostile et d’empêcher les rechutes.
Les gardiens immunitaires qui restent sur place
En utilisant un modèle murin qui reproduit certains aspects de la sclérose en plaques, les chercheurs ont suivi différents types de cellules T au pic de la maladie puis pendant la phase de récupération. Alors que les cellules T auxiliaires classiques qui favorisent l’inflammation diminuaient en nombre à mesure que les symptômes s’amélioraient, les cellules T régulatrices — des cellules spécialisées qui atténuent normalement les réponses immunitaires — demeuraient dans le SNC. Leur part relative au sein du pool local de cellules T augmentait même, et elles se regroupaient en niches distinctes autour des espaces contenant le liquide cérébrospinal et des membranes protectrices entourant le cerveau. En étiquetant l’origine des cellules T entrantes, l’équipe a montré qu’après la récupération, très peu de nouvelles cellules T régulatrices arrivaient des ganglions lymphatiques. À la place, la population du SNC se maintenait largement localement, suggérant une force « maintien de la paix » résidente à long terme. 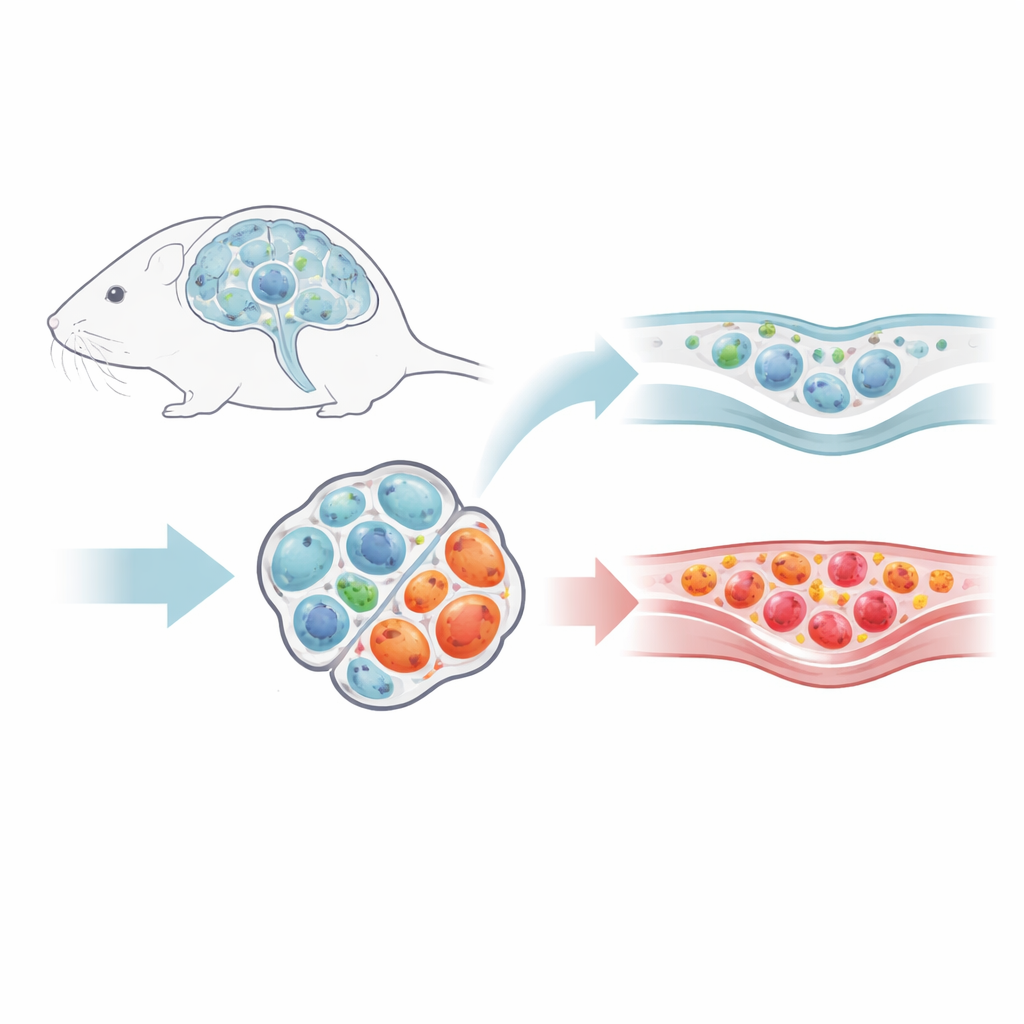
Gardiens tolérants au stress d’une niche hostile
Le SNC post-inflammatoire est loin d’être accueillant pour ces gardiens. Après la vague principale de la maladie, les niveaux du signal de croissance interleukine-2 (IL-2) — dont les cellules T régulatrices dépendent fortement — chutent car la plupart des cellules T conventionnelles se sont retirées. Parallèlement, le tissu est riche en la molécule métabolique NAD+, qui peut déclencher la mort cellulaire ou altérer des récepteurs de surface clés lorsqu’elle est modifiée par une enzyme spécifique. En marquant génétiquement et en suivant des cellules T régulatrices individuelles, les auteurs ont distingué des cellules « stables » qui conservaient leur identité de cellules « instables » ayant perdu leur programme Foxp3 caractéristique. Les cellules stables présentaient une empreinte bien plus marquée de signalisation IL-2 et des niveaux plus élevés de récepteurs à l’IL-2, ce qui suggère que la capacité à détecter des quantités d’IL-2 rares est centrale pour survivre dans cet environnement stressant.
Contrôle local des rechutes depuis l’intérieur du cerveau
Pour tester si ces cellules T régulatrices résidentes sont réellement importantes pour le contrôle à long terme de la maladie, les chercheurs les ont éliminées sélectivement du SNC à l’aide d’une toxine délivrée directement dans le liquide cérébrospinal, tout en laissant la plupart des cellules T régulatrices systémiques intactes ailleurs dans l’organisme. En quelques jours, des souris en convalescence ont développé de sévères rechutes avec une paralysie renouvelée. En revanche, l’élimination des cellules T régulatrices uniquement dans le corps, en épargnant celles du SNC, n’a pas déclenché de flambées. La rechute impliquait une réactivation rapide et une expansion de cellules T effectrices déjà présentes dans le SNC, même lorsque leur recrutement depuis le sang était bloqué. Cela démontre que ce sont les cellules T régulatrices locales, et non les circulantes, qui sont essentielles pour maîtriser les cellules agressives résiduelles qui persistent après la phase aiguë.
Comment une enzyme protège les cellules régulatrices
En approfondissant, les auteurs ont cherché des molécules qui distinguent les cellules T régulatrices du SNC tolérantes au stress. Un acteur clé a émergé : CD38, une enzyme de surface qui dégrade le NAD+ extracellulaire. Dans le SNC enflammé, les cellules T régulatrices augmentaient fortement l’expression de CD38, tandis que les cellules T conventionnelles ne montraient pas un tel changement marqué. Lorsque l’équipe a transféré des cellules T régulatrices réactives au myéline dépourvues de CD38 chez des souris, ces cellules atteignaient le SNC mais ne parvenaient pas à contrôler la maladie, contrairement à leurs homologues normales. Chez des animaux chimériques mixtes, où seules les cellules T régulatrices résidentes étaient déficientes en CD38, la suppression de la fraction suffisante en CD38 était suffisante pour provoquer des rechutes, montrant que CD38 agit de manière intrinsèque à la cellule pour permettre un contrôle efficace.
Protéger le signal vital
Des expériences mécanistiques ont révélé comment CD38 confère cette résilience. Des niveaux élevés de NAD+ dans le SNC peuvent alimenter la modification chimique des protéines de surface par l’enzyme ARTC2.2. Une cible sensible est la sous-unité à haute affinité du récepteur à l’IL-2, que les cellules T régulatrices expriment à des niveaux très élevés, surtout lorsqu’elles reconnaissent des antigènes cérébraux. Dans les cellules T régulatrices déficientes en CD38 exposées au NAD+, la plupart des récepteurs à l’IL-2 étaient modifiés, conduisant à une activation plus faible du messager en aval STAT5 et à une réactivité réduite à l’IL-2. Au contraire, les cellules exprimant CD38 diminuaient localement le NAD+ autour d’elles, limitant cette modification néfaste et préservant une signalisation IL-2 robuste. Chez la souris vivante, l’injection de NAD+ dans le cerveau tua sélectivement la plupart des cellules T régulatrices via cette voie, tout en épargnant les cellules T conventionnelles, soulignant à quel point la niche est précaire sans cette enzyme protectrice. 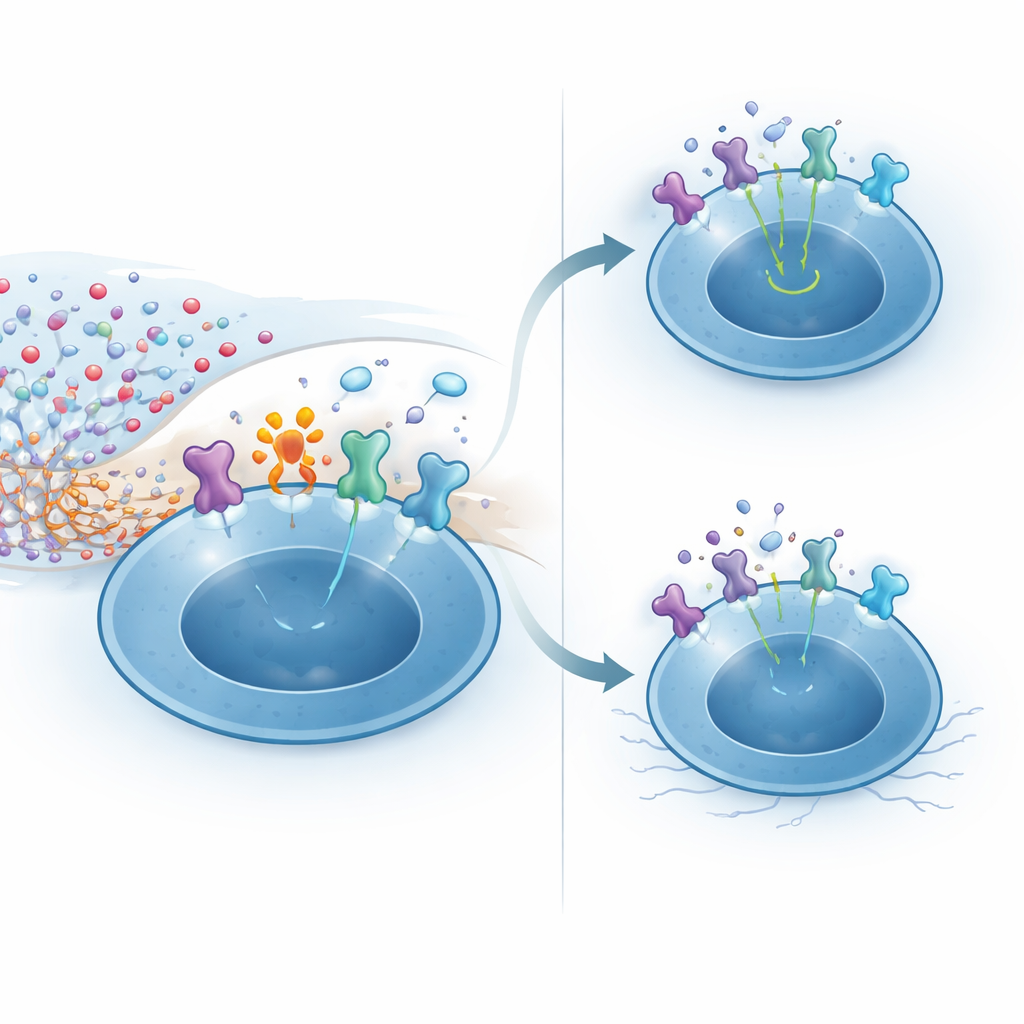
Ce que cela signifie pour l’auto-immunité cérébrale chronique
Ce travail décrit l’auto-immunité chronique du SNC comme une bataille compartimentalisée : de petits amas de cellules T agressives résiduelles résident dans le cerveau et la moelle épinière, retenues en respect par des cellules T régulatrices locales tout aussi spécialisées. Ces gardiens sont « tolérants au stress » parce que CD38 leur permet de survivre à des niveaux élevés de NAD+ et de continuer à détecter de faibles quantités d’IL-2, préservant ainsi leur identité et leur fonction suppressive. Pour un lectorat non spécialiste, la conclusion clé est que le contrôle à long terme de maladies comme la sclérose en plaques pourrait dépendre moins du système immunitaire circulant et davantage de l’entretien et de la protection de ces gardiens résidents au sein même du cerveau — potentiellement en ciblant des voies qui renforcent la fonction de CD38 ou la sensibilité à l’IL-2 dans les cellules T régulatrices.
Citation: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Mots-clés: cellules T régulatrices, sclérose en plaques, inflammation du système nerveux central, enzyme CD38, tolérance immunitaire